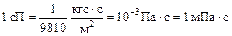Соотношения между единицами измерения
ТАБЛИЦЫ, РАСЧЕТНЫЕ НОМОГРАММЫ И ДИАГРАММЫ ПО КУРСУ
«ПРОЦЕССЫ И АППАРАТЫ ХИМИЧЕСКОЙ ТЕХНОЛОГИИ»
Справочно-методическое пособие
Для студентов химических специальностей всех форм обучения
Утверждено
редакционно-издательским
советом университета
Протокол № 3 от 02.10.2003
Харьков 2003
УДК 541.10/083
Рецензенты: д-р техн. наук, проф. Шапорев В.П.
Составители: Товажнянский Л.Л.
Лещенко В.А.,
Рябова И.Б.,
Дуравкина Г.Л.,
Новикова Г.С.,
Горбунов К.А.
Таблицы, расчетные номограммы и диаграммы по курсу «Процессы и аппараты химической технологии», справочно-методическое пособие /Тожнянский Л.Л., Лещенко В.А. и др. – Харьков: НТУ «ХПИ», 2003. – 96 с. На рус. яз.
В справочном издании приведены таблицы, диаграммы, номограммы для определения физико-химических свойств и других характерных параметров различных веществ.
Предназначено для студентов химических специальностей.
Табл. 59. Ил. 51. Библиогр. 4 назв.
ПРЕДИСЛОВИЕ
Для изучения дисциплины «Процессы и аппараты химической технологии» чрезвычайно важно освоение студентами инженерных методов расчета при решении задач на практических занятиях, выполнении лабораторного практикума и курсовом проектировании.
Выполнение практических расчетов позволяет понять физико-химическую сущность процессов, определить их важнейшие параметры или характеристики, приобрести необходимые расчетные навыки.
Для выполнения расчетов необходимо использовать обширный перечень физико-химических свойств большого количества веществ, которые представлены в специальной справочной литературе.
В предлагаемом пособии представлены таблицы, номограммы и диаграммы, которые содержат информацию о свойствах веществ и других характерных параметрах, необходимых для выполнения инженерных расчетов основных гидромеханических, тепловых и массообменных процессов. Номограммы и диаграммы снабжены схемой поясняющей принцип определения параметров или свойств веществ, а также коэффициентами для пересчета величин в СИ.
Данное пособие может быть использовано при изучении других учебных дисциплин и выполнении различных инженерных расчетов.
Соотношения между единицами измерения
| Величины
| Единицы измерения в СИ
| Соотношение между единицами измерения в СИ и наиболее часто встречающимися единицами других систем и внесистемными
| | Длина
| м
| 1 мкм = 10–6 м
| | 1 Å = 10–10 м
| | 1 ft = 0,3048 м
| | 1 in = 25,4×10–3 м
| | Масса
| кг
| 1 т = 1000 кг
| | 1 ц = 100 кг
| | 1 lb = 0,454 кг
| | Температура
| K
| t °C = (t + 273,15) K
| 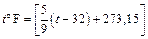 K K
| | Угол плоский
| рад
|  рад рад
|  рад рад
| | 1 оборот = 2p рад = 6,28 рад
| | Вес (сила тяжести)
| Н
| 1 кг = 9,81 Н
| | 1 дин = 10–5 Н
| | 1 стен = 103 Н
| | 1 lbf = 4,45 Н
| | Вязкости коэффициент динамический
| Па × с
| 1 П = 1 дин×с/см2 = 0,1 Па×с
| 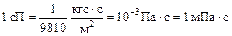
| | 1 lbf×s/ft2 = 47,88 Па×с
| | Вязкости коэффициент кинематический
| м2/с
| 1 Ст = 1 см2/с = 10–4 м2/с
| | 1 ft2/s = 0,093 м2/с
| | 1 ft2/h = 25,81 м2/с
| | Давление
| Па
| 1 бар = 105 Па
| | 1 мбар = 100 Па
| | 1 дин/см2 = 1 мкбар = 0,1 Па
| | 1 кгс/см2 = 1 ат = 9,81×104 Па = 735 мм рт. ст.
| | 1 кгс/м2 = 9,81 Па
| | 1 мм вод. ст. = 9,81 Па
| | 1 мм рт. ст. = 133,3 Па
| | 1 lbf/in2 = 6894,76 Па
| | 1 lbf/ft2 = 47,88 Па
| | Диффузии коэффициент
| м2/с
| 1 ft2/s = 0,0929 м2/с
| | Мощность
| Вт
| 1 кгс×м/с = 9,81 Вт
| | 1 эрг/с = 10–7 Вт
| | 1 ккал/ч = 1,163 Вт
| | 1 lbf×ft/s = 1,356 Вт
| | Натяжение поверхностное
| Н/м
| 1 кгс/м = 9,81 Дж/м2
| | 1 эрг/см2 = 1 дин/см = 10–3 Дж/м2 = 10–3 Н/м
| |
|
|
| | Объем
| м3
| 1 л = 10–3 м3 = 1 дм3
| | 1 ft3 = 28,3 дм3 = 2,83×10–2 м3
| | 1 in3 = 16,387 см3 = 16,39×10–6 м3
| | Объем удельный
| м3/кг
| 1 м3/т = 10–3 м3/кг
| | 1 дм3/кг = 1 см3/г = 10–3 м3/кг
| | Плотность
| кг/м3
| 1 т/м3 = 1 кг/дм3 = 1 г/см3 = 103 кг/м3
| | 1 кгс×с2/м4 = 9,81 кг/м3
| | 1 lb/ft3» 16,02 кг/м3
| | 1 lb/in3» 27,68×103 кг/м3
| | Плотность теплового потока (теплонапряжение, удельная тепловая нагрузка
| Вт/м2
| 1 ккал/(м2×ч) = 1,163 Вт/м2
| | Площадь
| м2
| 1 ft2 = 0,0929 м2
| | 1 in2 = 6,451×10–4 м2
| | Работа, энергия, количество теплоты
| Дж
| 1 кгс×м = 9,81 Дж
| | 1 эрг = 10–7 Дж
| | 1 кВт×ч = 3,6×106 Дж
| | 1 ккал = 4,1868×103 Дж = 4,19 кДж
| | 1 lbf×ft = 1,356 Дж
| | 1 lbf×in = 0,113 Дж
| | 1 BTU = 1055,1 Дж
| | Расход массовый
| кг/с
| 1 lb/s = 0,454 кг/с
| | 1 b/h = 1,26 ×10–4 кг/с
| | Расход объемный
| м3/с
| 1 л/мин = 16,67×10–6 м3/с
| | 1 ft3/s = 28,3×10–3 м3/с
| | 1 in3/s = 16,4×10–6 м3/с
| | Скорость линейная
| м/с
| 1 ft/s = 0,3048 м/с
| | Скорость угловая
| рад/с
| 1 об/мин = π/30 рад/с
| | 1 об/с = 2p рад/с
| | Теплоемкость удельная массовая
| Дж/(кг×K)
| 1 ккал/(кг×°С) = 4,19 кДж/(кг×K)
| | 1 эрг/ (г × K) = 10–4 Дж/ (кг × K)
| | BTU/lb·deg F = 4,19 Дж/ (кг × K)
| | Теплоотдачи коэффициент, теплопередачи коэффициент
| Вт/(м2×K)
| 1 ккал/(м2·ч·°С) = 1,163 Вт/(м2×K)
| | 1 BTU/ (ft2× h× deg F) = 5,6 Вт/(м2×K)
| | Теплопроводности коэффициент
| Вт/(м×K)
| 1 ккал/ (м×ч×°С) = 1,163 Вт/(м×K)
| | 1 BTU/ (ft× h× deg F) = 1,73 Вт/(м×K)
| | Теплота удельная (фазового превращения)
| Дж/кг
| 1 ккал/кг = 1 кал/г = 4,19 кДж/кг
| | 1 ВТU/ lb = 2326 Дж/кг
| | Ускорение линейное
| м/с2
| 1 in/s2 = 25,4 × 10–3 м/с2
| | 1 ft/s2 = 0,3048 м/с2
| | Частота
| Гц
| 1 Гц = 1 с–1
| | 1 об/с = 1 Гц
| | 1 об/мин = 1/60 Гц
| | Энтальпия удельная
| Дж/кг
| 1 ккал/кг = 1 кал/г = 4,19 кДж/кг
| | 1 BTU/lb = 2326 Дж/кг
| | Энтропия удельная
| Дж/(кг× K)
| 1 ккал/ (кг×°С) = 4,19 кДж/ (кг× K)
| | 1 BTU/(lb × deg F) = 4,19 кДж (кг× K)
|
Таблица 1 – Атомные массы некоторых элементов по Международной таблице 1977 г.
| Наименование
| Символ
| Атомная масса
| Наименование
| Символ
| Атомная масса
| Наименование
| Символ
| Атомная масса
| | Азот
| N
| 14,0067
| Кальций
| Ca
| 40,08
| Радий
| Ra
| 226,0254
| | Алюминий
| Al
| 26,98154
| Кислород
| O
| 15,999
| Ртуть
| Hg
| 200,5
| | Аргон
| Ar
| 39,94
| Кобальт
| Co
| 58,9332
| Свинец
| Pb
| 207,2
| | Барий
| Ba
| 137,33
| Кремний
| Si
| 28,085
| Серебро
| Ag
| 107,868
| | Бериллий
| Be
| 9,01218
| Криптон
| Kr
| 83,80
| Сера
| S
| 32,06
| | Бор
| B
| 10,81
| Ксенон
| Xe
| 131,30
| Стронций
| Sr
| 87,62
| | Бром
| Br
| 79,904
| Литий
| Li
| 6,94
| Сурьма
| Sb
| 121,7
| | Ванадий
| V
| 50,9415
| Магний
| Mg
| 24,305
| Титан
| Ti
| 47,90
| | Висмут
| Bi
| 208,9804
| Марганец
| Mn
| 54,9380
| Углерод
| C
| 12,011
| | Водород
| H
| 1,0079
| Медь
| Cu
| 63,54
| Уран
| U
| 238,02
| | Гелий
| He
| 4,00260
| Молибден
| Mo
| 95,94
| Фосфор
| P
| 30,97376
| | Железо
| Fe
| 55,84
| Мышьяк
| As
| 74,9216
| Фтор
| F
| 18,998403
| | Золото
| Au
| 196,9665
| Натрий
| Na
| 22,98977
| Хлор
| Cl
| 35,453
| | Иод
| I
| 126,9045
| Никель
| Ni
| 58,70
| Хром
| Cr
| 51,996
| | Кадмий
| Cd
| 112,41
| Олово
| Sn
| 118,6
| Цинк
| Zn
| 65,38
| | Калий
| K
| 39,098
| Платина
| Pt
| 195,0
|
|
|
|
Таблица 2 – Физические свойства воды (на линии насыщения).
Пересчет в СИ: 1кгс/см2 = 9,81.104 Па
| P, кгс/см2
| t, °С
| r, кг/м3
| i, кДж/(кг×К)
| c, кДж/(кг×К)
| λ×102, Вт/(м×К)
| α∙107, м2/с
| μ∙106, Па∙с
| ν∙106, м2/с
| β∙106, К–1
| σ∙106, кг/с2
| Рr
| |
|
|
|
| 4,23
| 55,1
| 1,31
|
| 1,79
| –0,63
|
| 13,7
| |
|
|
| 41,9
| 4,19
| 57,5
| 1,37
|
| 1,31
| +0,70
|
| 9,52
| |
|
|
| 83,8
| 4,19
| 59,9
| 1,43
|
| 1,01
| 1,82
|
| 7,02
| |
|
|
|
| 4,18
| 61,8
| 1,49
|
| 0,81
| 3,21
|
| 5,42
| |
|
|
|
| 4,18
| 63,4
| 1,53
|
| 0,66
| 3,87
|
| 4,31
| |
|
|
|
| 4,18
| 64,8
| 1,57
|
| 0,556
| 4,49
|
| 3,54
| |
|
|
|
| 4,18
| 65,9
| 1,61
|
| 0,478
| 5,11
|
| 2,98
| |
|
|
|
| 4,19
| 66,8
| 1,63
|
| 0,415
| 5,70
|
| 2,55
| |
|
|
|
| 4,19
| 67,5
| 1,66
|
| 0,365
| 6,32
|
| 2,21
| |
|
|
|
| 4,19
| 68,0
| 1,68
|
| 0,326
| 6,95
|
| 1,95
| | 1,03
|
|
|
| 4,23
| 68,3
| 1,69
|
| 0,295
| 7,5
|
| 1,75
| | 1,46
|
|
|
| 4,23
| 68,5
| 1,69
|
| 0,268
| 8,0
|
| 1,58
| | 2,02
|
|
|
| 4,23
| 68,6
| 1,72
|
| 0,244
| 8,6
|
| 1,43
| | 2,75
|
|
|
| 4,27
| 68,6
| 1,72
|
| 0,226
| 9,2
|
| 1,32
| | 3,68
|
|
|
| 4,27
| 68,5
| 1,72
|
| 0,212
| 9,7
|
| 1,23
| | 4,85
|
|
|
| 4,32
| 68,4
| 1,72
|
| 0,202
| 10,3
|
| 1,17
| | 6,30
|
|
|
| 4,36
| 68,3
| 1,72
|
| 0,191
| 10,8
|
| 1,10
| | 8,08
|
|
|
| 4,40
| 67,9
| 1,72
|
| 0,181
| 11,5
|
| 1,05
| | 10,23
|
|
|
| 4,44
| 67,5
| 1,72
|
| 0,173
| 12,2
|
| 1,01
|
Таблица 3 – Основные физические свойства некоторых газов.
Пересчет в СИ: 1 мм.рт.ст = 133,3 Па; 1 кгс/см2 = 9,81 104.
| Название
| Формула
| Плотность при 0°С и 760 мм рт. ст., кг/м3
| Молекулярная масса, кг/кмоль
| Удельная теплоемкость при 20°С и rабс»0,1 Мпа, кДж/(кг×К)
| k = cr/cv
| Температура кипения при 760 мм.рт.ст., кДж/кг
| Удельная теплота испарения при 760 мм рт.ст,. кДж/кг
| Критические точки
| Вязкость μ0 при 0°С и rабс=1кгс/см2
| | ср
| cv
| температура, °С
| давление (абс.), кгс/см2
| 106 Па×с
| константа С ур-я (1.13)
| | Азот
| N2
| 1,25
|
| 1,05
| 0,746
| 1,40
| –195,8
| 199,4
| –147,1
| 33,49
|
|
| | Аммиак
| NH3
| 0,77
|
| 2,22
| 1,68
| 1,29
| –33,4
|
| +132,4
| 111,5
| 9,18
|
| | Аргон
| Ar
| 1,78
| 39,9
| 0,53
| 0,323
| 1,66
| –185,9
|
| –122,4
| 48,00
| 20,9
|
| | Ацетилен
| C2H2
| 1,171
| 26,0
| 1,68
| 1,36
| 1,24
| –83,7 (возг.)
|
| +35,7
| 61,6
| 9,35
|
| | Бензол
| C6H6
| —
| 78,1
| 1,25
| 1,140
| 1,1
| +80,2
|
| +288,5
| 47,7
| 7,2
| —
| | Бутан
| C4H10
| 2,673
| 58,1
| 1,92
| 1,80
| 1,08
| –0,5
|
| +152
| 37,5
| 8,1
|
| | Воздух
| —
| 1,293
| (29,0)
| 1,01
| 0,721
| 1,40
| –195
|
| –140,7
| 37,2
| 17,3
|
| | Водород
| H2
| 0,0899
| 2,02
| 14,3
| 10,140
| 1,407
| –252,8
|
| –239,9
| 12,80
| 8,42
|
| | Гелий
| He
| 0,179
| 4,0
| 5,28
| 3,18
| 1,66
| –268,9
| 19,5
| –268,0
| 2,26
| 18,8
|
| | Диоксид азота
| NO2
| —
| 46,0
| 0,804
| 0,62
| 1,31
| +21,2
|
| +158,2
| 100,00
| —
| —
| | Диоксид серы
| SO2
| 2,93
| 64,1
| 0,633
| 0,503
| 1,25
| –10,8
|
| +157,5
| 77,78
| 11,7
|
| | Диоксид углерода
| CO2
| 1,98
| 44,0
| 0,838
| 0,654
| 1,30
| –78,2 (возг.)
| 574,0
| +31,1
| 72,9
| 13,7
|
| | Кислород
| O2
| 1,429
|
| 0,913
| 0,654
| 1,40
| –183,0
|
| –118,8
| 49,71
| 20,3
|
| | Метан
| CH4
| 0,72
| 16,0
| 2,23
| 1,70
| 1,31
| –161,6
|
| –82,15
| 45,6
| 10,3
|
| | Оксид углерода
| CO
| 1,25
| 28,0
| 1,05
| 0,754
| 1,40
| –191,5
|
| –140,2
| 34,53
| 16,6
|
| | Пентан
| C5H12
| —
| 72,2
| 1,72
| 1,58
| 1,09
| +36,1
|
| 197,1
| 33,0
| 8,74
| —
| | Пропан
| C3H8
| 2,02
| 44,1
| 1,87
| 1,65
| 1,13
| –42,1
|
| 95,6
|
| 7,95 (18°С)
|
| | Пропилен
| C3H6
| 1,91
| 42,1
| 1,63
| 1,44
| 1,17
| –47,7
|
| 91,4
| 45,4
| 8,35 (20°С)
|
| | Сероводород
| H2S
| 1,54
| 34,1
| 1,060
| 0,804
| 1,30
| –60,2
|
| 100,4
| 188,9
| 11,66
| —
| | Хлор
| C12
| 3,22
| 70,9
| 0,482
| 0,355
| 1,36
| –33,8
|
| 144,0
| 76,1
| 12,9 (16°С)
|
| | Хлористый метил
| CH3Cl
| 2,3
| 50,5
| 0,742
| 0,582
| 1,28
| –21,4
|
|
| 66,0
| 9,89
|
| | Этан
| C2H6
| 1,36
| 30,1
| 1,73
| 1,45
| 1,20
| –88,50
|
| 32,1
| 48,85
| 8,5
|
| | Этилен
| C2H4
| 1,26
| 28,1
| 1,53
| 1,26
| 1,20
| –103,7
|
| 9,7
| 50,7
| 9,85
|
|

Обзор компонентов Multisim Компоненты – это основа любой схемы, это все элементы, из которых она состоит. Multisim оперирует с двумя категориями...
|

Композиция из абстрактных геометрических фигур Данная композиция состоит из линий, штриховки, абстрактных геометрических форм...
|

Важнейшие способы обработки и анализа рядов динамики Не во всех случаях эмпирические данные рядов динамики позволяют определить тенденцию изменения явления во времени...
|

ТЕОРЕТИЧЕСКАЯ МЕХАНИКА Статика является частью теоретической механики, изучающей условия, при которых тело находится под действием заданной системы сил...
|
Субъективные признаки контрабанды огнестрельного оружия или его основных частей
Переходя к рассмотрению субъективной стороны контрабанды, остановимся на теоретическом понятии субъективной стороны состава преступления...
ЛЕЧЕБНО-ПРОФИЛАКТИЧЕСКОЙ ПОМОЩИ НАСЕЛЕНИЮ В УСЛОВИЯХ ОМС 001. Основными путями развития поликлинической помощи взрослому населению в новых экономических условиях являются все...
МЕТОДИКА ИЗУЧЕНИЯ МОРФЕМНОГО СОСТАВА СЛОВА В НАЧАЛЬНЫХ КЛАССАХ В практике речевого общения широко известен следующий факт: как взрослые...
|
ОСНОВНЫЕ ТИПЫ МОЗГА ПОЗВОНОЧНЫХ Ихтиопсидный тип мозга характерен для низших позвоночных - рыб и амфибий...
Принципы, критерии и методы оценки и аттестации персонала
Аттестация персонала является одной их важнейших функций управления персоналом...
Пункты решения командира взвода на организацию боя. уяснение полученной задачи; оценка обстановки; принятие решения; проведение рекогносцировки; отдача боевого приказа; организация взаимодействия...
|
|

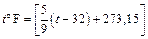 K
K
 рад
рад
 рад
рад