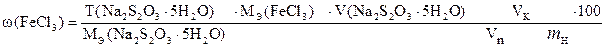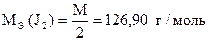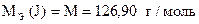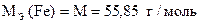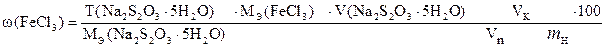| Стандартный раствор:
| тиосульфат натрия.
|
| Индикатор:
| крахмал.
|
| Способ титрования:
| замещение.
|
| Способ взятия навески:
| пипетирование.
|
2FeCl3 + 2KJ = 2FeCl2 + J2 + 2KCl
|
| Fe3+ + 1e- = Fe2+
|
|
| 2J- - 2e- = J2
|
|
| 2Fe3+ + 2J- = 2Fe2+ + J2
|
j0 J2 / 2J- = + 0,536 B
j0 Fe3+ / Fe2+ = + 0,77 B
Dj = 0,77 - 0,536 = 0,234 B
Выделяется J2 в количестве, эквивалентном взятому FeCl3, содержащемуся в объеме пипетки.
J2 + 2Na2S2O3 = Na2S4O6 + 2NaJ
|
| 2S2O32- – 2e- = S4O62-
|
|
| J2 + 2e- = 2J-
|
|
| 2S2O32- + J2 = S4O62- + 2J-
|
|
j 0 S4O62-/ 2S2O32- = + 0,09 В
j0 J2 / 2J- = + 0,536 B
Dj = 0,536 - 0,09 = 0,446 B
| 
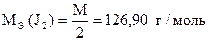
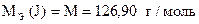


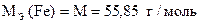
|