Аномальные свойства воды.
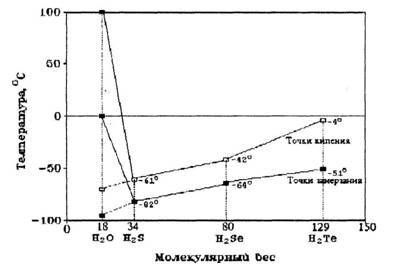
Исследуя воду и, особенно ее водные растворы, ученые раз за разом убеждались, что вода обладает ненормальными — аномальными свойствами, присущими только ей, ее Величеству — Воде, подарившей нам Жизнь и возможность мыслить. Мы даже и не подозреваем, что столь привычные и естественные свойства воды в природе, в различных технологиях, наконец, в обыденной жизни нашей являются уникальными и неповторимыми. Ученые согласны в том, что вода является одним из самых трудных объектов исследования, так как, прежде всего в воде всегда есть примеси и что она обладает кооперативным характером взаимодействия ее молекул. В рамках микроскопического подхода структура воды отличается относительно беспорядочным динамически меняющимся расположением молекул, а высокая плотность обуславливает сильное межмолекулярное взаимодействие, осуществляемое посредством водородных связей. Таким образом, вода представляет собой сложную ассоциированную жидкость с тетраэдрической сеткой молекул, соединенных водородными связями. В результате теплового движения молекул эта сетка подвержена спонтанной перестройке. В трехмерной сетке водородных связей размещены флуктуационные микрообъемы молекул воды, обладающие сравнительно малой энергией теплового движения и более высокой степенью структурного упорядочения. Это — микрокластеры. В то же время вокруг микрокластеров в макрообъеме ассоциированной среды с повышенной энергией теплового движения молекул Н20 наблюдается большая степень структурной беспорядочности, то есть более низкий уровень структурного упорядочения. Вещества — аналоги воды, молекулы которых по химическому составу похожи на воду, — H2S, H2Se, H2Te, то есть соединения водорода и серы, водорода и селена, водорода и теллура и так далее, при комнатной температуре находятся в газообразном состоянии. Казалось бы, вода, сохрани она такие же свойства, должна бы закипать при температуре -70°С, а превращаться в лед при -90 °С. Эти условия вряд ли бы способствовали развитию жизни на Земле, ведь она должна была бы существовать в интервале температур от -70 °С до -90 °С (рис.3). В таком холоде разве возможна жизнь?
Иначе говоря, если бы вода — гидрид кислорода Н2О — была бы нормальным мономолекулярным соединением, таким, например, как ее аналоги по шестой группе Периодической системы элементов Д.И.Менделеева — гидрид серы H2S, гидрид селена H2Se, гидрид теллура H2Te, то в жидком состоянии вода существовала бы в пределах от минус 95 °С до минус 70 °С, а не такая, какая реально существует сейчас. Нетрудно понять, что в этом случае биологической жизни на Земле не могло бы существовать. На рис.3 показаны необычные точки замерзания и кипения воды по сравнению с другими жидкостями.
Аномалии точек кипения и замерзания воды по сравнению с другими соединениями водорода.
Но, к счастью для нас и для всего живого на свете вода обладает аномальными свойствами. Вода «не признает» периодических закономерностей, характерных для бесчисленного множества соединений на Земле и в Космосе, а следует своим, еще не вполне понятным для науки законам, подарившим нам удивительный «мир Жизни». «Ненормальные» температуры плавления (0 °С) и кипения (+100 °С) воды далеко не единственная ее аномальность. Для всей биосферы исключительна важной особенностью воды является ее способность при замерзании увеличивать, а не уменьшать свой объем, то есть уменьшать плотность. Действительно, при переходе любой жидкости в твердое состояние молекулы располагаются теснее, а само вещество, уменьшаясь в объеме, становится плотнее. Да, для любой из необозримо разных жидкостей, но не воды. Вода и здесь представляет исключение.
При охлаждении вода сначала ведет себя как и другие жидкости: постепенно уплотняясь, уменьшает свой объем. Такое явление можно наблюдать до +3,98 °С. Затем, при дальнейшем снижении температуры до 0 °С, вся вода замерзает и расширяется в объеме. В результате удельный вес льда становится меньше воды и лед плавает. Если бы лед не всплывал, а тонул, то все водоемы (реки, озера, моря) промерзли бы до дна, испарение бы резко сократилось, все пресноводные животные и растения погибли бы. Жизнь на Земле стала бы невозможной.
Вода — единственная жидкость на Земле, лед которой не тонет за счет того, что его объем на 1/11 больше объема воды. Еще одно удивительное свойство воды — ее огромное поверхностное натяжение. Благодаря тому, что круглые шарики воды очень упруги, идет дождь, выпадает роса.Что же это за удивительная сила, которая сохраняет капли росы, а поверхностный слой воды в любой лужице делает эластичным и относительно прочным? Известно, что если стальную иголку осторожно положить на поверхность воды, налитой в блюдце, то иголка не тонет. А ведь удельная масса металла значительно больше, чем у воды. Молекулы воды связаны силой поверхностного натяжения, которая позволяет им подниматься вверх по капиллярам, преодолевая силу земного притяжения. Без этого свойства воды жизнь на Земле была бы также невозможна. Ни одно вещества на Земле не обладает такой способностью поглощать тепло, как вода. Для превращения в пар 1г воды требуется 537 калории тепла. Конденсируясь, пар возвращает эти 537 калорий в окружающую среду. Ни одно вещество в мире не поглощает и не отдает среде столько тепла, сколько вода. Теплоемкость воды в 10 раз больше теплоемкости стали и в 30 раз больше ртути. Вода сохраняет тепло на Земле. С поверхности морей, океанов, суши испаряется за год 520000 кубических километров воды, которые, конденсируясь, отдают много тепла холодным и полярным регионам.
Не обладай вода такой уникальной способностью поглощать и отдавать тепло, климат Земли оказался бы непригодным для существования человека. В высоких широтах тогда царил бы нестерпимый холод, а в низких — солнце испепелило бы все живое. Благодаря наземному Мировому океану атмосфера представляет собой надежное теплое одеяло, укрывающее тело планеты и защищающее его от космического холода. Подземный океан снабжает Землю теплом из внутренних источников планеты. Ни одна жидкость не поглощает газы с такой жадностью, как вода. Но она их также легко отдает.
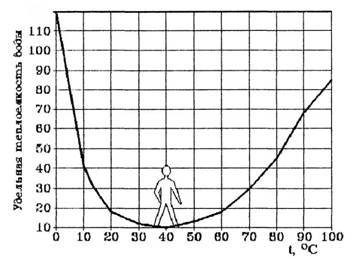
Дождь растворяет в себе все ядовитые газы атмосферы. Вода - ее мощный природный фильтр, очищающий атмосферу от всех вредных и ядовитых газов. Еще одно удивительное свойство воды проявляется при воздействии на нее магнитного поля. Вода, подвергнутая магнитной обработке, меняет растворимость солей и скорость химических реакций. Магнитная вода не только не дает накипи в котлах, но и срывает ранее образовавшиеся отложения, повышает прочность бетона, ускоряет его застывание, увеличивает процент выхода обогащенной руды. Ряд удивительных свойств воды связан с ее теплоемкостью. Легче всего вода нагревается и быстрее всего охлаждается в своеобразной “температурной яме”, соответствующей +37 °С, температуре человеческого тела (рис. 4). Как видно из рис.4, теплоемкость воды своих минимальных значений достигает около +37 °С. Это нормальная температура тела человека. Именно при температуре 36,6-37оС сложнейшие реакции обмена веществ в организме человека наиболее интенсивны. Значит, при этой температуре организм человека находится в наивыгоднейшем энергетическом состоянии.
Температурная зависимость удельной теплоемкости воды.
Вода в организме человека составляет 70-90%. от веса тела. Не обладай вода такой теплоемкостью, как сейчас, обмен веществ в теплокровных и холоднокровных организмах был бы невозможен. В клетках живых организмов различают “объемную” и “связанную” воду. Первая — вода, с которой мы имеем дело в повседневной жизни. В ней растворен цитозоль клетки. Под “связанной” водой мы понимаем воду, связанную с биологическими молекулами, мембранами. В живых клетках обычная вода, будучи связанной с мембранами, неизвестным образом превращается в воду со структурой льда. И она уже не во власти незыблемых законов физики — все ее свойства коренным образом меняются. Диэлектрическая проницаемость, например, уменьшается в десять раз, а теплопроводность возрастает в семьдесят раз и тому подобное. Любая живая клетка имеет наружную и внутреннюю биологические мембраны. Это как бы избирательно проницаемая стенка, ограждающая содержимое клетки, ее органоиды от повреждения. На поверхности биологических образований молекулы воды подвергаются структурно -функциональной упорядоченности, образуют так называемую клатратную пленку — кристаллогидрат со строго ориентированными дипольными моментами молекул воды. В самой клатратной пленке, размещенной, к примеру, на поверхности клеточной мембраны, процессы обмена между молекулами воды осуществляются с частотой десять тысяч раз в секунду, в то время как с окружающей объемной водой молекулы Н2О меняются местами с частотой в два раза меньшей. Это приводит к тому, что растворенным в воде примесям термодинамически невыгодно находиться в клатратных слоях воды, поэтому они предпочитают объемную воду. Итак, будучи связанной с живой материей и защищая ее, клатраты сами защищены невидимым барьером от разрушающего действия на них объемной воды с растворенными в ней вредными и ядовитыми веществами. И чем толще и крепче клатратная прослойка, тем более стабильны термодинамические и биологические условия функционирования отдельной молекулы и клетки организма. В связанной воде все молекулы Н2О имеют по четыре водородные связи и обеспечивают оптимальную скорость миграции протонов и электронов -эту основу обмена веществ в живых системах.
Заключение.
Обнаружена и изучается универсальная система водно-структурной регуляции жизненными процессами. Структура воды и растворенные в ней вещества (анионы и катионы) определяют и регулируют строение и функции макромолекул клетки и низкомолекулярных биорегуляторов, сборку и функционирование организмов и клеток, тканей, органов и систем органов, наконец, целого организма.
Она действует как на субмолекулярном и молекулярном, так и на более высоких уровнях организации живой материи, вплоть до биосферного. Она определяет миграцию протонов и электронов в клетках, структуру мембран, функции ДНК, РНК, белков, низкомолекулярных регуляторов, сборку клеточных структур, оплодотворение, эмбриональное развитие, зрелое функционирование организма, его управляющие, регуляторные и гомеостатические системы, его старение и смерть.
Таким образом, аномальные и специфические свойства воды играют ключевую роль в ее многообразном взаимодействии с живой и неживой природой. Все эти необычные особенности свойств воды настолько "удачны" для всего живого, что делает воду незаменимой основой существования жизни на Земле.
Мы вправе рассматривать воду как необъятную самостоятельную область познания — безбрежный океан, усыпанный белыми пятнами загадок. И едва удается раскрыть одну загадку, как появляется две, десять новых, еще более невероятных»
Список использованной литературы
1. Арабаджи В. И. Загадки простой воды. - М.: «Знание», 2003г. 2. http://voda.biz-at-home.ru/novosti/anomalnyie-svoystva-vodyi 3. Петрянов И.В. Самое необыкновенное вещество в мире - М.: «Педагогика», 2005г. 4. http://www.sunhome.ru/journal/119584 5. Бернал Дж. Д. Геометрия построек из молекул воды. Успехи химии, 1956
Министерство Образования и Науки Республики Казахстан Евразийский Национальный Университет им. Л.Н.Гумилева
Реферат «Окислительно-восстановительные процессы»
Выполнил: Саубаев М.Е. ТЭ-12. Проверила: доцент к.х.н. Кусепова Л.А.
Астана 2012
|