
Головна сторінка Випадкова сторінка
КАТЕГОРІЇ:
АвтомобіліБіологіяБудівництвоВідпочинок і туризмГеографіяДім і садЕкологіяЕкономікаЕлектронікаІноземні мовиІнформатикаІншеІсторіяКультураЛітератураМатематикаМедицинаМеталлургіяМеханікаОсвітаОхорона праціПедагогікаПолітикаПравоПсихологіяРелігіяСоціологіяСпортФізикаФілософіяФінансиХімія
For Whom The Bell Tolls 15 страница
Дата добавления: 2015-08-29; просмотров: 499
|
|
Влияние температуры на скорость химической реакции выражается уравнением Аррениуса:

где k - константа скорости реакции; А - предэкспоненциальный множитель, называемый также частотным или стерическим фактором; Е- энергия активации реакции.
Полимеризация включает несколько элементарных реакций. Для того, чтобы получить соотношение, связывающее суммарное значение энергии активации полимеризации с энергиями активации элементарных реакций, запишем уравнение начальной скорости полимеризации
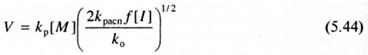
в логарифмической форме, заменив при этом kp, ko, kрасп на их выражения, следуемые из уравнения Аррениуса. В результате получаем:
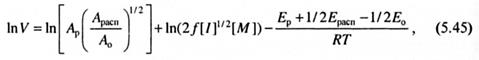
где Aрасп, Ар, Ао - частотные факторы, a Eрасп Ep, Ео - энергии активации реакций распада инициатора, роста и обрыва цепи. Напомним, что скорость распада инициатора определяет скорость инициирования, поэтому Epacn=Eин, Aрасп=Aин. Сопоставим уравнение (5.45) с уравнением Аррениуса, выраженным в логарифмической форме:

Оно показывает, что из экспериментальной зависимости скорости полимеризации от температуры, представленной в координатах lnV - 1/T, может быть определена суммарная энергия активации полимеризации 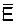 v, связанная с энергиями активации элементарных реакций соотношением:
v, связанная с энергиями активации элементарных реакций соотношением:
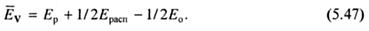
Влияние температуры на степень полимеризации в отсутствие заметной реакции передачи цепи может быть выявлено аналогичным образом, исходя из выражения (5.16), для длины кинетической цепи. Оно описывается соотношением:
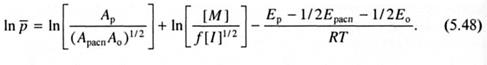
Из уравнений (5.46) и (5.48) следует, что суммарное значение энергии активации степени полимеризации, определенное из экспериментальной зависимости ln 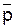 -1/T, равно:
-1/T, равно:
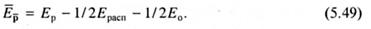
В том случае, когда молекулярная масса полимера контролируется передачей цепи на растворитель или регулятором молекулярной массы, всеми другими реакциями ограничения длины цепи можно пренебречь. Тогда, исходя из уравнения Майо (5.23), аналогичным путем легко можно получить:
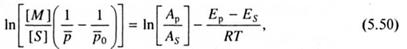
где AS, Es- предэкспоненциальный множитель и энергия активации реакции передачи цепи.
Используя известные значения энергетических параметров полимеризации, можно сделать следующие выводы о влиянии температуры на скорость и степень полимеризации:
1. Поскольку Eрасп обычно употребляемых инициаторов заключены в пределах 125-150 кДж/моль, а величины Eр и Ео, соответственно, в пределах 20-40 кДж/моль и 2-20 кДж/моль, суммарная энергия активации полимеризации наиболее распространенных мономеров составляет 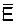 v≈80-90 кДж/моль. Это означает, что скорость полимеризации возрастает в 2 - 3 раза на 10°С, что примерно соответствует правилу Вант-Гоффа. Применение окислительно-восстановительных систем снижает
v≈80-90 кДж/моль. Это означает, что скорость полимеризации возрастает в 2 - 3 раза на 10°С, что примерно соответствует правилу Вант-Гоффа. Применение окислительно-восстановительных систем снижает 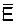 v примерно
v примерно
вдвое. Величина суммарной энергии активации степени полимеризации отрицательна и обычно близка к -60 кДж/моль, поэтому молекулярная масса полимера весьма заметно понижается с ростом температуры.
2. При фотохимической полимеризации Еин=0, поэтому скорость и степень полимеризации возрастают с ростом температуры вследствие положительной величины суммарной энергии активации, близкой к 20 кДж/моль.
3. Энергия активации реакции передачи цепи заметно превосходит энергию активации реакции роста, обычно Ер - Es = -(20 - 60) кДж/моль. Это означает в соответствии с (5.50), что при полимеризации в их присутствии повышение температуры приводит к уменьшению степени полимеризации.
Влияние давления на константу скорости химической реакции описывается выражением:

где 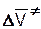 - активационный объем, т.е. разница объемов переходного комплекса и реагентов. Следовательно, влияние давления на скорость полимеризации будет определяться его влиянием на константы скорости элементарных реакций, входящие в уравнения (5.9) или (5.44). Исходя из этого и с учетом (5.51), имеем:
- активационный объем, т.е. разница объемов переходного комплекса и реагентов. Следовательно, влияние давления на скорость полимеризации будет определяться его влиянием на константы скорости элементарных реакций, входящие в уравнения (5.9) или (5.44). Исходя из этого и с учетом (5.51), имеем:
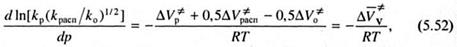
где 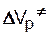 ,
, 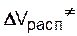 ,
, 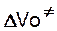 , - активационные объемы реакций распада инициатора, роста и обрыва цепи. Для большинства мономеров характерны следующие значения активационных объемов элементарных реакций:
, - активационные объемы реакций распада инициатора, роста и обрыва цепи. Для большинства мономеров характерны следующие значения активационных объемов элементарных реакций:
распад инициатора +(5-10) см3/моль,
рост цепи -(15-25) см3/моль,
обрыв цепи +(13-25) см3/моль,
что приводит к суммарной величине 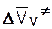 = -(11 -20) см3/моль. Это означает в соответствии с (5.51), что максимальный эффект от увеличения давления в 1000 раз - от 1 до 1000 МПа при 30-50 °С может соответствовать возрастанию скорости в 50 раз.
= -(11 -20) см3/моль. Это означает в соответствии с (5.51), что максимальный эффект от увеличения давления в 1000 раз - от 1 до 1000 МПа при 30-50 °С может соответствовать возрастанию скорости в 50 раз.
Объем переходного комплекса обычно превышает объем реагентов, когда реакция приводит к увеличению числа частиц, и наоборот. Поэтому следовало ожидать отрицательных значений активационного объема как для реакции роста, так и для реакции обрыва, поскольку в обоих случаях из двух частиц образуется одна. Однако в последнем случае 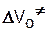 > 0, что находит простое объяснение. Увеличение давления вызывает рост вязкости реакционной смеси и, в соответствии с диффузионным механизмом обрыва, уменьшение скорости этой реакции. Такой результат в соответствии с (5.51) приводит к кажущимся положительным значениям
> 0, что находит простое объяснение. Увеличение давления вызывает рост вязкости реакционной смеси и, в соответствии с диффузионным механизмом обрыва, уменьшение скорости этой реакции. Такой результат в соответствии с (5.51) приводит к кажущимся положительным значениям 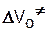 .
.
Влияние давления на степень полимеризации определяется его влиянием на константы элементарных реакций в уравнении средней длины кинетической цепи (в отсутствие реакции передачи цепи). Исходя из (5.16) и (5.51), имеем:
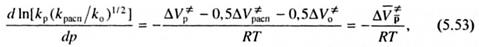
где 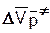 - средний активационный объем для степени полимеризации. Из приведенных выше значений активационных объемов элементарных реакций следует, что
- средний активационный объем для степени полимеризации. Из приведенных выше значений активационных объемов элементарных реакций следует, что 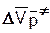 = -(19-30) см3/моль. Это означает, что с увеличением давления степень полимеризации должна возрастать быстрее, чем скорость. Однако экспериментальные данные не соответствуют этому выводу. Если скорость полимеризации с возрастанием давления увеличивается постоянно, то рост степени полимеризации замедляется и может прекратиться, что объясняется активизацией реакции передачи цепи.
= -(19-30) см3/моль. Это означает, что с увеличением давления степень полимеризации должна возрастать быстрее, чем скорость. Однако экспериментальные данные не соответствуют этому выводу. Если скорость полимеризации с возрастанием давления увеличивается постоянно, то рост степени полимеризации замедляется и может прекратиться, что объясняется активизацией реакции передачи цепи.
Давление также влияет на полимеризационно-деполимеризационное равновесие. Известно, что полимеризация ненасыщенных соединений сопровождается уменьшением объема на 15-25%. Из этого следует, что в соответствии с известным термодинамическим соотношением:

где Кравн - константа равновесия; ∆V- разность объемов конечных и исходных продуктов реакции, увеличение давления приводит к смещению константы равновесия в сторону образования полимера.
| <== предыдущая лекция | | | следующая лекция ==> |
| For Whom The Bell Tolls 14 страница | | | For Whom The Bell Tolls 16 страница |