КЛАССИФИКАЦИЯ, НОМЕНКЛАТУРА И СТРУКТУРНАЯ ИЗОМЕРИЯ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ. ЭЛЕКТРОННОЕ СТРОЕНИЕ АТОМОВ ЭЛЕМЕНТОВ-ОРГАНОГЕНОВ
Мотивация цели. Органические соединения очень многочисленны и разнообразны. Для их изучения необходимо иметь представление об их классификации и знать основные принципы химической номенклатуры. Химические свойства органических соединений обусловлены типом химических связей, природой связываемых атомов и их взаимным влиянием. А это, в свою очередь, определяется электронным строением атомов и взаимодействием их атомных орбиталей. Цель самоподготовки. В процессе самоподготовки следует усвоить классификацию и изомерию химических соединений и принципы заместительной номенклатуры IUPAC, электронное строение атомов углерода, водорода, азота и кислорода, типы их гибридизации. План изучения темы 1. Классификация органических соединений. 1.1. Классификация по строению углеродного скелета. 1.2. Классификация по характеру функциональных групп. - определение понятия «функциональная группа»; - функциональные группы важнейших классов органических соединений. 2. Структурная изомерия органических соединений. 2.1. Определение понятий «изомерия», «изомеры». 2.2. Виды структурной изомерии: - изомерия углеродного скелета; - изомерия положения заместителя (кратной связи); - изомерия функциональных групп (межклассовая изомерия). 3. Основные термины номенклатуры IUPAC. 3.1. Органический радикал (определение). Строение следующих углеводородных радикалов: метил, этил, пропил, изопропил, фенил. 3.2. Родоначальная структура (определение). 3.3. Характеристические группы (по их старшинству). 3.4. Заместители: углеводородные радикалы; не старшие характеристические группы; группы, не имеющие старшинства. 4. Формирование названия по заместительной номенклатуре 4.1. Составные части названия: префиксы, корень, суффиксы. 4.2. Последовательность составления названия. 5. Электронное строение атомов углерода, азота, кислорода. 5.1. Типы гибридизации атомных орбиталей, пространственная направленность гибридных орбиталей. 5.2. Типы электронной конфигурации sp2-гибридных атомов азота и кислорода. Рекомендуемая литература А – с. 11-28. А* - с. 16-33, 48. А** - с. 11-28, 40-41. Б – тема 1.1 – обучающая задача 1 (с. 24-25). Вопросы для самоконтроля (задания, обозначенные*, обязательны для выполнения в письменном виде) 1*. Назовите по заместительной номенклатуре IUPAC следующие соединения:
К каким классам органических соединений они относятся? 2. Напишите структурные формулы следующих соединений: - пропанон-2 - пропандиол-1, 2 - бутендионовая кислота - 2-метилпропанол-2 - 2-оксопентановая кислота - 2, 6-диаминогексановая кислота - 2-амино-3-меркапто-3-метилбутановая кислота 3. Приведите структурные формулы изомеров состава C4H10O, назовите их по заместительной номенклатуре IUPAC.
Укажите валентный угол. Опишите электронную конфигурацию (распределение электронов по орбиталям) для подчёркнутых атомов.
|

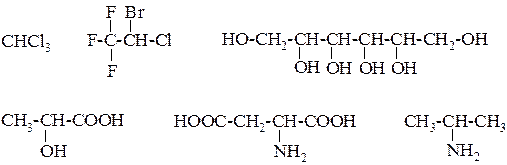

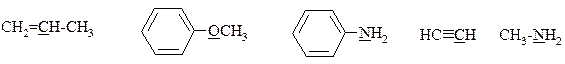 4*. Определите тип гибридизации каждого атома в следующих соединениях:
4*. Определите тип гибридизации каждого атома в следующих соединениях:


