Метод теоретических тарелок.Метод теоретических тарелок получил наибольшее применение для расчета процесса разделения как бинарных, так и многокомпонентных смесей. Расчет ведут по массам вещества, отнесенным к 1кг или 1кг-молю готового продукта - дистиллята (ректификата). В дальнейшем будем обозначать: F= Gf/Gd – количество кг-молей поступающей на ректификацию смеси, отнесенное к 1 кг-молю готового продукта; W= GW/Gd – количество кг-молей кубовой жидкости, отнесенное к 1 кг-молю готового продукта; R= GR/Gd – флегмовое число или количество кг-молей возвращающегося в колонну дистиллята (флегмы), отнесенное к 1 кг-молю готового продукта; п=РА/РВ – относительная летучесть компонентов, равная отношению давления пара чистого низкокипящего компонента (РА) к давлению пара чистого высококипящего компонента (РВ) при той же температуре; V=(R+1) – количество кг-молей паров, выходящих из колонны в дефлегматор для конденсации; yf, yd, yw – молярное содержание низкокипящего компонента в парах, равновесное жидкости исходной смеси, дистиллята и кубового остатка; хf, хd, хw - молярное содержание низкокипящего компонента в жидкой фазе: соответственно в исходной смеси, в дистилляте и кубовом остатке.
Материальный баланс ректификационной колонны для всей смеси Gf = Gd + Gw (1) или F=1 + W; (2) для низкокипящего компонента в смеси Gf*xf = Gd*xd + Gw*xw (3)
или F*xf = xd + W*xw = xd + (F-1)*xw. (4)
В основу расчета процессов разделения взаиморастворимых смесей положен закон Рауля: парциальное давление одного из компонентов в паровой фазе, находящейся в равновесии с кипящей жидкостью при некоторой температуре, равно мольной доле этого компонента в жидкости, умноженной на давление насыщенных паров этого же компонента, кипящего в чистом виде при температуре смеси.
рА = РА*хА. (5) где рА - парциальное давление пара низкокипящего компонента А над кипящей смесью; РА – давление насыщенных паров чистого низкокипящего компонента А при температуре кипения смеси.
Уравнение для высококипящего компонента В будет иметь вид: pВ=РВ*(1 - хА). (6)
Суммарное давление паров в смеси: P=pA+pB=PA*xA+PB*(1-xA). (7)
Из уравенения 7 следует, что
(8)
Если учесть, что между парциальным давлением любого компонента и его мольной концентрацией в паровой фазе существует связь в форме закона Дальтона
уA=pA/P; yB=pB/P,
где Р – общее давление над смесью, то нетрудно, подставив выражение (5), получить соотношение, устанавливающее зависимость между содержанием легколетучего компонента в равновесных парах и его концентрацией в жидкой смеси:
(9) .
Соотношение (9) можно записать в виде:
Для второго (высококипящего) компонента: pB=yB*P (по закону Дальтона); pB=хB*P (по закону Рауля) или
(11)
Выражение (11) можно переписать в более удобной форме, подставив его в (9):
(12)
Введем в выражение (12) относительную летучесть aп=РА/РВ,получим:, т.е. относительное содержание легколетучего компонента в паровой фазе в aп раз больше, чем в жидкой смеси. Этот факт известен под названием закона Коновалова: пар относительно жидкости обогащен тем компонентом, прибавление которого к смеси повышает общее давление пара. Таким образом, чем больше относительная летучесть aп, тем значительнее различие концентраций паровой и жидкой фаз, и тем легче осуществить разделение смеси на составляющие её компоненты. Выбрав несколько значений температуры кипения смеси, лежащих между температурами кипения чистых компонентов А и В, можно построить фазовую t – x,y диаграмму (рис. 2). На этой диаграмме: по оси абсцисс – концентрация низкокипящего компонента в жидкости «х» и в парах «у»; по оси ординат – температура Т; T=f(x) – линия кипения смеси; T=f(y) – линия конденсации смеси.
Для расчета числа тарелок ректификационной колонны пользуются диаграммой равновесия, в которой на оси абсцисс откладывают концентрацию низкокипящего компонента в жидкости х, а по оси ординат – концентрацию низкокипящего компонента в парах у (рис. 3). Процесс ректификации можно представить как разделение исходной жидкой смеси на дистиллят и остаток в результате процесса взаимодействия жидкости с парами в двух частях колонны: верхней – укрепляющей, и нижней - исчерпывающей. В нижней части колонны жидкая смесь F, поступающая на ректификацию с концентрацией низкокипящего компонента xf, взаимодействует в противотоке с парами, первоначальная концентраций которых равна концентрации паров кубового остатка уw. В результате тепло- и массообмена стекающая жидкая смесь обедняется низкокипящим компонентом, а поднимающиеся из куба пары обогащаются низкокипящим компонентом. В верхней части колонны пар с начальной концентрацией уf, соответствующей концентрации исходной жидкой смеси F, взаимодействует в противотоке с флегмой R, начальная концентрация которой равна концентрации дистиллята хd. При этом он обогащается низкокипящим компонентом до заданной конечной концентрации уd. а высококипящий компонент извлекается из паровой фазы и смешивается со стекающей жидкостью. Пар для тепломассообмена с жидкостью получается в ректификационной колонне в результате испарения жидкой смеси в нижней (кубовой) части аппарата, а также
путем многоступенчатого испарения стекающей жидкости при контакте с поднимающимися парами. В укрепляющую и исчерпывающую части колонны жидкость поступает в виде исходной смеси и части возвращаемого в колонну дистиллята – флегмы; кроме того, жидкость образуется в процессе конденсации движущегося в колонне пара. Приняв за основу равенство количеств конденсирующейся жидкости и образующихся паров, материальный баланс тарелки ректификационной колонны для низкокипящего компонента можно выразить равенствами: для верхней части колонны:
(R+1)*yd = R*(xd); (14)
для нижней части колонны:
(R+1)*yw = (R+F)*(xw); (15)
На участке верхней части колонны от произвольного сечения с концентрациями х в жидкости и у в паре до выходного сечения с концентрациями соответственно xd и yd изменение концентрации флегмы (xd - x) и концентрации паров (yd - y) выразится уравнением:
(R+1)*(yd – y)= R*(xd - x); (16)
Используя допущение (yd=xd), преобразуем уравнение (16):
где А и В – постоянные коэффициенты при выбранных или заданных R и xd.
На участке от произвольного сечения нижней части колонны с концентрациями х и у до ее нижнего сечения изменение концентрации выразится из уравнения (15):
(R+1)*(y - yw)= (R+F)*(x - xw). (18)
Используя допущение (yw=xw), преобразуем уравнение (18): где A’ и В’ – постоянные коэффициенты при выбранных для расчета значениях R, F и xw.
|



 (10)
(10)
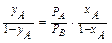
 (13)
(13)








