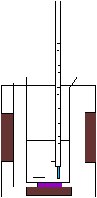
ЛАБОРАТОРНАЯ РАБОТАОпыт 1. Определение изменения энтальпии реакции нейтрализации Для проведения эксперимента необходимо взять (по указанию преподавателя) один из растворов сильной кислоты (HCl, H2SO4, HNO3) и один из растворов щелочи (NaOH, KOH) заданных концентраций и заданных объемов. Составьте уравнение реакции между указанными веществами в молекулярном и ионном виде. Опыт проводят в калориметрической установке, упрощенная схема которой показана на рисунке 1. Установка состоит из двух алюминиевых стаканов, вставленных один в другой и изолированных друг от друга корковыми или резиновыми прокладками для уменьшения потерь тепла. Во внутренний стакан калориметра помещается стеклянный химический стакан, в котором проводится опыт.
Взвесьте калориметрический стеклянный стакан. Измерьте его диаметр и высоту с точностью до 1 мм. При помощи мерных цилиндров точно отмерьте равные объемы (20‑30 мл, объем указывает преподаватель) растворов кислоты и щелочи равных концентраций; при этом необходимо пользоваться разными цилиндрами, маркированными соответственно буквами «К» и «Щ». В стеклянный стакан калориметра, предварительно вытащив его из калориметрической установки, аккуратно, без потерь, внесите отмеренный объем раствора щелочи. Стакан с раствором щелочи вновь поместите в калориметрическую установку. Измерьте температуру раствора щелочи, находящегося в стеклянном стакане калориметра при помощи ртутного термометра с точностью до 0,1оС. Не вынимая термометр из калориметрической установки, быстро и без потерь влейте весь раствор кислоты в стеклянный химический стакан. При помощи термометра аккуратно перемешайте раствор и отметьте максимальную температуру. После этого вытащите стеклянный стакан из калориметрической установки и измерьте высоту столба жидкости в нем. С помощью ареометра измерьте плотность полученного раствора.
Результаты опыта внесите в таблицу.
На основании полученных данных рассчитайте изменение энтальпии реакции нейтрализации. Пояснения к расчетам: 1. Вычисление теплоты, выделившейся в ходе опыта, проводится по формуле: Q = (mр‑раСр‑ра + mстеклаСстекла)Dt (Дж), где Dt = tмакс. – tнач; Ср‑ра – удельная теплоемкость раствора (примерно равна теплоемкости воды 4,184 Дж/г ·К); Сстекла – удельная теплоемкость стекла (Сстекла = 0,753 Дж/г ·К); mр‑ра – масса раствора после проведения реакции; mстекла – масса стакана, контактирующая с раствором. Массу раствора можно определить, суммируя массы растворов кислоты и щелочи. Массу раствора кислоты (или щелочи) определим через его плотность и объем. Массу стакана, занятого раствором, можно оценить по пропорции, предварительно вычислив его общую площадь и площадь, занятую раствором. 2. Зная концентрации и объемы исходных растворов, вычислить количества n кислоты и щелочи, взятые для проведения реакции. По найденной величине сделать пересчет выделившегося количества тепла на 1 моль Н+ (ОН–). 3. Рассчитать теоретическое значение изменения энтальпии реакции нейтрализации по табличным данным: DНобр.о(Н+) = 0, DНобр.о(ОН–) = –230,19, DНобр.о(Н2О(ж)) = –285,83 кДж/моль). 4. Определить (в %) абсолютную ошибку опыта.
• Почему реакция нейтрализации сопровождается выделением тепла? Почему тепловой эффект реакции нейтрализации сильного основания сильной кислотой не зависит от природы кислоты и основания? Относится ли то же самое к слабым кислотам и основаниям и почему?
|