Классификация кислот
Тема: Основные классы неорганических соединений. Урок: Кислоты 1. Классификация кислот Кислоты – это вещества молекулярного строения. Атомы в молекулах кислот связаны ковалентными полярными связями. Чем больше поляризована связь между атомом водорода, способным отщепляться, и электроотрицательным атомом (кислорода, серы или атомом галогена), то тем более эта связь склонна диссоциировать по гетеролитическому пути. А значит, тем больше в растворе будет катионов водорода и тем кислее будет среда. Большое значение имеет не только полярность, но и поляризуемость связи. Поляризуемость – это способность связи поляризоваться под действием определенных реагентов. Например, молекул воды. Классификация кислот Классификация кислот по содержанию атомов кислорода, по количеству атомов водорода, по растворимости и другим признакам. См. Табл. 1.
Табл. 1. 2. Химические свойства кислот 1. Реакция с металлами. Металлы, расположенные в ряду напряжений металлов (Рис. 1.) до водорода, вытесняют водород из кислот. Mg + 2HCl = MgCl2 + H2↑
Рис. 1. С концентрированной азотной и серной кислотой реакции идут за счет анионного остатка. Водород не выделяется. Рис. 2. Cu + 4HNO3(конц) = Cu (NO3)2 + 2NO2↑ + H2O Cu + 2H2SO4(конц) = Cu SO4 + SO2↑ + H2O
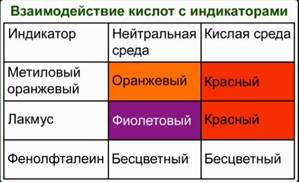
Рис. 2 2. Реакция с основными и амфотерными оксидами с образованием соли и воды. K2O+ HNO3 = KNO3 + H2O Al2O3 + 6HCl = 2AlCl3 + 3H2O 3. Реакция с солями. Кислоты реагируют с растворами солей, если в результате реакции один из продуктов выпадает в осадок, поскольку образование нерастворимых соединений смещает равновесие вправо и делает её практически необратимой. Н2SO4 + BaCl2 = BaSO4↓ +2 HCl H2CO3 + BaCl2 = BaCO3↓ +2 HCl 4. Реагируют с основаниями и амфотерными гидроксидами. KOН+ HNO3 = KNO3 + H2O Al(OН)3 + 3HCl = AlCl3 + 3H2O NaOH + HNO3 = NaNO3 + H2O 5. Обнаружение кислот при помощи кислотно-основных индикаторов. В кислой среде лакмус приобретает красную окраску. Метиловый оранжевый – красную, а фенолфталеиновый – бесцветный. Рис. 3 3. Получение кислот
|