Тиск газу
План Ідеальний газ Тиск газу 3. Основне рівняння МКТ Приклади задач Питання контролю Всі тіла складаються з молекул, які хаотично рухаються і взаємодіють між: собою. У газах сипи взаємодії такі малі, що ними можна знехтувати. Тому для пояснення властивостей речовин у газоподібному стані використовують модель ідеального газу. Ідеальний газ. Ідеальний газ це газ взаємодією молекул в якому можна знехтувати, а молекули розглядати як матеріальні точки. Природні гази при не дуже низьких температурах і досить малих тисках - розряджені гази - за своїми властивостями близькі до ідеального газу. Тиск газу Молекули газу перебувають в безперервному хаотичному русі. Рухаючись в деякій посудині вони зіштовхуються як між собою так і з стінками посудини. Середня сила
Одиниці вимірювання тиску в СІ:
Крім того є і інші одиниці вимірювання тиску. Бар: Технічна атмосфера: Міліметри ртутного стовпчика: Фізична атмосфера: Тиск можна виміряти за допомогою барометра та манометра. Барометром визначають атмосферний тиск, манометром – тиск в резервуарах, шинах, і т.п. Нормальний атмосферний тиск: Принцип дії манометра, барометра см § 3.8 стор 37 Для визначення повного тиску за допомогою манометра до значення яке показує стрілка манометра додають атмосферний тиск. Вакуумце середовище в якому тиск менше атмосферного. Чим нижче тиск тим глибше вакуум. Глибокий вакуум необхідний для нормальної роботи багатьох пристроїв та установок, наприклад телевізійних трубок, рентгенівських установок, радіоламп і т.п. 3. Основне рівняння м.к.т. газу. Вияснимо, від чого залежить тиск газу? По-перше, він залежить від маси молекули газу. Чим більше маса молекул, тим більше тиск:
По-друге, тиск газу залежить від кількості молекул в одиниці об’єму, отже концентрації. Концентрація
Одиниці вимірювання концентрації в СІ:
По-третє, тиск газу залежить від середньої швидкості руху молекул.
Таким чином, користуючись законами збереження (стор 40), можна вивести рівняння яке об’єднує ці три параметра з тиском. Таке рівняння називається основним рівнянням м.к.т. газу, і має вигляд:
Кінетична енергія:
Тоді тиск можна визначити за формулою:
Якщо виразити швидкість з рівняння (2), то дістанемо
Зв’яжемо тиск газу та густину:
Приклади розв’язування задач 1. Знайти середню квадратичну швидкість молекули газу, що має густину
2. Визначити концентрацію молекул повітря в аудиторії при нормальних умовах, якщо густина повітря
Контрольні питання. 1. Як пояснити тиск газу с точки зору молекулярно-кінетичної теорії? 2. Якими приладами визначається тиск? 3. В яких одиницях вимірюється тиск? 4. Що таке вакуум? 5. Де зустрічається глибокий вакуум? 6. Чому дорівнює нормальний атмосферний тиск? 7. Від яких параметрів залежить тиск? 8. Що таке концентрація і в яких одиницях вимірюється в системі СІ? 9. Який вигляд має основне рівняння МКТ (3 формули)? Домашнє завдання: 2.37 Знайти середню квадратичну швидкість молекул газу, якщо його густина
|

 яка діє з боку молекул газу на одиницю площини
яка діє з боку молекул газу на одиницю площини  перпендикулярної поверхні і характеризує тиск газу.
перпендикулярної поверхні і характеризує тиск газу.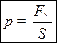
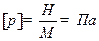

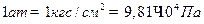
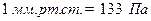

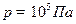
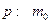
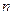 це кількість молекул в одиниці об’єму.
це кількість молекул в одиниці об’єму.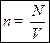 ;
;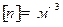
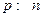

 основне рівняння м.к.т. газу. (1)
основне рівняння м.к.т. газу. (1) середня кінетична енергія руху молекули. (2)
середня кінетична енергія руху молекули. (2)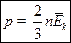 основне рівняння м.к.т. газу. (3)
основне рівняння м.к.т. газу. (3) 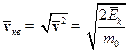 - середня квадратична швидкість молекул.
- середня квадратична швидкість молекул.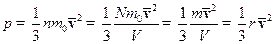
 основне рівняння м.к.т. газу.(4)
основне рівняння м.к.т. газу.(4) 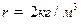 і знаходиться під тиском
і знаходиться під тиском  .
. ; звідки
; звідки  тоді
тоді 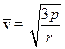
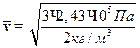 =
=

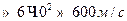
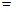 Відповідь:
Відповідь: 


 , а маса однієї молекули
, а маса однієї молекули  .
.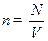 (1);
(1);  (2)
Підставимо в (2) в (1):
(2)
Підставимо в (2) в (1):
 (3); Враховуючи що
(3); Враховуючи що 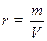 , рівняння (3) буде мати вигляд:
, рівняння (3) буде мати вигляд: 
 =
= 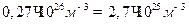 Відповідь:
Відповідь: 


 а тиск дорівнює
а тиск дорівнює 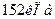 . (Відповідь: 500 м/с)
. (Відповідь: 500 м/с)


