Измерения
5.4.1 Установите начальное значение объема Vнач = 40 дм3 и начальную температуру Т1 газа, близкую к числам из таблицы 1. Для этого нажмите кнопку «ВЫБОР», и переместите маркер мыши так, чтобы его острие находилось в указанной точке вблизи границы столбика на градуснике, и коротко нажмите и удерживая левую кнопку мыши двигайте столбик, или с помощью нажатия левой клавиши мыши установите необходимую температуру. 5.4.2 Нажмите мышью кнопку «Старт» на экране и наблюдайте перемещение поршня на левой картинке модели и перемещение точки по красной кривой теоретической адиабаты. Попробуйте останавливать процесс нажатием кнопки «СТОП». Последующий запуск процесса осуществляется нажатием кнопки «Старт». 5.4.3 После автоматической остановки процесса запустите его снова, нажав кнопку «Старт», и останавливайте, нажимая кнопку «Стоп», когда крестик на теоретической адиабате (красная кривая) будет находиться вблизи следующих значений объема: 15, 20, 25, 30, 35 и 40 дм3 (6 значений), записывая при остановке значения объема, температуры и давления в таблицу 2, аналогичную в методических указаниях. 5.4.4. Установите новое значение температуры Т2, взяв его из таблицы 1, задавая Vнач = 40 дм3 и повторите измерения, записывая результаты в таблицу 3, аналогичную в методических указаниях..
ТАБЛИЦА 1. Начальные значения температуры (не перерисовывать)
Таблицы 2,3 Результаты измерений при Tн = ____ K
5.5 Обработка результатов и оформление отчета: 1 Постройте на одном рисунке графики экспериментальных зависимостей логарифма давления от логарифма объема для обеих адиабат (указав на них начальные температуры). 2 Для каждой адиабаты определите по графику экспериментальное значение показателя, используя формулу 3 Определите число степеней свободы молекулы газа, исследуемого в данной компьютерной модели, используя формулу (9). 4 Подберите распространенный газ, структура молекулы которого близко к наблюдаемой. 5 Запишите ответы и проанализируйте ответы и графики. Контрольные вопросы
1. Что такое параметры состояния системы? 2. Дайте определение равновесного состояния системы. 3. Какой процесс называется обратимым? 4. Что такое цикл? 5. Что такое уравнение состояния? 6. Для какого физического газа можно применить модель «идеальный газ»? 7. Какому уравнению подчиняется состояние идеального газа? Напишите его. 8. Дайте определение теплоемкости тела. 9. Дайте определение удельной теплоемкости. 10. Напишите формулу для теплоемкости при постоянном объеме. 11. Напишите формулу для теплоемкости идеального газа при постоянном давлении. 12. Что такое число степеней свободы? Чему оно равно для одноатомной молекулы? 13. Что такое показатель адиабаты? 14. Напишите формулу связи показателя адиабаты с числом степеней свободы молекулы идеального газа. 15. Дайте определение адиабатического процесса. 16. Напишите уравнение адиабатического процесса. 17. Дайте определение изопроцесса. Перечислите известные изопроцессы. 18. Напишите уравнение и нарисуйте PV-диаграмму изотермического процесса. 19. Напишите уравнение и нарисуйте PV-диаграмму изобарического процесса. 20. Напишите уравнение и нарисуйте PV-диаграмму изохорического процесса. 7 Содержание отчёта 7.1 Наименование работы. 7.2 Цель работы. 7.3 Описание используемого оборудования. 7.4 Краткое описание хода работы. Уравнение адиабаты с необходимыми пояснениями. 7.5 Таблицы полученных данных. 7.6 Графики экспериментальных зависимостей логарифма давления от логарифма объема для обеих адиабат (указав на них начальные температуры). 7.8 Выводы. Список использованной литературы
1. Трофимова Т.И. Курс физики. М.: Высшая школа, 2001. Гл.9, § 55. 2. Детлаф А.А., Яворский Б.М. Курс физики. М.: Высшая школа, 2000. Гл. 9, § 9.6. 3. Лукьянов А.Б. Физическая и коллоидная химия: Учебник для техникумов. – 2-е изд., перераб. И доп. – М.: Химия, 1988. – 288 с.: ил.
|

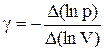 .
.


