И ОСНОВНЫЕ КОНСТАНТЫ
Единицы длины – [м, см, нм, Å ] 1м=102см =109нм=1010Å. Единицы энергии – [Дж, кДж, эВ] 1Дж= 10-3кДж; 1 эВ = 1, 6× 10-19 Дж. Единицы массы – [кг, г] 1кг = 103 г. Относительная атомная масса (А) и относительная молекулярная масса (М) – средняя масса атома или молекулы отнесенная к 1/12 массе атома углерода 12С (1 атомная единица массы). 1а.е.м. = 1, 6605× 10-27 кг. Количество вещества – моль – количество вещества, содержащее 6, 02× 1023 структурных единиц (атомов, молекул, ионов). N А=6, 02× 1023 [1/моль] – число Авогадро. Молярная масса (m n) – масса одного моля вещества, выраженная в граммах, численно равна молекулярной массе (m n = М г). Молярный объем – объем одного моля вещества. Для любого вещества в газообразном состоянии при нормальных условиях (Р = 1, 013× 105 Па (Н/м2); Т = 273, 15 К) молярный объем равен 22, 4 л. Абсолютная термодинамическая шкала температур (Кельвина) T K = t oC + 273, 15. Стандартные термодинамические условия: Р 0 = 1, 013× 105 Па (Н/м2); Т 0 = 298, 15 К. Элементарный электрический заряд е = 1, 602× 10-19 Кл. Электрон: масса m = 9, 11× 10-31 кг, заряд е = 1, 60× 10-19 Кл. Скорость света в вакууме c = 2, 9979× 108 м/с. Постоянная Планка h = 6, 6262× 10-34 Дж× с, Константа в законе Кулона Радиус первой боровской орбиты атома водорода r 1 = 0, 53Å. Энергия электрона атома водорода в основном состоянии Е 1= –13, 6 эВ. Постоянная Больцмана k = 1, 381× 10-23 Дж/К. Универсальная газовая постоянная R = 8, 314 Дж/моль× К.
|

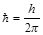 =1, 0546× 10-34 Дж× с.
=1, 0546× 10-34 Дж× с. (Н× м/Кл).
(Н× м/Кл).


