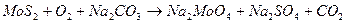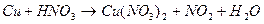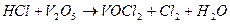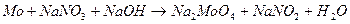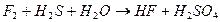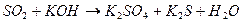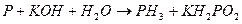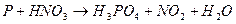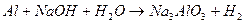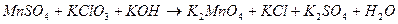Модуль II. 81.Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) Na2CO3 и H2SO4; б) K2SiO3 и HCl; в)BaCl2 и Na2SO4
81. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) Na2CO3 и H2SO4; б) K2SiO3 и HCl; в)BaCl2 и Na2SO4. 82. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) K2S и HCl; б) FeSO4 и (NH4)2S; в) Cr(OH)3 и KOH. 83. Составьте по три молекулярных уравнения реакций, которые выражаются ионно-молекулярными уравнениями: а) Mg2++CO32− = MgCO3 б) H++OH − = H2O 84. Какое из веществ: Al(OH)3; H2SO4; Ba(OH)2 – будет взаимодействовать с гидроксидом калия? Выразите эти реакции молекулярными и ионно-молекулярными уравнениями. 85. Составьте молекулярные и ионно-молекулярные уравнения реакции взаимодействия в растворах между: а) K2CO3 и HCl; б) Zn(OH)2 и NaOH; в) CaCl2 и AgNO3. 86. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) CuSO4 и H2S; б) BaCO3 и HNO3; в) FeCl3 и KOH. 87. Составьте по три молекулярных уравнения реакций, которые выражаются ионно-молекулярными уравнениями: а) Cu2++S2− = CuS б) SiO32− +2H+ = H2SiO3 88. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) Sn(OH)2 и HCl; б) BeSO4 и KOH; в) NH4Cl и Ba(OH)2. 89. Какое из веществ: K2CO3, CH3COOH, NiSO4, Na2S – взаимодействует с раствором серной кислоты? Запишите молекулярные и ионно-молекулярные уравнения этих реакций. 90. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) AgNO3 и K2CrO4; б) Pb(NO3)2 и KI; в) CdSO4 и Na2S. 91. Составьте молекулярные уравнения реакций, которые выражаются ионно-молекулярными уравнениями: а) CaCO3 + 2H+ = Ca2+ + H2O + CO2 б) Al(OH)3 + OH ‾ = AlO2‾ + 2 H2O в) Pb2+ + 2I ‾ = PbI2 92. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) Be(OH)2 и NaOH; б)Cu(OH)2 и HNO3; в)ZnCO3 и HCl 93. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а)Na3PO4 и CaCl2; б) K2CO3 и BaCl2; в) Zn(OH)2 и KOH. 94. Составьте молекулярные уравнения реакций, которые выражаются ионно-молекулярными уравнениями: Fe(OH)3 + 3H+ = Fe3+ + 3H2O Cd2+ + 2OH ‾ = Cd(OH)2 H+ + NO2‾ = HNO2 95. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) CdS и HCl; б) Cr(OH)3 и NaOH; в) Ba(OH)2 и CoCl2. 96. Составьте молекулярные уравнения реакций, которые выражаются ионно-молекулярными уравнениями: а) Zn2+ + H2S = ZnS + 2H+ б) HCO3‾ + H+ = H2O + CO2 в) Ag+ + Cl ‾ = AgCl 97. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) H2SO4 и Ba(OH)2; б) FeCl3 и NH4OH; в) CH3COONa и HCl. 98. Составьте молекулярные и ионно-молекулярные уравнения реакций взаимодействия в растворах между: а) FeCl3 и KOH; б) NiSO4 и (NH4)2S; в) MgCO3 и HNO3. 99. Составьте молекулярные уравнения реакций, которые выражаются ионно-молекулярными уравнениями: а) Ве(OH)2 + 2OH ‾ = BeO22‾ + 2H2O б) CH3COO‾ + H+ = CH3COOH в) Ba2+ + SO42‾ = BaSO4 100. Какое из веществ: NaCl, NiSO4, Be(OH)2, KHCO3 - взаимодействует с раствором гидроксида натрия. Запишите молекулярные и ионно-молекулярные уравнения этих реакций.
101. Методом электронного баланса рассчитайте стехиометрические коэффициенты в уравнении реакции:
102. Методом электронного баланса рассчитайте стехиометрические коэффициенты в уравнении реакции:
103. Методом электронного баланса рассчитайте стехиометрические коэффициенты в уравнении реакции:
104. Методом электронного баланса рассчитайте стехиометрические коэффициенты в уравнении реакции:
105. Методом электронного баланса рассчитайте стехиометрические коэффициенты в уравнении реакции:
106. Методом электронного баланса рассчитайте стехиометрические коэффициенты в уравнении реакции:
107. Методом электронного баланса рассчитайте стехиометрические коэффициенты в уравнении реакции:
108. Методом электронного баланса рассчитайте стехиометрические коэффициенты в уравнении реакции:
109. Методом электронного баланса рассчитайте стехиометрические коэффициенты в уравнении реакции:
110. Методом электронного баланса рассчитайте стехиометрические коэффициенты в уравнении реакции:
111. Методом электронного баланса рассчитайте стехиометрические коэффициенты в уравнении реакции:
112. Методом электронного баланса рассчитайте стехиометрические коэффициенты в уравнении реакции:
113. Методом электронного баланса рассчитайте стехиометрические коэффициенты в уравнении реакции:
114. Методом электронного баланса рассчитайте стехиометрические коэффициенты в уравнении реакции:
115. Методом электронного баланса рассчитайте стехиометрические коэффициенты в уравнении реакции:
116. Методом электронного баланса рассчитайте стехиометрические коэффициенты в уравнении реакции:
117. Методом электронного баланса рассчитайте стехиометрические коэффициенты в уравнении реакции:
118. Методом электронного баланса рассчитайте стехиометрические коэффициенты в уравнении реакции:
119. Методом электронного баланса рассчитайте стехиометрические коэффициенты в уравнении реакции:
120. Методом электронного баланса рассчитайте стехиометрические коэффициенты в уравнении реакции:
121. В два сосуда с голубым раствором медного купороса поместили в первый цинковую пластинку, а во второй серебряную. В каком сосуде цвет раствора постепенно пропадает? Почему? Составьте электронные и молекулярное уравнения соответствующей реакции. 122. Увеличится, уменьшится или останется неизменной масса цинковой пластинки при взаимодействии ее с растворами: а) CuSO4; б) MgSO4; в) Pb(NO3)2? Почему? Составьте электронные и молекулярные уравнения соответствующих реакций. 123. При какой концентрации ионов Zn2+ (в моль/дм3) потенциал цинкового электрода будет на 0, 015 В меньше его стандартного электродного потенциала? 124. Увеличится, уменьшится или останется неизменной масса кадмиевой пластинки при взаимодействии ее с растворами: а) AgNO3; б) ZnSO4; в) NiSO4? Почему? Составьте электронные и молекулярные уравнения соответствующих реакций. 125. Марганцевый электрод в растворе его соли имеет потенциал –1, 23 В. Вычислите концентрацию ионов Mn2+(в моль/дм3). Ответ: 2 × 10-2 моль/ дм3. 126. Потенциал серебряного электрода в растворе AgNO3 составил 95% от значения его стандартного электродного потенциала. Чему равна концентрация ионов Ag+ (в моль/л)? 127. Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС медно-кадмиевого гальванического элемента, в котором [Cd2+]=0, 8 моль/ дм3, а [Cu2+]=0, 01 моль/ дм3. 128. Составьте схемы двух гальванических элементов, в одном из которых медь была бы катодом, а в другом – анодом. Напишите для каждого из этих элементов электронные уравнения реакций, протекающих на катоде и аноде. 129. При какой концентрации ионов Cu2+(в моль/ дм3) значение потенциала медного электрода становится равным стандартному потенциалу водородного электрода? 130. Какой гальванический элемент называется концентрационным? Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС гальванического элемента, состоящего из серебряных электродов, опущенных: первый в раствор AgNO3 с концентрацией 0, 01моль/ дм3, а второй в раствор AgNO3 с концентрацией 0, 1 моль/ дм3. 131. При каком условии будет работать гальванический элемент, электроды которого сделаны из одного и того же металла? Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС гальванического элемента, в котором один никелевый электрод находится в растворе с концентрацией 0, 001 моль/дм3, а другой такой же электрод – в растворе сульфата никеля с концентрацией 0, 01 моль/ дм3. 132. Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС гальванического элемента, состоящего из свинцовой и магниевой пластин, опущенных в растворы своих солей с концентрацией [Pb2+] = [Mg2+] = 0, 01 моль/дм3. Изменится ли ЭДС этого элемента, если концентрацию каждого из ионов увеличить в одинаковое число раз? 133. Составьте схемы двух гальванических элементов, в одном из которых никель является катодом, а в другом – анодом. Напишите для каждого из этих элементов электронные уравнения реакций, протекающих на катоде и аноде. 134. Железная и серебряная пластины соединены внешним проводником и погружены в раствор серной кислоты. Составьте схему данного гальванического элемента и напишите электронные уравнения процессов, происходящих на аноде и катоде. 135. Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС гальванического элемента, состоящего из пластин кадмия и магния, опущенных в растворы своих солей с концентрацией [Mg2+] = [Cd2+] = 1 моль/ дм3. Изменится ли значение ЭДС, если концентрацию каждого из ионов понизить до 0, 01 моль/ дм3? 136. Составьте схему гальванического элемента, состоящего из пластин цинка и железа, погруженных в растворы их солей. Напишите электронные уравнения реакций, протекающих на катоде и аноде. Какой концентрации надо было бы взять ионы железа (моль/ дм3), чтобы ЭДС элемента стала равной нулю, если [Zn2+] = 0, 001 моль/ дм3? 137. Составьте схему гальванического элемента, в основе которого лежит реакция, протекающая по уравнению Ni + Pb(NO3)2 = Ni(NO3)2 + Pb Напишите электронные уравнения анодного и катодного процессов. Вычислите ЭДС этого элемента, если [Ni2+] = 0, 01 моль/ дм3, [Pb2+] = 0, 0001 моль/ дм3. 138. Какие химические процессы протекают на электродах при зарядке и разрядке свинцового аккумулятора? 139. Какие химические процессы протекают на электродах при зарядке и разрядке никель-кадмиевого аккумулятора? 140. Какие химические процессы протекают на электродах при зарядке и разрядке железо-никелевого аккумулятора?
141. Как происходит атмосферная коррозия луженого и оцинкованного железа при нарушении покрытия? Составьте электронные уравнения анодного и катодного процессов. 142. Медь не вытесняет водород из разбавленных кислот. Почему? Однако если к медной пластинке, опущенной в кислоту, прикоснуться цинковой, то на меди начинается бурное выделение водорода. Дайте этому объяснение, составив электронные уравнения анодного и катодного процессов. Напишите уравнение протекающей химической реакции. 143. Как происходит атмосферная коррозия луженого железа и луженой меди при нарушении покрытия? Составьте электронные уравнения анодного и катодного процессов. 144. Если пластинку из чистого цинка опустить в разбавленную кислоту, то начинающееся выделение водорода вскоре почти прекращается. Однако при прикосновении к цинку медной палочкой на последней начинается бурное выделение водорода. Дайте этому объяснение, составив электронные уравнения анодного и катодного процессов. Напишите уравнение протекающей химической реакции. 145. В чем сущность протекторной защиты металлов от коррозии? Приведите пример протекторной защиты железа в электролите, содержащем растворенный кислород. Составьте электронные уравнения анодного и катодного процессов. 146. Железное изделие покрыли никелем. Какое это покрытие - анодное или катодное? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этого изделия при нарушении покрытия во влажном воздухе и в хлороводородной (соляной) кислоте. Какие продукты коррозии образуются в первом и во втором случаях? 147. Составьте электронные уравнения анодного и катодного процессов с кислородной и водородной деполяризацией при коррозии пары магний - никель. Какие продукты коррозии образуются в первом и во втором случаях? 148. В раствор хлороводородной (соляной) кислоты поместили цинковую пластинку и цинковую пластинку, частично покрытую медью. В каком случае процесс коррозии цинка происходит интенсивнее? Ответ мотивируйте, составив электронные уравнения соответствующих процессов. 149. Почему химически чистое железо более стойко против коррозии, чем техническое железо? Составьте электронные уравнения анодного и катодного процессов, происходящих при коррозии технического железа во влажном воздухе и в кислой среде. 150. Какое покрытие металла называется анодным и какое - катодным? Назовите несколько металлов, которые могут служить для анодного и катодного покрытия железа. Составьте электронные уравнения анодного и катодного процессов, происходящих при коррозии железа, покрытого медью, во влажном воздухе и в кислой среде. 151. Железное изделие покрыли кадмием. Какое это покрытие — анодное или катодное. Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этого изделия при нарушении покрытия во влажном воздухе и в хлороводородной (соляной) кислоте. Какие продукты коррозии образуются в первом и во втором случаях? 152. Железное изделие покрыли свинцом. Какое это покрытие — анодное или катодное? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этого изделия при нарушении покрытия во влажном воздухе и в хлороводородной (соляной) кислоте. Какие продукты коррозии образуются в первом и в втором случаях? 153. Две железные пластинки, частично покрытые одна оловом, другая медью, находятся во влажном воздухе. На какой из этих пластинок быстрее образуется ржавчина? Почему? Составьте электронные уравнения анодного и катодного процессов коррозии этих пластинок. Каков состав продуктов коррозии железа? 154. Какой металл целесообразней выбрать для протекторной защиты от коррозии свинцовой оболочки кабеля: цинк, магний или хром? Почему? Составьте электронные уравнения анодного и катодного процессов атмосферной коррозии. Какой состав продуктов коррозии? 155. Если опустить в разбавленную серную кислоту пластинку из чистого железа, то выделение на ней водорода идет медленно и со временем почти прекращается. Однако, если цинковой палочкой прикоснуться к железной пластинке, то на последней начинается бурное выделение водорода. Почему? Какой металл при этом растворяется? Составьте электронные уравнения анодного и катодного процессов. 156. Цинковую и железную пластинки опустили в раствор сульфата меди. Составьте электронные и ионно-молекулярные уравнения реакций, происходящих на каждой из этих пластинок. Какие процессы будут проходить на пластинках, если наружные концы их соединить проводником? 157. Как влияет рН среды на скорость коррозии железа и цинка? Почему? Составьте электронные уравнения анодного и катодного процессов атмосферной коррозии этих металлов. 158. В раствор электролита, содержащего растворенный кислород, опустили цинковую пластинку и цинковую пластинку, частично покрытую медью. В каком случае процесс коррозии цинка проходит интенсивнее? Составьте электронные уравнения анодного и катодного процессов. 159. Составьте электронные уравнения анодного и катодного процессов с кислородной и водородной деполяризацией при коррозии пары алюминий - железо. Какие продукты коррозии образуются в первом и во втором случаях? 160. Как протекает атмосферная коррозия железа, покрытого слоем никеля, если покрытие нарушено? Составьте электронные уравнения анодного и катодного процессов. Каков состав продуктов коррозии? Таблица вариантов контрольных заданий (номер варианта определяется по двум последним цифрам номера студенческого билета)
|