Примеры. Пример 1. Какое количество продуктов горения выделится при сгорании 1м3 ацетилена в воздухе, если температура горения составила 1450 К
Пример 1. Какое количество продуктов горения выделится при сгорании 1м3 ацетилена в воздухе, если температура горения составила 1450 К. Решение. Горючее-индивидуальное химическое соединение (формула 1.2.1). Запишем уравнение химической реакции горения C2H2+ Объём продуктов горения при нормальных условиях
Объём продуктов горения при 1450 К
Пример 2. Определить объём продуктов горения при сгорании 1 кг фенола, если температура горения 1200 К, давление 95000 Па, коэффициент избытка воздуха 1, 5. Решение. Горючее-индивидуальное химическое соединение(формула 1.2.2). Запишем уравнение химической реакции горения C6H5OH+ Молекулярная масса горючего 98. Теоретический объём продуктов горения при нормальных условиях
Практический объём воздуха при нормальных условиях
Объём продуктов горения при заданных условиях
Пример 3. Определить объём продуктов горения при сгорании 1 кг органической массы состава: С-55%, О-13%, Н-5%, S-7%, N-3%, W 17%, если температура горения 1170 К, коэффициент избытка воздуха – 1.3. Решение. Горючее вещество сложного состава (формулы 1.2.3 - 1.2.6). Теоретический состав продуктов горения при нормальных условиях
Полный теоретический объём продуктов горения при нормальных условиях
Практический объём продуктов горения при нормальных условиях
Практический объём продуктов горения при температуре горения
Пример 4. Рассчитать объём продуктов горения при сгорании 1м3 газовой смеси, состоящей из С3Н6-70%, С3Н8-10%, СО2-5%, О2-15%, если температура горения 1300 К, коэффициент избытка воздуха – 2, 8. Температура окружающей среды 293 К. Решение. Горючее - смесь газов (формула 1.2.7).
Объём продуктов горения определяется по формуле (1.2.8)
Так как газовая смесь содержит в составе кислород, он будет окислять часть горючих компонентов, следовательно, понизится расход воздуха (формула 1.1.5). В этом случае теоретический объём азота удобнее определять по формуле (1.2.14)
Теоретический объём продуктов горения
Практический объём продуктов горения
Объём продуктов горения при температуре 1300 К
Пример 5. Определить состав продуктов горения метилэтилкетона. Решение. При такой постановки задачи рационально определить непосредственно из уравнения горения объём продуктов в кмолях, выделившихся при сгорании 1 кмоля горючего
По формуле (1.2.11) находим состав продуктов горения
Пример 6. Определить объём и состав продуктов горения 1 кг минерального масла состава: С-85%, Н-15%, если температура горения 1450 К, коэффициент избытка воздуха – 1, 9. Решение. По формулам (1.2.3 - 1.2.6) определим объём продуктов горения
Теоретический объём продуктов горения при нормальных условиях
Практический объём продуктов горения при нормальных условиях формула (1.2.10)
Объём продуктов горения при температуре 1450 К
Очевидно, что состав продуктов горения не зависит от температуры горения, поэтому целесообразно определить его при нормальных условиях. По формулам (1.2.11; 1.2.13)
Пример 7. Определить количество сгоревшего ацетона, кг, если объём выделившийся двуокиси углерода, приведённый к нормальным условиям, составил 50 м3. Решение. Запишем уравнение реакции горения ацетона в воздухе
Из уравнения следует, что при горении из 58 кг (молекулярная масса ацетона) выделяется
Пример 8. Определить количество сгоревшей органической массы состава C-58%, O-22%, H-8%, N-2%, W-10% в помещении объёмом 350 м3, если содержание двуокиси углерода составило 5%. Решение. Определим объём выделившейся двуокиси углерода
По формуле (1.2.6) для вещества сложного состава определим объём СО2, выделившейся при горении 1 кг горючего,
Определим количество сгоревшего вещества
Пример 9. Определить время, когда содержание двуокиси углерода в помещении объёмом 480 м3 в результате горения древесины (C-45%, H-50%, O-42%, W-8%) составило 8%, если удельная массовая скорость выгорания древесины 0, 008 кг/(м2с), а поверхность горения 38 м2. При решении газообмен с окружающей средой не учитывать, разбавлением в результате выделения продуктов горения пренебречь. Решение. Поскольку не учитывается разбавление продуктов горения, определяем объём выделившейся в результате горения двуокиси углерода, соответствующей 8% её содержания в атмосфере
Из выражения (1.2.3) определим, сколько должно сгореть горючего материала, чтобы выделился данный объём двуокиси углерода
Время горения определим, исходя из соотношения
где Мг - масса выгоревшей древесины, кг;
F - поверхность горения, м2;
Задание на самостоятельную работу Задача: Определить объем продуктов горения при сгорании 1 кг заданного вещества, если тепература горения... К, давление... мм рт.ст., a=....
Задача: Определить объем и состав (% об.) продуктов горения, выделившихся при сгорании 1 м3 горючего газа, если температура горения составила... К, давление... мм рт.ст.
|

 O2+
O2+  N2=2CO2+H2O+
N2=2CO2+H2O+  м3/м3
м3/м3
 м3/м3
м3/м3 O2+
O2+  N2=6CO2+3H2O+
N2=6CO2+3H2O+  м3/кг
м3/кг м3/кг
м3/кг м3/м3
м3/м3 м3/кг
м3/кг м3/кг
м3/кг м3/кг
м3/кг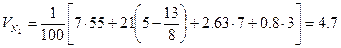 м3/кг
м3/кг =1+0, 8+0, 05+4, 7=6, 55 м3/кг
=1+0, 8+0, 05+4, 7=6, 55 м3/кг (1, 3-1)=6, 55+1, 8=8, 35 м3/кг
(1, 3-1)=6, 55+1, 8=8, 35 м3/кг =
=  м3/кг.
м3/кг.

 м3/м3
м3/м3 м3/м3
м3/м3 м3/м3
м3/м3 м3/м3
м3/м3
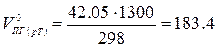 м3/м3.
м3/м3. ,
,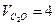 кмоля;
кмоля;  кмоля;
кмоля;  кмоля;
кмоля;  кмоля.
кмоля.

 м3/кг
м3/кг м3/кг
м3/кг м3/кг
м3/кг м3/кг
м3/кг м3/кг
м3/кг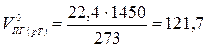 м3/кг
м3/кг ;
;  ;
;


 м3 двуокиси углерода. Тогда для образования 50 м3 двуокиси углерода должно вступить в реакцию Мг горючего
м3 двуокиси углерода. Тогда для образования 50 м3 двуокиси углерода должно вступить в реакцию Мг горючего кг
кг м3.
м3. м3/кг.
м3/кг. кг.
кг. м3
м3 кг.
кг.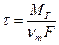 ,
, - время горения;
- время горения; - массовая скорость выгорания древесины, кг/(м2с);
- массовая скорость выгорания древесины, кг/(м2с); мин.
мин.


