равновесие идеальных двухкомпонентных смесей
Жидкие смеси могут состоять из компонентов с полной растворимостью, с ограниченной растворимостью и полной нерастворимостью компонентов.
Смеси с полной взаимной растворимостью делятся на идеальные и неидеальные. Идеальные смеси подчиняются закону Рауля, неидеальные не подчиняются.
Закон Рауля:
Парциальное давление компонента идеальной смеси  над раствором при равновесии пропорционально его мольной доле в жидкости
над раствором при равновесии пропорционально его мольной доле в жидкости 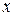 .
.
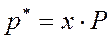 ,
,
Обозначим низкокипящий компонент (НКК) через  , его температура кипения tКА, а высококипящий компонент (ВКК) через
, его температура кипения tКА, а высококипящий компонент (ВКК) через  , его температура кипения tКВ.
, его температура кипения tКВ. 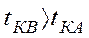
 ,
, 
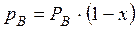 ,
,
где  - давление насыщенных паров компонентов А и В;
- давление насыщенных паров компонентов А и В;
 - парциальное давление;
- парциальное давление;
x - мольная доля НКК в жидкости;
1 -x - мольная доля ВКК в жидкости.
Закон Дальтона
 ,
где P – общее давление.
Состав жидкой фазы при достижении равновесия можно рассчитать: ,
где P – общее давление.
Состав жидкой фазы при достижении равновесия можно рассчитать:
 , ,
 , т.е. , т.е. 
|  Кривые зависимости давления насыщенных паров компонентов А и В от температуры
Кривые зависимости давления насыщенных паров компонентов А и В от температуры
|
Согласно закону Дальтона парциальное давление компонента равно общему давлению, умноженному на мольную долю этого компонента в газовой или паровой смеси, т.е.
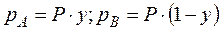
,
где y - мольная доля низкокипящего компонента в парах;
(1 -y) - мольная доля высококипящего компонента в парах.
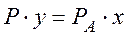
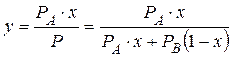 - уравнение равновесной кривой идеальной двухкомпонентной системы.
- уравнение равновесной кривой идеальной двухкомпонентной системы.
Если делить дробь на РВ и ввести отношение 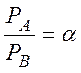 (
( - относительная летучесть компонента А), то
- относительная летучесть компонента А), то

|  Чем меньше относительная летучесть, тем труднее разделяются смеси, т.е. тем больше будут затраты на проведение ректификации.
Чем меньше относительная летучесть, тем труднее разделяются смеси, т.е. тем больше будут затраты на проведение ректификации.
|
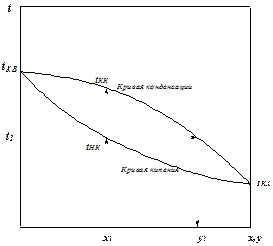
| На диаграмме t-x,y нижняя кривая – кипения, верхняя – кривая конденсации. Под кривой кипения находится жидкая фаза, точки выше кривой конденсации характеризуют перегретый пар, точки внутри гетерогенной области характеризуют неустойчивую парожидкостную смесь. Узлы кривых соответствуют чистым компонентам, которые кипят при постоянной температуре. Смеси выкипают в некотором диапазоне температур tнк ¸ tкк.
|
При кипении смеси получают пар, в котором концентрация НКК больше, чем в жидкости:
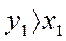
,
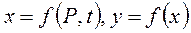
.
Давление насыщенных паров индивидуальных веществ можно рассчитать по уравнению Антуана, если нет в справочнике готовых PA, PB.
Для неидеальных смесей данные по равновесию определяют экспериментально и приводят в справочниках.
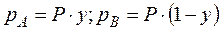 ,
,
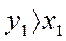 ,
, 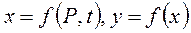 .
.

 над раствором при равновесии пропорционально его мольной доле в жидкости
над раствором при равновесии пропорционально его мольной доле в жидкости 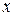 .
.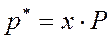 ,
, , его температура кипения tКА, а высококипящий компонент (ВКК) через
, его температура кипения tКА, а высококипящий компонент (ВКК) через  , его температура кипения tКВ.
, его температура кипения tКВ. 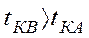
 ,
, 
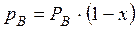 ,
, - давление насыщенных паров компонентов А и В;
- давление насыщенных паров компонентов А и В; - парциальное давление;
- парциальное давление; ,
где P – общее давление.
Состав жидкой фазы при достижении равновесия можно рассчитать:
,
где P – общее давление.
Состав жидкой фазы при достижении равновесия можно рассчитать:
 ,
,
 , т.е.
, т.е. 
 Кривые зависимости давления насыщенных паров компонентов А и В от температуры
Кривые зависимости давления насыщенных паров компонентов А и В от температуры
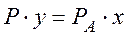
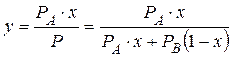 - уравнение равновесной кривой идеальной двухкомпонентной системы.
- уравнение равновесной кривой идеальной двухкомпонентной системы.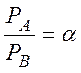 (
( - относительная летучесть компонента А), то
- относительная летучесть компонента А), то
 Чем меньше относительная летучесть, тем труднее разделяются смеси, т.е. тем больше будут затраты на проведение ректификации.
Чем меньше относительная летучесть, тем труднее разделяются смеси, т.е. тем больше будут затраты на проведение ректификации.




