Лаб. раб. 2. Определение энтальпии реакции. 1. Вычислите ΔH в реакции: 2В2S3(к) + 9O2(г) ↔ 2В2O3(к) + 6SO2(г), если
1. Вычислите ΔH ΔH0обр, кДж/моль -252 0 -1254 -297 2. Рассчитайте энтальпию образования (ΔH 3. Укажите знак ΔH0 в процессах: а) горение алюминия; б) расщепление крахмала; в) нейтрализация соляной кислоты гидроксидом калия.
Лаб. раб. 3. Скорость химических реакций. Химическое равновесие 1. Выразите математически скорости прямой и обратной реакций, протекающих в гомогенной системе: СО + Н2О ↔ CO2 + Н2. 2. Выразите математически скорости прямой и обратной реакций, протекающих в гетерогенной системе: H2O(г) + Fe(к) ↔ Fe2O3(к) + H2(г). 3. Напишите формулу для вычисления константы равновесия реакции: N2(г) + О2(г) ↔ NО2(г). 4. В каком направлении будет смещаться равновесие обратимой реакции: NO + O2 ↔ NO2 при повышении температуры?
Лаб. раб. 4. Растворы электролитов 1. Укажите, какие из солей ZnCl2, BaSO4, Cr(CH3COO)3 гидролизуются? Напишите для них молекулярные и ионные уравнения гидролиза. Укажите характер (рН) среды в растворе каждой из солей. 2. Рассчитайте степень диссоциации борной кислоты HBO3, в 0,001 М растворе, если Кд = 5,8 ∙ 10-10. 3. Определите рН водных растворов НСl и НNО2 (Кд = 4,6 · 10-4), если их концентрация равна 0,025 моль/л. 4. Рассчитайте растворимость ZnS (моль/л) при комнатной температуре, если ПР = 1,6 ∙ 10-24. Лаб. раб. 5. Окислительно-восстановительные реакции 1. Подберите коэффициенты методом электронного баланса в уравнениях реакций: Ca3(PO4)2+ C + SiO2 → Ca2SiO4 + P4 + CO (NH4)2Cr2O7 → Cr2O3 + N2 + H2O RhF6 + Cl2 → RhF3 + ClF 2. Составьте уравнение реакции и подберите коэффициенты методом электронного баланса: хлорат калия + оксид марганца (IV) + гидроксид калия → манганат калия + хлорид калия + …
|

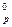 в реакции: 2В2S3(к) + 9O2(г) ↔ 2В2O3(к) + 6SO2(г), если
в реакции: 2В2S3(к) + 9O2(г) ↔ 2В2O3(к) + 6SO2(г), если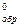 ) NH3, если при образовании 1,7 г выделилось 4,6 кДж тепла.
) NH3, если при образовании 1,7 г выделилось 4,6 кДж тепла.


