Лаб. раб. 6. Коррозия металлов и защита от коррозии
1. В каком из контактов скорость коррозии меньше: а) Mg/Zn; б) Mg/Ni; в) Mg/Ag? Ответ подтвердите расчетами. 2. В контакте с каким из указанных металлов Ni является катодом: Zn, Fe, Ag? 3. Составьте схему работы гальванопары (анодный и катодный процессы) Ni/Cu в щелочной среде. Задание к лабораторным работам Вариант 23
Лаб. раб. 1. Основные классы неорганических соединений 1. Назовите по систематической номенклатуре следующие вещества: CuCl2, NaOH, Cu(OH)2, NaCl. 2. Рассчитать массу 10 м3 ацетилена при н.у. 3. Рассчитать молярную массу вещества, если 10 г его занимают при температуре 800С и давлении 200000 Па объем 3,34 л. 4. Рассчитать объем воздуха при н.у., необходимый для сжигания 1 м3 бытового газа (70% С3Н8, 30% С4Н10). 5. Определить объем хлора, который можно получить из 1 т руды, содержащей 70% NaCl и 30% KCl.
Лаб. раб. 2. Определение энтальпии реакции 1. Рассчитайте ΔH ΔH0обр, кДж/моль -1120 0 -272 -110 2. Рассчитайте энтальпию образования (ΔH 3. Укажите знак ΔH в процессах: а) CS2 + 3O2 → CO2 + 2SO2; б) HI(г) → HI(ж); в) TiCl4 → Ti + 2Cl2.
Лаб. раб. 3. Скорость химических реакций. Химическое равновесие 1. Выразите математически скорости прямой и обратной реакций, протекающих в гомогенной системе: NH3 + O2 ↔ N2 + H2O. 2. Выразите математически скорости прямой и обратной реакций, протекающих в гетерогенной системе: Fe3O4(к) + H2(г) ↔ Fe(к) + H2O(г). 3. Напишите формулу для вычисления константы равновесия реакции:PCl5(г) ↔ PCl3(г) + Cl2(г). 4. В каком направлении будет смещаться равновесие обратимой реакции: N2 + H2 ↔ NH3 при повышении давления?
|

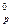 реакции: Fe3O4(к) + C(к) ↔ 3FeO(к) + CO(г), если
реакции: Fe3O4(к) + C(к) ↔ 3FeO(к) + CO(г), если ) CCl4, если при образовании 15,4 г выделилось 13,5 кДж.
) CCl4, если при образовании 15,4 г выделилось 13,5 кДж.


