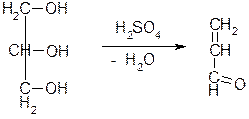Физические и химические свойства жиров
Физические свойства. Жиры при обычной температуре имеют плотную или мягкую консистенцию. Жирные масла являются густыми, прозрачными жидкостями. На бумаге жиры оставляют жирное пятно, которое при нагревании еще сильнее расплывается (отличие от эфирных масел). Окраска, запах и вкус жиров зависят от сопутствующих веществ. Окраска чаще белая или желтоватая. Запах отсутствует или слабый, специфический. Вкус нежный и маслянистый, реже неприятный, как у касторового масла. Жиры легче воды, плотность от 0,910 до 0,970. Большинство жиров оптически неактивны. Исключение составляет касторовое масло. Показатель преломления (коэффициент рефракции) характерен и постоянен для каждого масла. Так, у оливкового масла он составляет 1,46-1,71. Чем выше молекулярная масса глицеридов и чем больше двойных связей, тем выше показатель преломления. Все жиры нерастворимы в воде, мало растворимы в этаноле, легко растворимы в эфире, хлороформе, петролейном эфире. Исключение: касторовое масло легко растворимо в 96 % этаноле, трудно - в петролейном эфире. Сами жиры являются хорошими растворителями для многих лекарственных веществ (камфора, гормоны, эфирные масла и др.). Жиры хорошо смешиваются между собой. Химические свойства жиров обусловлены наличием: 1) сложных эфирных связей; 2) двойных связей в углеводородных радикалах жирных кислот; 3) наличием глицерина в составе жира. 1.1. Жиры легко подвергаются гидролитическому расщеплению при участии ферментов с образованием глицерина и жирных кислот. Ферментативный гидролизпроисходит ступенчато. Фермент липаза содержится во всех семенах масличных растений. Гидролизу способствуют влага и повышенная температура. Происходит гидролитическое прогоркание жира. Указанное свойство учитывается при хранении жиров. 1.2. Жиры расщепляются под действием щелочей с образованием глицерина и солей жирных кислот. Соли называют мылами: калиевые мыла - жидкие, натриевые - твердые. Процесс называют омылением.
Свойство используется при анализе жиров. На нем основано производство мыл и шампуней. 2. По двойным связям жирных кислот могут присоединяться водород, галогены, кислород. 2.1. Присоединение водорода - гидрирование жиров (гидрогенизация жиров) идет при повышенной температуре в присутствии катализатора (никель). Непредельные жирные кислоты переходят в предельные, жидкие масла превращаются в твердые. Получают саломассы, их используют в медицинской практике как мазевые и суппозиторные основы (бутирол) и в пищевой промышленности (производство маргарина). 2.2. Присоединение галогенов используют в анализе жиров при определении химической константы - йодного числа. 2.3. Присоединение кислорода воздуха приводит к окислению и прогорканию жиров. Различают химическое окисление (альдегидное) и биохимическое при участии микроорганизмов (кетонное). Жиры приобретают специфический вкус и запах и становятся непригодными к употреблению. Изменяется цвет жира (чаще жиры обесцвечиваются); изменяются физические и химические свойства: увеличиваются плотность и кислотное число, уменьшаются йодное число и вязкость. Различают 3 вида окислительного прогоркания: а) неферментативное - кислород присоединяется по месту двойных связей, образуя пероксиды; при разложении пероксидов жирных кислот получаются альдегиды.
б) ферментативное с участием липоксидаз и липоксигеназ, образуются гидропероксиды.
Гидропероксиды способны окислять биологически активные вещества, содержащиеся в масле, например каротиноиды. Гидропероксиды подвергаются разложению с образованием альдегидов и кетонов. Свойство учитывают при хранении жиров и при их анализе. в) ферментативное (кетонное) - происходит при участии микроорганизмов.
3. Глицерин,входящий в состав жира, подвергается окислению и дегидратации при нагревании жира с концентрированной кислотой серной. При этом образуется альдегид акролеин, имеющий неприятный запах. Акролеиновая проба позволяет отличить жиры от жироподобных веществ.
|