Примеры решения задач. Пример 7.1. Водный раствор содержит 354 г H3PO4 в 1 л
Пример 7.1. Водный раствор содержит 354 г H3PO4 в 1 л. Плотность раствора ρ = 1,18 г/мл. Вычислить: а) массовую долю (%) H3PO4 в растворе; б) молярную концентрацию; в) молярную концентрацию эквивалентов; г) моляльность; д) титр; е) молярные доли H3PO4 и Н2О. Решение. а). Для расчета массовой доли воспользуемся формулой
б). Молярная концентрация вещества В или молярность(с В или М) – отношение количества растворенного вещества к объему раствора:
где n B – количество вещества В, моль; m B – масса вещества В, г; М В– молярная масса вещества В, г/моль; V р– объем раствора, л. Молярная масса H3PO4 равна 98 г/моль. Молярную концентрацию раствора находим из соотношения (1):
в). Молярную концентрацию эквивалентов рассчитываем по формуле г). Моляльная концентрация вещества В или моляльность(с m(B)) – отношение количества растворенного вещества к массе растворителя:
где n В – количество вещества В, моль; m B – масса вещества В,г; m S – масса растворителя, г; М В − молярная масса вещества В, г/моль. Для определения моляльности по формуле (2) необходимо рассчитать массу растворителя в растворе. Масса раствора составляет 1,18∙1000 = 1180 г. Масса растворителя в растворе m S = 1180 – 354 = 826 г. Моляльная концентрация раствора равна
д). Титр раствора можно рассчитать по формулам:
е). Молярная (мольная) доля вещества В(х В), безразмерная величина – отношение количества данного вещества к суммарному количеству всех веществ, составляющих раствор, включая растворитель. Если раствор состоит из одного растворенного вещества и растворителя, то молярная доля вещества (х В) равна
а молярная доля растворителя (x S)
где n B – количество растворенного вещества, моль; n S – количество вещества растворителя, моль. Сумма молярных долей всех веществ раствора равна единице. В 1 л раствора содержится 3,61 моль H3PO4 (см. пункт б). Масса растворителя в растворе 826 г, что составляет Молярные доли H3PO4 и Н2О рассчитываем по формулам (3) и (4):
Пример 7. 2. Сколько миллилитров 50 %-го раствора HNO3, плотность которого 1,32 г/мл, требуется для приготовления 5 л 2 %-го раствора, плотность которого 1,01 г/мл? Решение. При решении задачи пользуемся формулой
Сначала находим массу азотной кислоты в 5 л 2 %-го раствора:
Чтобы ответить на вопрос задачи, надо определить, в каком объеме раствора с массовой долей HNO3 50 % содержится 101 г HNO3:
Таким образом, для приготовления 5 л 2 %-го раствора HNO3 требуется 153 мл 50 %-ного раствора HNO3. Пример 7. 3. На нейтрализацию 50 мл раствора Решение. Так как вещества взаимодействуют между собой в эквивалентных количествах, то можно написать V A ∙;н. (А) = V B ∙;н. (B); 50∙н. (кислоты ) = 25∙0,5, отсюда н. (кислоты) = Следовательно, для реакции был использован 0,25 н. раствор кислоты.
|

 ;
;  .
. , моль/л, (1)
, моль/л, (1) =
=  3,61 моль/л.
3,61 моль/л. . Молярная масса эквивалентов H3PO4 равна
. Молярная масса эквивалентов H3PO4 равна  32,7 г/моль.
32,7 г/моль. 
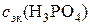 =
= 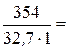 10,83 моль/л.
10,83 моль/л. , моль/кг, (2)
, моль/кг, (2) = 4,37 моль/кг.
= 4,37 моль/кг. ;
;  =
=  = 0,354 г/мл,
= 0,354 г/мл, ;
;  = 0,354 г/мл,
= 0,354 г/мл, ;
; 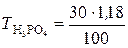 = 0,354 г/мл.
= 0,354 г/мл. , (3)
, (3) , (4)
, (4) = 45,9 моль.
= 45,9 моль.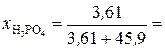 0,073;
0,073;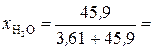 0,927.
0,927.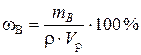 .
. 101 г.
101 г. = 153 мл.
= 153 мл. 0,25 н..
0,25 н..


