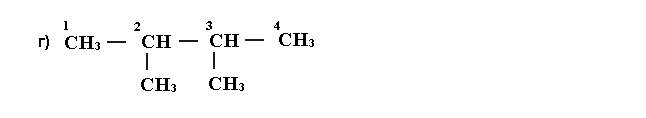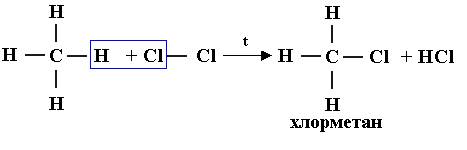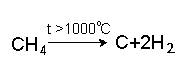Темазанятия по КТП
Дисциплина ОД.10 химия
Курс 1курс
Цель Сформировать понятие о предельных углеводородах Предельных углеводородах. Познакомить студентов со строением и свойствами алканов на примере метана. Развивать умение сравнивать обобщать и устанавливать причинно- следственную связь между строением и свойствами веществ
Углеводороды - это органические соединения, состоящие из двух элементов - углерода и водорода. Алканы - название предельных углеводородов по международной номенклатуре. Предельные углеводороды - это углеводороды с общей формулой CnH2n+2, которые не присоединяют водород и другие элементы. Парафины - исторически сохранившееся название предельных углеводородов (лат. parrum affinis - малоактивный). Гомологический ряд предельных углеводородов
Общая формула предельных углеводородов CnH2n+2 В таблице "Гомологический ряд предельных углеводородов" встречается термин "свободные радикалы"- это частицы, имеющие неспаренные электроны и обладающие в связи с этим неиспользованными валентностями. Номенклатура углеводородов 1. Выбирают в формуле наиболее длинную углеродную цепь и символы атомов углерода в ней нумеруют, начиная с того конца цепи, к которому ближе разветвление:
2. Называют радикалы (начиная с простейшего) и при помощи цифр указывают их место у нумерованных атомов углерода. a. 2-метил… b. 2,2-диметил… c. 3-метил… d. 2,3-диметил… 3. Полное название данному углеводороду дают по числу атомов углерода в нумерованной цепи: a. 2-метилпентан b. 2,2-диметилбутан c. 3-метилпентан d. 2,3-диметилбутан Физические свойства Метан - газ без запаха и цвета, почти в два раза легче воздуха, мало растворим в воде. Этан, пропан, бутан при нормальных условиях - все они газы. От пентана до пентадекана - жидкости. Следующие гомологи - твердые вещества. Химические свойства 1.Наиболее характерными реакциями предельных углеводородов являются реакции замещения.
2.Все предельные углеводороды горят с образованием оксида углерода(IV) и воды. Метан горит бесцветным пламенем, с выделением теплоты: CH4+2O2=CO2+2H2O+880кДж 3.При сильном нагревании (выше 1000oС) без доступа воздуха предельные углеводороды разлагаются:
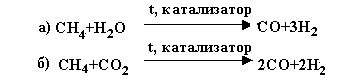
Нахождение в природе Метан образуется в природе при разложении растительных и животных организмов без доступа воздуха. Метан составляет основную массу природного газа (80-97%). Он содержится и в газах, выделяющихся при добыче нефти. В состав природного газа и нефтяных газов входят также этан C2H6, пропан C3H8, бутан C4H10 и др. Газообразные, жидкие и твердые предельные углеводороды содержатся в нефти. Применение Применение метана очень разнообразно. В виде природного газа метан широко используется в качестве топлива. Метан является исходным продуктом для получения метанола, уксусной кислоты, синтетических каучуков, синтетического бензина и многих других ценных продуктов. Для синтеза многих упомянутых продуктов в промышленности используется так называемый синтез - газ, который получают из метана. Обычно объемный (молярный) состав этого газа соответствует смеси, состоящей из одного объема оксида углерода (II) и двух объемов водорода (CO+2H2).
Вопросы для самоконтроля
1. Дайте определение и назовите общую формулу алканов 2. Запишите молекулярную и структурную формулу этана 3. Назовите способы получения алканов 4. Охарактеризуйте физические свойства алканов 5. Запишите уравнения характеризующие химические свойства алканов на примере пропана 6. Назовите области применения алканов 7. Назовите виды изомерии характерные для алканов
|