Концентрирование H2SO4
Во многих производствах H2SO4 используется как водоотнимаюшее средство, также при оргсинтезе разбавленная кислота получается как отход, при башенном способе тоже получается разбавленная H2SO4,=> необходимо концентрировать. Но при нагревании растворов H2SO4 сначало из них испаряется вода, и повышается концентрация кислоты при с=80% появляются пары серной кислоты при дальнейшем концентрировании количество паров увеличивается. Зависимость t кип H2SO4 и ее содержание в паре от концентрации кислоты.
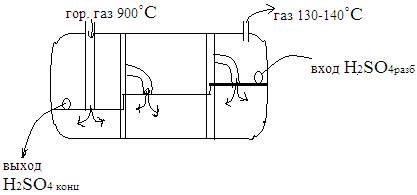
Для 98% H2SO4 в паре обе кривые совпадают. => 100% кислоту получить не возможно. Для концентрации H2SO4 применяю аппараты двух видов: I. аппараты, где тепло топочных газов передается концентрируемой кислоте через стенки. II. Аппараты, где тепло топочных газов передается непосредственно соприкосновении с кислотой путем пропускания их над поверхностью кислоты или барботажа через слой кислоты В аппаратах II типа тепло используется более рационально, но кислота загрязняется, поэтому используют очищенный природный газ или мазут. В I аппарате трудно подобрать материал, горячая кислота разъедает стенки, и плохая теплопроводность. Концентрирование кислоты осуществляется в барбатажных барабанах- концентраторах, длиной 15м, разделенный перегородками.
При кипячении разбавленной H2SO4 вначале в паровую фазу переходит только вода, когда концентрация достигает 70% в паровой фазе появляется H2SO4 При концентрации 98,3% t = 336,6˚С, состав паровой фазы равен жидкой фазы, т.е. получается азеотропная смесь.
|