Классическая теория теплоемкости
Как известно из статистической физики, энергия ситстемы равнораспределена по степеням свободы (возможным движениям тела) и на каждую степень свободы молекулы приходится одинаковая энергия, равная
где f – количество степеней свободы. Количество молекул N можно вычислить как произведение числа Авогадро N A на число киломолей ν газа, которое определяется делением массы газа M на молярную массу газа μ. Таким образом,
Учитывая, что
Теплоемкости при постоянном объеме и при постоянном давлении для идеального газа
Формула для cp получена с учетом известной формулы Майера
Отношение теплоемкостей равно
Вычисленные по этим формулам значения теплоемкостей для различных газов сравнительно хорошо совпадают с экспериментально измеренными их значениями в области комнатных температур. Расхождение с экспериментом становится существенным при повышении температуры. Главной причиной расхождения теории с экспериментом является то, что при получении выражения для внутренней энергии газов не принимались во внимание квантовые эффекты, учет которых приводит к тому, что число вращательных и колебательных степеней свободы молекул перестает быть постоянной величиной, а зависит от энергии столкновения молекул, т.е., от температуры. Кроме того, с увеличением температуры многоатомные молекулы частично диссоциируют и химический состав газа может заметно измениться. Лекция 4
|

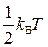 , где
, где 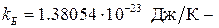 постоянная Больцмана. Тогда внутренняя энергия идеального газа равна
постоянная Больцмана. Тогда внутренняя энергия идеального газа равна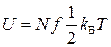 .
. .
. , получим
, получим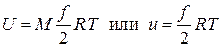 .
.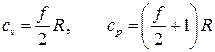 .
. .
. .
.


