ИДЕАЛЬНЫЙ ГАЗ
1.10 В баллоне объемом V = 3 л находится m = 4 г кислорода. Определить количество вещества, количество молекул N и их концентрацию n в баллоне. 1.11 Определить число атомов N ртути и количество вещества, содержащихся в объеме V = 1 см3 при температуре t=270°С, если давление паров ртути Р=0,75 Па. 1.12 Одна треть молекул азота массой 10 г распалась на атомы. Определить полное число частиц N, находящихся в газе. 1.13 В сосуде объемом V = 5 л находится однородный газ количеством вещества 0,2 моля. Определить, какой это газ, если его плотность 1,12 кг/м3. 1.14 В сосуде объемом V = 5 л находится кислород, концентрация молекул которого равна n = 9,41 1023 м–3. Определить массу газа m. 1.15 Рассматривая молекулы жидкости как шарики, соприкасающиеся друг с другом, оценить порядок размера молекулы жидкого сероуглерода СS2. Плотность сероуглерода равна 1,26∙103 кг/м3. 1.16 В сосуде объемом V = 48 дм3 находится N1 = 1,9∙1024 молекул водорода, 3,5 моля азота и m3 = 200 г аргона. Определить среднее расстояние между молекулами смеси газов. 1.17 Радоновые ванны содержат N = 1,8∙106 атомов радона на V = 1 дм3 воды. На сколько молекул воды приходится атом радона? Плотность воды 103 кг/м3. 1.18 Концентрация молекул в некоторой жидкости n = 2 1027 м–3. Оцените, за какое время испарится эта жидкость, налитая в цилиндрический сосуд диаметром d = 10 см и высотой Н = 3 см. Скорость испарения жидкости из сосуда считать постоянной и равной ΔN/Δt = 5∙1020 1/с. 1.19 В сосуде объемом V = 1,12 л находится азот при нормальных условиях. При нагревании до некоторой температуры 30% молекул распалось на атомы. Определить количество вещества азота после нагревания. 1.20 В сосуде объемом V = 8 л находится m = 8 г гелия при давлении Р = 105 Па. Определить количество молекул гелия в сосуде и их полную кинетическую энергию. 1.21 На сколько изменилась температура аргона, если средняя кинетическая энергия его атома уменьшилась в k = 1,2 раза? Начальная температура аргона Т0 = 400 К. 1.22 Чему равна средняя кинетическая энергия движения молекулы аргона, если 2 моля этого газа в баллоне объемом V = 10 л создают давление Р = 106 Па? 1.23 В сосуде объемом V = 20 см3 при температуре t = 27°С и давлении Р = 104 Па находится идеальный одноатомный газ. Определить число атомов в сосуде и их суммарную кинетическую энергию. 1.24 При некоторой температуре молекулы кислорода имеют среднюю квадратичную скорость vср.кв.1 = 460 м/с. Какова при этой температуре средняя квадратичная скорость vср.кв.2 молекул азота? 1.25 В закрытом сосуде находится идеальный газ. На сколько процентов изменится его давление, если средняя квадратичная скорость его молекул увеличится на 20%? 1.26 Давление идеального газа после его нагревания в закрытом сосуде увеличилось в k = 16 раз. Во сколько раз изменилась средняя квадратичная скорость его молекул? 1.27 Каково давление идеального газа, если его плотность равна 3 кг/м3, а средняя скорость его молекул vср.кв. = 100 м/с? 1.28 Средняя квадратичная скорость молекул некоторого газа при температуре Т = 296 К равна vср.кв. = 480 м/с. Сколько молекул содержится в m = 10 г этого газа? 1.29 Давление воздуха внутри плотно закупоренной бутылки при температуре t1 = 7°С было Р1 = 100 кПа. При нагревании бутылки пробка вылетела. До какой температуры t2 нагрели бутылку, если известно, что пробка вылетела при давлении воздуха в бутылке Р2 = 130 кПа. 1.30 Найти массу воздуха, заполняющего аудиторию высотой h = 5 м и площадью пола S = 200 м3. Давление воздуха Р = 105 Па, температура в помещении t = 170С. 1.31 В цилиндре длиной L = 1,6 м, заполненном воздухом при нормальном атмосферном давлении Р0 = 105 Па, начали медленно вдвигать поршень площадью S = 200 см2. Определить силу F, которая будет действовать на поршень, если его остановить на расстоянии h = 10 см от дна цилиндра. 1.32 Во сколько раз плотность воздуха, заполняющего помещение зимой (t1 = 70С), больше его плотности летом (t2=270С)? Давление газа считать постоянным. 1.33 Некоторый газ при температуре t = 100С и давлении Р = 200 кПа имеет плотность 0,34 кг/м3. Определить, что это за газ. 1.34 Масса m = 12 г газа занимает объем V = 4 л при температуре t1 = 70С. После нагревания газа при постоянном давлении его плотность стала равной 0,6 кг/м3. До какой температуры T2 нагрели газ? 1.35 Масса m = 10 г кислорода находится при давлении Р = 304 кПа и температуре t1 = 100С. После нагревания при постоянном давлении кислород занял объем V2 = 10 л. Определить объем газа до расширения V1, температуру Т2 газа после расширения, плотности газа до и после расширения. 1.36 При повышении температуры на Т = 3 К объем газа увеличился на α= 1 %. Какова была начальная температура газа, если процесс протекал изобарически? 1.37 При сгорании топлива в цилиндре дизельного двигателя вовремя предварительного расширения объем газа увеличился в n = 2,2 раза при постоянном давлении. Определить изменение температуры газа, если начальная температура была равна Т = 1650 К. 1.38 Воздушный шарик внесли с улицы, где температура воздуха была t1 = –130С, в комнату с температурой t2 = 170С? На сколько процентов изменится объем шарика? Натяжением резины пренебречь. 1.39 Баллон, содержащий m1 = 1,45 кг азота, при испытании лопнул при температуре t1 = 4270С. Какую массу кислорода m2 можно хранить в таком же баллоне при температуре t2 = 170С, имея четырехкратный запас прочности (т.е. давление в баллоне не должно превышать одной четвертой значения давления, при котором баллон разрушается)? 1.40 Баллон содержит сжатый идеальный газ при температуре t1 = 270С и давлении Р1 = 0,2 МПа. Каким будет давление Р2 в баллоне, когда из него будет выпущено α= 0,7 массы газа, а температура понизится до t2 = 00С? 1.41 В баллоне емкостью V = 0,5 м3 находится идеальный газ при температуре t = 270С. Вследствие утечки давление снизилось на ∆Р = 103 Па. Какое количество молекул вышло из баллона, если температура газа не изменилась? 1.42 Из баллона выпустили ∆ m = 2 г идеального газа, в результате чего давление уменьшилось на α= 10%. Определить объем баллона, если вначале плотность газа была равна 2·10–4 г/см3. Температура газа постоянна. 1.43 Стеклянная колба с воздухом при атмосферном давлении Р0 = 105 Па взвешена при температуре t1 = 800С. Воздух в колбе нагревают до t2 = 185ºС. При последующем взвешивании колба оказалась на ∆m = 0,25 г легче. Чему равен объем колбы V? Молярная масса воздуха 0,029 кг/моль. 1.44 При аэродинамическом торможении в атмосфере планеты температура внутри автоматического спускаемого аппарата увеличилась с t1 = 200С до t2 = 800С. Какую часть воздуха необходимо выпустить, чтобы давление внутри аппарата не изменилось? 1.45 Аэростат наполнен водородом при нормальном атмосферном давлении Р0 = 105 Па и температуре t0 = 150С. В солнечный день температура водорода поднялась до t = 370С. Чтобы давление в оболочке не изменилось, m = 6 кг водорода было выпущено через клапаны. Определить объем аэростата. 1.46 При уменьшении объема, занимаемого идеальным газом, на α= 10%, температура газа увеличилась на t = 160С, а давление возросло на β= 20%. Какова начальная температура газа? 1.47 Определить, на сколько процентов изменилось количество газа в сосуде, если объем сосуда увеличился на α= 20%, давление возросло на β= 10%, а температура увеличилась на γ= 40%. 1.48 В сосуде объемом V1 = 4·10–3 м3 при давлении Р1 = 1 атм находится m = 2 г водорода. Газ сжали. При этом давление газа стало равным Р2 = 4 атм, а объем уменьшился на ∆V = 2 10–3 м3. На сколько изменилась температура газа? 1.49 Перед стартом при нормальных условиях объем аэростата с эластичной оболочкой был равен V1 = 4000 м3. Аэростат поднялся на высоту, где давление составляет Р = 5·104 Па, а температура понижается до t = –170С. На сколько изменился объем аэростата? Натяжением материала оболочки пренебречь. 1.50 Эластичная оболочка метеозонда, заполненная гелием массой m = 1 кг при температуре Т = 300 К, была пробита метеоритом. Сечение отверстия S = 10 мм2. Через какое время из оболочки вытечет α = 50% газа, если скорость истечения гелия через пробоину постоянна и равна v = 5 м/с, а объем оболочки меняется так, что плотность газа остается постоянной? Молярная масса гелия 0,004 кг/моль, атмосферное давление Р0 = 105 Па. Температуру гелия считать постоянной. Натяжением материала оболочки пренебречь. 1.51 По трубе сечением S = 5·10-4 м2 течет углекислый газ под давлением Р = 3,92·105 Па при температуре Т = 280 К. Определить среднюю скорость протекания газа по трубе, если через поперечное сечение за t = 10 минут протекает m = 20 кг газа. 1.52 Аэростат объемом V = 300 м3 заполнен водородом при температуре t = 200С и давлении Р = 95 кПа. Сколько времени продолжалось заполнение, если в аэростат каждую секунду поступало m = 2,5 г водорода? 1.53 В камеру футбольного мяча объемом V = 2,5 л накачивают воздух насосом, забирающим при каждом качании V0 = 0,15 л атмосферного воздуха при давлении Р0 = 105 давление в камере мяча после n = 50 качаний, если камера вначале была пустой? Температуру воздуха считать постоянной. 1.54 Автомобильную камеру емкостью V = 10 л нужно накачать до давления Р = 2 атм. Определить, сколько качаний следует сделать насосом, забирающим при каждом качании V = 500 см3 воздуха из атмосферы, если камера вначале была заполнена воздухом при нормальном атмосферном давлении Р0 = 105 Па. Изменением температуры пренебречь. 1.55 Давление воздуха в резервуаре компрессора Р0 = 105 Па. Объем цилиндра компрессора в k = 40 раз меньше объема резервуара. Сколько качаний должен сделать поршень компрессора, чтобы давление в резервуаре стало Р = 4 атм? Изменением температуры пренебречь. 1.56 После одного хода откачивающего поршневого насоса, объем рабочей камеры которого в k = 2 раза меньше объема откачиваемого сосуда, давление воздуха в сосуде упало до Р = 16 кПа. Определить начальное давление газа в сосуде. Температуру считать постоянной. 1.57 Давление воздуха в сосуде было равно Р0 = 105 Па. После трех ходов откачивающего поршневого насоса давление воздуха упало до Р = 2 кПа. Определить отношение объема сосуда к объему цилиндра поршневого насоса. Температуру считать постоянной.
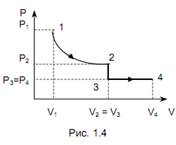
1.59 Сосуд объемом V = 87 л откачивают насосом. Определить, через какое время давление в сосуде уменьшится в n = 1000 раз. Скорость откачки считать постоянной и равной С = 10 л/с. Процесс откачки – изотермический. 1.60 Идеальный газ, занимающий объем V1 при давлении Р1 и температуре Т1 = 300 К, расширился изотермически до объема V2 = 2 л. Затем давление газа было уменьшено изохорически в k = 2 раза. Далее газ расширился при постоянном давлении до объема V4 = 4 л. Процессы, происходящие с газом, изображены на Р – V диаграмме (рис.1.4). Определить конечную температуру газа Т4. 1.61 Идеальный газ сначала изотермически сжимают в k = 4 раза, а затем изобарически расширяют в n = 3 раза. Построить этот процесс на Р – V, Р – Т и V – Т диаграммах. 1.62 Начальные параметры газа Р0, V0, Т0. Газ сначала изобарически расширили до объема V1, после чего нагрели при постоянном объеме до давления Р2. Определить температуру Т2 в конечном состоянии. 1.63 Идеальный газ сначала изохорически нагрели до абсолютной температуры в два раза большей начальной, а затем изобарически температуру еще увеличили еще в два раза. Определить отношение конечного объема к начальному объему.
1.65 В вертикальном сосуде под поршнем находится m = 1 г азота. Площадь поршня S = 10 см2, масса поршня М = 1 кг. Азот нагревают на ∆Т = 10 К. На сколько при этом поднимется поршень? Давление над поршнем нормальное Р0 = 105 Па. Трением пренебречь.
1.67 В вертикальном, открытом сверху цилиндре под поршнем находится воздух (рис.1.5). Поршень имеет форму, показанную на рисунке. Масса поршня М = 6 кг, площадь сечения S = 20 см2, атмосферное давление Р0 = 1 атм. Определить массу груза, который надо положить на поршень, чтобы объем воздуха уменьшился в два раза? Температуру считать постоянной. Трения нет. 1.68 В гладкой, открытой с обоих торцов вертикальной трубе, имеющей два разных сечения, находятся в равновесии два поршня, соединенные невесомой нерастяжимой нитью (см. рис.1.6). Между поршнями находится = 1 моль идеального газа. Площадь сечения верхнего Р0 поршня на S = 10 см2 больше, чем нижнего. Общая масса поршней m = 5 кг. Давление наружного воздуха Р0 = 1 атм. На сколько градусов надо нагреть газ между поршнями, чтобы они переместились на расстояние L = 5 см? 1.69 Газ, находящийся в вертикальном, открытом сверху цилиндре под поршнем, нагрели при постоянном давлении так, что его объем увеличился в n = 1,5 раза. Затем поршень закрепили и нагрели газ так, что его давление возросло в m = 2 раза. Найти отношение конечной температуры к начальной. 1.70 Внутри закрытого с обоих торцов горизонтального цилиндра находится в равновесии тонкий поршень. С одной стороны поршня находится m1 = 2 г водорода, с другой – m2 = 14 г азота. Какую часть объема цилиндра занимает азот, если температуры газов одинаковы? 1.71 Цилиндрический, закрытый с обоих торцов, горизонтальный сосуд длиной L0 = 40 см разделен на две части легким тонким поршнем, скользящим без трения. Поршень находится на расстоянии L1 = 26,7 см от одного из торцов цилиндра. С одной стороны поршня находится водород, а с другой – идеальный газ с неизвестной молярной массой М2. Определить М2 газа, если его масса равна массе водорода, а температуры газов одинаковы. 1.72 Закрытый с обоих торцов горизонтальный цилиндрический сосуд содержит идеальный газ при температуре t = 00С. Внутри сосуд перегорожен поршнем радиусом r = 0,02 м, не проводящим тепло, на две части объемами V1 = 10 см3 и V2 = 50 см3. Поршень находится в равновесии. На какое расстояние h переместится поршень, если газ, заключенный в большем объеме, нагреть на Т = 30 К? 1.73 Закрытый с обоих торцов горизонтально расположенный цилиндрический сосуд разделен подвижным поршнем на две части, объемы которых относятся как один к двум. Температура газа в обеих частях одинакова и равна Т0 = 300 К. До какой температуры нужно нагреть газ в сосуде меньшего объема, чтобы отношение объемов изменилось на обратное? Поршень и сосуд теплоизолированы. 1.74 Определить период малых колебаний поршня массой m, разделяющего закрытый с обоих торцов цилиндрический сосуд сечением S на две равные части длиной L каждая. По обе стороны от поршня находится воздух при давлении Р0. Трения нет. Температуру считать неизменной. 1.75 Приближенно воздух можно считать смесью азота (α1 = 80% по массе) и кислорода (α2 = 20% по массе). Определить молярную массу воздуха. 1.76 В баллоне объемом V = 7,5 л при температуре Т = 300 К находится смесь газов: 0,1 моля кислорода, 0,2 моля азота и 0,3 моля углекислого газа. Считая газы идеальными, определить: 1) давление смеси; 2) молярную массу смеси. 1.77 Сосуд объемом V = 20 л содержит смесь водорода и гелия при температуре t = 200С и давлении Р = 2 атм. Масса смеси m = 5 г. Найти отношение массы водорода к массе гелия в смеси. 1.78 Определить плотность газовой смеси водорода и кислорода, если их массовые доли равны соответственно α1 = 1/9 и α2 = 8/9. Давление смеси Р = 100 кПа, температура смеси Т = 300 К 1.79 Смесь, состоящая из кислорода и азота, находится в баллоне под давлением Р = 1 МПа. Определить парциальные давления кислорода Р1 и азота Р2, если массовая доля кислорода в смеси равна α1 = 0,2. 1.80 В двух сосудах находится одинаковый идеальный газ. Сосуды соединены трубкой с краном. В первом сосуде масса газа m1 = 1 кг при давлении Р1 = 105 кПа, во втором – m2 = 2 кг при давлени Р2 = 4·105 Па. Какое давление установится в сосудах, если открыть кран? Температуру считать постоянной. 1.81 В сосуде объемом V = 1 л находится m = 0,28 г азота. Газ нагревают до температуры t = 15000С, при которой α= 30% молекул азота диссоциировало на атомы. Определить давление в сосуде. 1.82 В сосуде находится идеальный двухатомный газ. Под действием ультрафиолетового излучения распалось на атомы α= 12% молекул и после этого установилось давление Р = 93 кПа. Определить первоначальное давление в сосуде. Температуру газа считать постоянной. 1.83 В сосуде находится идеальный двухатомный газ. При увеличении температуры в n = 3 раза давление увеличилось в k = 3,15 раза. Сколько процентов молекул от их первоначального количества распалось на атомы? 1.84 Во сколько раз изменится давление двухатомного идеального газа в сосуде, если при той же температуре треть молекул распадется на атомы? 1.85 На какой глубине h радиус пузырька вдвое меньше, чем у поверхности воды? Атмосферное давление Р0 = 105 Па, Температуру воздуха считать неизменной, плотность воды 103 кг/м3. 1.86 Аквалангист, находясь на глубине h = 15 м от поверхности воды, вдохнул воздух, заполнивший объем легких V = 5,5 л. До какого объема расширятся его легкие, если аквалангист быстро вынырнет на поверхность? Плотность воды 103 кг/м3, атмосферное давление Р0 = 105 Па. 1.87 В широкий сосуд с водой был опрокинут цилиндрический стакан (рис.1.7). Уровни воды в сосуде и стакане находятся на одинаковой высоте. Расстояние от уровня воды до дна опрокинутого стакана равно L = 40 см. На какую высоту h поднимется вода в стакане при понижении температуры от Т1 = 310 К до Т2 = 273 К? Атмосферное давление Р0 = 105 Па, плотность воды 103 кг/м3.
1.89 Стеклянная трубка длиной L0 наполовину погружена в ртуть. Ее закрывают пальцем и вынимают. При этом часть ртути вытекает. Какова длина столбика ртути, оставшегося в трубке? Атмосферное давление равно Н мм. рт. ст.
1.91 Полый шар с жесткой оболочкой, масса которой m = 10 г, наполнен водородом. Объем шара V = 10 дм3. Температура водорода и окружающего шар воздуха t = 00С. Найти давление водорода в шаре, если подъемная сила шара равна нулю. Атмосферное давление Р0 = 105 Па. 1.92 Аэростат, наполненный гелием при давлении Р0 = 105 Па и температуре Т = 300 К, должен подняться на высоту h = 1,5 км, чтобы не стать помехой движению самолетов. Плотность воздуха на такой высоте на α = 20% меньше, чем у поверхности земли. Определить массу оболочки аэростата, если его объем V = 500 м3. Оболочка нерастяжима и герметична. Давление воздуха у поверхности земли нормальное, температуру считать постоянной. 1.93 Во время сжатия идеального газа его давление и объем изменяются по закону: PV-1= const. Температура газа при этом уменьшилась в n = 4 раза. Каково было начальное давление Р1 газа, если после сжатия его давление Р2 = 105 Па? 1.94 Идеальный газ расширяется по закону: const PV2, и его объем увеличивается в n = 3 раза. Найти первоначальную температуру Т1, если после расширения его температура Т2 = 100 К.
1.96 Найти максимально возможную температуру идеального газа в процессе, происходящем по закону: 20 V P P, где Р0 и - положительные постоянные, V – молярный объем газа. 1.97 Найти максимально возможную температуру идеального газа в процессе, происходящем по закону: V0e P P, где Р0 и - положительные постоянные, V – объем моля газа. 1.98 На рис.1.8 приведен процесс изменения состояния идеального газа. Когда газ занимал объем V1, его температура равнялась Т1. Какова будет температура газа Т2, когда он займет объем V2?
1.100 Идеальный газ совершает циклический процесс, представленный на рис.1.10. Температуры газа в состояниях 1 и 3 равны Т1 = 300 К и Т3 = 400 К соответственно. Определить температуру газа в состоянии 2.
|

 1.58 Определить давление воздуха в откачиваемом сосуде как функцию времени t. Объем сосуда V, начальное давление в сосуде Р0. Скорость откачки равна С и не зависит от давления. Процесс откачки считать изотермическим.
1.58 Определить давление воздуха в откачиваемом сосуде как функцию времени t. Объем сосуда V, начальное давление в сосуде Р0. Скорость откачки равна С и не зависит от давления. Процесс откачки считать изотермическим. 1.64 Идеальный газ, находящийся при температуре t1 = 1270С и давлении Р1 = 4·105 Па, занимает первоначально объем V1 = 2 л. Этот газ изотермически сжимают, затем изохорически охлаждают до температуры t3 = –730С и далее изотермически доводят его объем до V4 = 1л. Определить установившееся давление Р4 газа.
1.64 Идеальный газ, находящийся при температуре t1 = 1270С и давлении Р1 = 4·105 Па, занимает первоначально объем V1 = 2 л. Этот газ изотермически сжимают, затем изохорически охлаждают до температуры t3 = –730С и далее изотермически доводят его объем до V4 = 1л. Определить установившееся давление Р4 газа.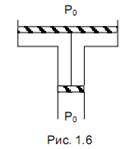 1.66 В вертикальном, открытом сверху цилиндрическом сосуде, имеющем площадь поперечного сечения S = 100 см2, под тяжелым поршнем находится m = 10 г кислорода. После увеличения температуры кислорода на ∆Т = 50 К поршень поднялся на h = 12 см. Определить массу поршня, если над поршнем давление Р0 = 105 Па. Трением поршня о стенки цилиндра пренебречь.
1.66 В вертикальном, открытом сверху цилиндрическом сосуде, имеющем площадь поперечного сечения S = 100 см2, под тяжелым поршнем находится m = 10 г кислорода. После увеличения температуры кислорода на ∆Т = 50 К поршень поднялся на h = 12 см. Определить массу поршня, если над поршнем давление Р0 = 105 Па. Трением поршня о стенки цилиндра пренебречь.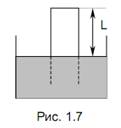 1.88 Узкая цилиндрическая вертикальная трубка длиной L, запаянная с одного конца, содержит воздух, отделенный от наружного воздуха столбиком ртути длиной h. Плотность ртути равна. Трубка расположена открытым концом вверх. Какова была первоначальная длина столбика ртути в трубке, если при перевертывании трубки открытым концом вниз из трубки вылилась половина ртути? Атмосферное давление Р0.
1.88 Узкая цилиндрическая вертикальная трубка длиной L, запаянная с одного конца, содержит воздух, отделенный от наружного воздуха столбиком ртути длиной h. Плотность ртути равна. Трубка расположена открытым концом вверх. Какова была первоначальная длина столбика ртути в трубке, если при перевертывании трубки открытым концом вниз из трубки вылилась половина ртути? Атмосферное давление Р0. 1.90 Цилиндрический стакан массой m, высотой h и сечением S плавает верх дном в жидкости плотностью. При температуре Т1 глубина погружения стакана (расстояние от поверхности жидкости до дна стакана) равна h1. До какой величины надо понизить температуру воздуха в стакане, чтобы глубина погружения стала равной h2?
1.90 Цилиндрический стакан массой m, высотой h и сечением S плавает верх дном в жидкости плотностью. При температуре Т1 глубина погружения стакана (расстояние от поверхности жидкости до дна стакана) равна h1. До какой величины надо понизить температуру воздуха в стакане, чтобы глубина погружения стала равной h2?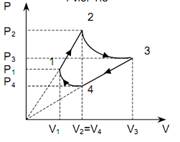 1.95 С идеальным газом происходит процесс: V=αT2. Температура газа при этом увеличилась в n = 5 раз. Определить конечное давление, если начальное давление газа равно Р1 = 105 Па.
1.95 С идеальным газом происходит процесс: V=αT2. Температура газа при этом увеличилась в n = 5 раз. Определить конечное давление, если начальное давление газа равно Р1 = 105 Па. 1.99 На Р – V диаграмме (рис.1.9) представлен циклический процесс, проведенный с идеальным газом. Участки 1-2 и 3-4 лежат на прямых, проходящих через начало координат, участки 4-1 и 2-3 – изотермы. Найти объем V3, если известны объемы V1 и V2, и известно, что объемы V2 и V4 равны.
1.99 На Р – V диаграмме (рис.1.9) представлен циклический процесс, проведенный с идеальным газом. Участки 1-2 и 3-4 лежат на прямых, проходящих через начало координат, участки 4-1 и 2-3 – изотермы. Найти объем V3, если известны объемы V1 и V2, и известно, что объемы V2 и V4 равны.


