Химические свойства. 1. Диссоциация кислот. В водном растворе карбоновые кислоты диссоциируют:
1. Диссоциация кислот. В водном растворе карбоновые кислоты диссоциируют:
Однако это равновесие диссоциации сильно сдвинуто влево, поэтому карбоновые кислоты, как правило, слабые кислоты. 2. Образование солей
3. Образование функциональных производных а) Сложные эфиры образуются при нагревании кислоты со спиртом в присутствии серной кислоты - реакция этерификации:
Б) Хлорангидриды получают действием хлорида фосфора (V) на кислоты:
г) Реакции хлорангидридов карбоновых кислот с аммиаком приводят к образованию амидов:
б)При нагревании кислот с водоотнимающими средствами получаются ангидриды карбоновых кислот R—СО—О—СО—R': 4. Окислительно-восстановительные реакции карбоновых кислот.
Вопрос 8. Гетерофункциональные соединения Соединения, имеющие в своем составе одну функциональную группу, называются монофункциональными. Соединения, имеющие несколько функциональных групп, называются полифункциональными. Полифункциональные соединения делятся на гомополифункциональные, т.е. содержащие несколько одинаковых функциональных групп, и гетерополифункциональные, т.е. содержащие несколько разных функциональных групп. Большинство биологически важных органических соединений (метаболиты, биорегуляторы, структурные элементы биополимеров, лекарственные средства) являются гетерофункциональными соединениями. Наиболее важные из них - гидрокси-, оксо- и аминокислоты, аминоспирты. Аминокислоты — это органические бифункциональные соединения, в состав которых входят карбоксильная группа —СООН и аминогруппа —NH2. Оксокислоты – гетерофункциональные соединения, содержащие карбоксильную и карбонильную (альдегидную или кетонную) группы. Аминоспиртами называют соединения, содержащие в молекуле одновременно амино- и гидроксигруппы. Гидроксикислоты – гетерофункциональные соединения, содержащие карбоксильную и гидроксильную группы. Вопрос 9. Аминокислоты, классификация Аминокислоты — это органические бифункциональные соединения, в состав которых входят карбоксильная группа —СООН и аминогруппа —NH2. В зависимости от взаимного расположения обеих функциональных групп различают ά-,β -, γ -аминокислоты и т. д.:
1). По способности человека синтезировать аминокислоты из предшественников: Незаменимые: Триптофан, Фенилаланин, Лизин, Треонин, Метионин, Лейцин, Изолейцин, Валин; Заменимые: Тирозин, Цистеин, Гистидин, Аргинин, Глицин, Аланин, Серин, Глутамин, Глутаминовая кислота, Аспарагиновая кислота, Аспарагин, Пролин Некоторые заменимые аминокислоты синтезируются в организме человека в недостаточных количествах и должны поступать с пищей (гистидин и аргинин). 2). Аминокислоты делятся на протеиногенные (20 α-аминокислот) и непротеиногенные (4 аминокислоты). 3). По функциональным группам: Алифатические моноаминомонокарбоновые: аланин, валин, глицин, изолейцин, лейцин. Оксимоноаминокарбоновые: серин, треонин. Моноаминодикарбоновые: аспарагиновая кислота, глутаминовая кислота. Амиды моноаминодикарбоновых: аспарагин, глутамин. Диаминомонокарбоновые: аргинин, гистидин, лизин. Серосодержащие: цистеин (цистин), метионин. Ароматические: фенилаланин, тирозин. Гетероциклические: триптофан, гистидин. Иминокислоты: пролин (также входит в группу гетероциклических).
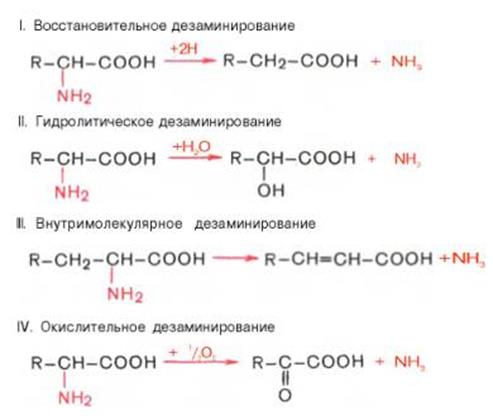
Вопрос 10. Дезаминирование, декарбоксилирование 3. Дезаминирование - это отщепление аминогруппы (—NH2) из молекулы органического соединения.
Дезаминирование играет важную роль в процессах обмена веществ, в частности в катаболизме аминокислот. Доказано существование 4 типов дезаминирования аминокислот (отщепление аминогруппы). Выделены соответствующие ферментные системы, катализирующие эти реакции, и идентифицированы продукты реакции. Во всех случаях NH2-группа аминокислоты освобождается в виде аммиака. 4. Декарбоксилирование – это процесс отщепления карбоксильной группы аминокислот в виде СО2 получил название декарбоксилирования. Несмотря на ограниченный круг аминокислот и их производных, подвергающихся декарбоксилированию в животных тканях, образующиеся продукты реакции – биогенные амины – оказывают сильное фармакологическое действие на множество физиологических функций человека и животных. Например, в животных тканях с высокой скоростью протекает декарбоксилирование гистидина под действием специфической декарбоксилазы.
Гистамин оказывает широкий спектр биологического действия. По механизму действия на кровеносные сосуды он резко отличается от других биогенных аминов, так как обладает сосудорасширяющим свойством. Большое количество гистамина образуется в области воспаления, что имеет определенный биологический смысл. Вызывая расширение сосудов в очаге воспаления, гистамин тем самым ускоряет приток лейкоцитов, способствуя активации защитных сил организма. Кроме того, гистамин участвует в секреции соляной кислоты в желудке, что широко используется в клинике при изучении секреторной деятельности желудка (гистаминовая проба). Он имеет прямое отношение к явлениям сенсибилизации и десенсибилизации. При повышенной чувствительности к гистамину в клинике используют антигистаминные препараты (санорин, димедрол и др.), оказывающие влияние на рецепторы сосудов. Гистамину приписывают также роль медиатора боли.
|


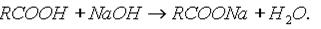

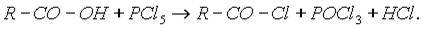


 Аминокислоты можно классифицировать по нескольким признакам:
Аминокислоты можно классифицировать по нескольким признакам: