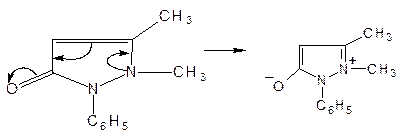Бутадион (фенилбутазон) ( Butadionum)
1,2-дифенил 4 бутил-пиразолидиндион-3,5: Сп Б, анальгетики ненарк.ряда, таб по 0,25;0,5. Произв-е пиразола применяют в качестве болеутоляющего, жаропонижающего и пр/воспол-го ср-ва. Назначают их внутрь при головных болях, невралгиях, аритмиях по 0,25-0,5г на приём. Бутадион назначают главным образом при острых формах ревматизма и полиартритов по 0,1-0,15г в настоящее время антипирин начинает успешно применяться в онкологической практике. Антипирин - бел.кр пор без запаха, слабо-горького вкуса. Оч л.р.в воде, легко –в спирте, хлф, практ не р. в эфире. Хим св-ва преп-тов этой группы опр-ся:1) ядром пиразола и 2) заместителем в 4 пол-ии. Пиразол, как и фуран, имеет ароматический характер, что связано с наличием сопряженной 6П-электронной системы, в которую входят 3е от атомов углерода и 3е от атомов азота. П/э,одно из важнейших св-в пиразола – способность к электрофильному замещению. Наличие в их стр-ре гидразиновой груп-ки, частично гидрированной системы пиразолина, а так же хар-тер заместителя при С4 обуславливает спос-ть к окислению. Итак, в соответствии с химическим строением для произ-х пиразола хар-ны след-е типы химич-го взаимодей-я: - солеобразования и комплексообр-я за счет кисл-осн-х св-в; - окисления - электрофильного замещения. - Гидролитич-го разложения. Подлинность: Общие р-ции. 1. реакции осаждения, осн-е на кислотно-основных св-вах. общеалкалоидные реактивы (как азотсодержащие соединения) реактив Люголя ---- бурый осадок перйодида антипирина. Реактив Драгендорфа ---- оранж ос-к Пикриновая к-та --- желт ос-к Кремневольфрамовая к-та --- бел ос-к 2. Антипирин (основные и нейтральные св-ва). реакции с тяж мет. Бутадион – аморфное соед-е, с преобл-ем кислотных св-в (СН-к-та), обусл-х подв-ю атома Н в С4 п и сп-тью его к енолизации. Осн-е св-ва значит-но ослаблены 2-С6Н5 радик-ми и проявл-ся только в СН3СООН лед. 3. За счет кислотных св-в, связ-х с таутомерн-ми превр-ми, бут-н вступает в реакции соле- и комплексообр-я с тяж мет. 4. Реакции окисления не проходят, т.к. антипирин пр-ки не обл. восст-ми св-ми. Бутадион тоже устойчив к окисл-ю, т.е.:а) с р-ром иода окисления нет; б) с р-ром 3% FeCl3 антипирин образует комплекс оранж-кр окр., а бутадион – бур осадок (осаждение); в) с крист. NaNO2 и к.H2 SO4 (т.е. жесткие условия) антип=изумрудно-зел окр; бутад=вишнево-кр.. кислотно-осн-е св-ва. Пр-е пиразола явл-ся слаб орг-ми основаниями. Гетероатом N в п.1 практ-ки не проявляет основных св-в, т.к.енольная пара вступает в сопряжение с П-электронами ароматического ядра, что значительно ослабляет основность. Азот в п.2 обусл-ет сл/основн св-ва и способность принимать Н+ только в неводной среде. Кисл-осн-е св-ва пр-х пиразола зависят кроме того от зам-ля в С4. Антипирин – способен обр-ть внутр-ю соль или бетаиновую стр-ру (цваттер-ион) вследствие перераспредел-я электронной плотности.
Цвиттер-ион (бетаин) Благодаря этому св-ву антипирин л.р. в воде (рН 6-7,5) и способен давать комплексную соль с FeCl3 – енолят Fe кр.цв.(ГФ10). Окраска р-ра исчезает при подкислении H2SO4р.
|