Уридилдифосфатглюкуроновая кислота ( УДФ-глюкуроновая кислота)
В лекциях «Углеводы 1, 2» изучены строение и участие глюкуроновой кислоты в обмене веществ. Вспомним: глюкуроновая кислота входит в состав гетерополисахаридов (ГАГ), которые образуют совместно с белками внеклеточный протеогликановый матрикс соединительный ткани. Глюкуроновая кислота участвует в обезвреживании(детоксикации) чужеродных соединений(ксенобиотиков), продуктов распада лекарственных препаратов и конечных метаболитов организма (билирубина). В этих соединениях глюкуроновая кислота образует β-гликозидную связь – β-глюкурониды.
Синтез глюкуроновой кислоты в условиях in vivo можно представить схемой:
+ АТФ изомеризация + УТФ Глюкоза ———> гл-6-фосфат ———> гл- 1-фосфат———>
окисление УДФ-глюкоза ———> УДФ-глюкуроновая кислота
УДФ-глюкуроновая кислота- твердое кристаллическое вещество, медленно разлагается при хранении, при Т=100 в растворе 0,01М НС1 гидролизуется в течение 15 мин. Карбоксильная группа имеет кислотные свойства в пределах других органических карбоновых кислот(рКа =4, 4)
УДФ-глюкуроновая кислота
Реакция детоксикации - глюкуронирования ксенобиотика.
УДФ-глюкуроновая кислота + R-ОН(ксенобиотик) ———>
УДФ + гликозид глюкуроновой кислоты
Никотинамиддинуклеотид(НАД +), никотинамидинуклеотидфосфат (НАДФ +) Динуклеотиды НАД +, НАДФ + были открыты в исследованиях всемирно известных биохимиков О.Г. Варбурга, Г. фон Эйлера, Ф. Шленка в 1935-1936 гг. Роль коферментов НАД +, НАДФ + в реакциях биологического окисления обсуждалась в лекции «Механизмы реакций биоорганических соединений», там же изучен механизм реакции гидридного переноса. в котором участвует активная часть этих молекул – никотинамид. Коферменты НАД +, НАДФ + состоят из двух нуклеотидов, образованных никотинамидом и аденином, связанных с рибофуранозой N-β-гликозидной связью. На атоме азота в пиридиновом цикле возникает положительный заряд, который не нарушает ароматическую систему, но увеличивает значение частичных положительных зарядов в пиридиновом цикле в положениях 2, 4, 6- по отношению к циклическому атому азота. В положении 4 пиридинового цикла происходит присоединение иона гидрида Н– Оба нуклеотида связаны посредством ангидридной связи между двумя фосфатами – эта связь имеет характер макроэргической. В организме человека известно более 150 ферментов оксидоредуктаз(дегидрогеназ)в составе которых находятся НАД +, НАДФ +. Биологические функции НАД + и НАДФ + имеют отличия: роль НАД + связана в большей степени с энергетическими процессами в клетке, а НАДФ + - с реакциями пластического обмена. Пример: Окисление молочной кислоты – фермент лактатдегидрогеназа
СН3 – СН – СООН + НАД+——> СН3 –С – СООН + НАДН + Н+ | | | ОН О
лактат пируват
На рисунках представлены: окисленная форма кофермента НАД+ и восстановленная форма кофермента НАДФН.
Сравните отличия в химическом строении пиридинового цикла окисленной и восстановленных форм, отметьте положение остатка фосфорной кислоты в НАДФН (НАДФ +)
кофермент НАД+ - окисленная форма
Сульфирует гетерополисахариды(ГАГ) в процессе образования хондроитинсульфата, дерматансульфата, активного гепарина и ксенобиотики, которые в виде сульфоэфиров фильтруются в почке и выделяются в составе мочи из организма.
Реакция детоксикации – сульфирование ксенобиотика
R-ОН(ксенобиотик) + ФАФС ——>
3’-Фосфоаденозил- 5’-фосфат + R-О- SO3 Н
|


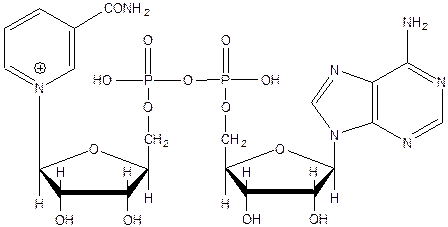
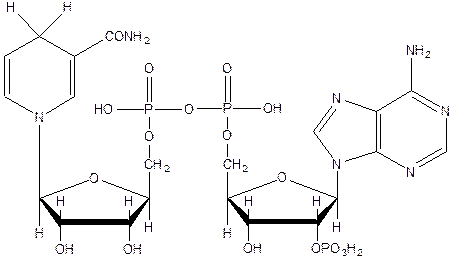 кофермент НАДФН - восстановленная форма
кофермент НАДФН - восстановленная форма
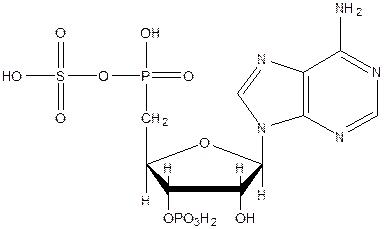 ФАФС
3’-Фосфоаденозил- 5’-фосфосульфат
ФАФС
3’-Фосфоаденозил- 5’-фосфосульфат



