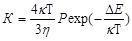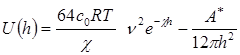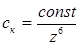Глава 7. Строение мицеллы гидрофобного золя. Коагуляция гидрофобного золя
[1] Публикация подготовлена при поддержке ГУ-ВШЭ, индивидуальный исследовательский проект №07-01-133 «Наследие Карла Шмитта и его актуальность для современной политической мысли». [2] Guenter Maschke. Kritik des Guerillero: Zur Theorie des Volkskrieges. Frankfurt a. M.: S. Fischer, 1973. [3] См. интернет-портал газеты: http://www.jungefreiheit.de/ После закрытия проекта «Критикон» газету «Юнге Фрайхайт» можно по праву называть рупором «новых правых». При этом не будет большим преувеличением сказать о том, что Карл Шмитт выступает как своего рода духовный покровитель этого издания: между 1997 и 2004 г. его имя встречается на страницах газеты более чем в 300 местах (см.: Karsten Dustin Hoffmann. Carl Schmitt in der Wochenzeitung «Junge Freiheit». GRIN Verlag, 2004), и количество посвященных ему материалов только увеличивается. [4] Перевод интервью в газете «Юнге Фрайхайт», 16 сентября 2005 г. (Junge Freiheit, Berlin, Nr. 38/05 16. September 2005) – здесь и далее примечания переводчика. [5] С. Schmitt.Frieden oder Pazifismus? Arbeiten zum Völkerrecht und zur internationalen Politik 1924 bis 1978. Hrsg., mit einem Vorwort und mit Anmerkungen versehen von Günter Maschke. Berlin: Duncker&Humblot, 2005. XXX und 1.010 Seiten. [6] Речь идет о Версальском мирном договоре 1919 г. Карл Шмитт, как и многие «консервативные революционеры», называл его не иначе как «Версальской диктатурой» или «Версальским диктатом» (см. также: С. Schmitt. Positionen und Begriffe im Kampf mit Weimar-Genf-Versailles 1923-1939. Hamburg, 1940). [7] Речь идет об используемом Шмиттом юридическом термине justa causa, войны за правое дело, характерной для жестоких религиозных войн средних веков, конец которым был положен Вестфальским миром (1648) и рождением системы jus publicum Europaeum, права континентальных европейских народов. Замена justa causa на justus hostis создало почву для гуманизации войны. Англо-американский империализм, прикрываясь новой универсалистской фразеологией, разрушил старое jus publicum Europaeum и ввел дискриминирующее понятие врага, основанное на понятии «справедливой войны». Впрочем, Шмитт не проводит четкого разграничения между понятием «справедливой войны», скажем, у Фомы Аквинского и современными формами дискриминирующей войны, которые не имеют никакой божественной легитимности. Шмитт заимствует не столько оценки, сколько язык апологетов дискриминирующей войны, которые называют ее «справедливой». Поэтому для него «справедливая война» фактически равнозначна утверждению несправедливости. [8] Пакт Келлога-Бриана (1928), Парижский пакт, об отказе от войны как орудия национальной политики; подписан 27 августа в Париже 15 государствами (Франция, США, Германия, Великобритания, Япония и др.). Назван по имени его инициаторов французского министра иностранных дел А. Бриана и государственного секретаря США Ф. Келлога. [9] Доктрина Стимсона – позиция Соединенных Штатов по поводу захвата Японией Маньчжурии в 1931-1932 г. Названа так по имени госсекретаря Соединенных Штатов Генри Стимсона в администрации Гувера, который 7 января 1932 года направил дипломатическую ноту правительствам Японии и Китая, выразив тем самым протест против действий Японии. [10] C. Schmitt. Nomos der Erde im Voelkerrecht des Jus Publicum Europaeum. Berlin, 1997. Глава 7. Строение мицеллы гидрофобного золя. Коагуляция гидрофобного золя Синтез гидрофобных дисперсных систем (суспензий, золей, в том числе аэрозолей, эмульсий) осуществляют методами диспергирования и конденсации. Диспергирование твердых и жидких веществ в выбранных средах проводят в шаровых и коллоидных мельницах вибропомола, ультразвуковых установках и др. Эффект усиливается при введение в среду ПАВ (эффект Ребиндера). Конденсационные методы основаны на физической или химической конденсации атомов или молекул с последующим образованием новой фазы в виде дисперсных частиц, распределенных в объёме среды (газообразной, жидкой или твердой). Методом физической конденсации получают золи, дымы, дисперсные металлы. При химической конденсации частицы новой фазы образуются в результате протекания в системе химической реакции с образованием малорастворимых соединений. Гидрофобные дисперсные системы термодинамически неустойчивы, так как частицы дисперсной фазы склонны к агрегации. Их термодинамическая агрегативная неустойчивость обусловлена избытком поверхностной энергии. Межфазное поверхностное натяжение в гидрофобных системах больше рассчитанного по соотношению Ребиндера-Щукина. Поэтому они не могут быть получены самопроизвольным диспергированием как лиофильныесистемы; для их образования должна быть затрачена внешняя энергия. Укрупнение частиц дисперсной фазы при потере агрегативной устойчивости достигается в результате изотермической перегонки (растворение мелких и рост крупных частиц в соответствии с уравнением Кельвина) или за счет слипания (слияния) частиц – коагуляции. Наиболее распространен процесс коагуляции. В зависимости от природы системы и концентрации дисперсной фазы этот процесс может заканчиваться или осаждением частиц, или структурообразованием. Гидрофобные дисперсные системы характеризуются кинетической агрегативной устойчивостью, определяемой скоростью процесса коагуляции. Кинетика коагуляции определяется уравнением Смолуховского:
где Константа К определяется соотношением
где Кб – константа скорости быстрой коагуляции; Р – стерический множитель, учитывающий благоприятные пространственные расположения частиц при столкновении; ΔЕ – энергия взаимодействия частиц, или потенциальный барьер; κ; - константа Больцмана; η; – вязкость дисперсионной среды. Константа скорости коагуляции К (константа скорости медленной коагуляции) является мерой кинетической агрегативной устойчивости. Если ΔЕ=0 и Р= 1, то эта константа равна константе скорости быстрой коагуляции, зависящей от вязкости среды и температуры системы. Если ΔЕ≠0 и Р≠1, то не все соударения частиц эффективны, и происходит медленная коагуляция. Замедление коагуляции, обусловленное потенциальным барьером, характеризуется фактором устойчивости, или коэффициентом стабильности:
При значительном потенциальном барьере может наступить такое состояние системы, когда скорость агрегации частиц равна скорости дезагрегации и система окажется термодинамически устойчивой к коагуляции. Таким образом, агрегативная устойчивость коллоидных систем обуславливается термодинамическими и кинетическими факторами. Термодинамические факторы, действие которых направлено на снижение поверхностного натяжения и увеличение энтропии, уменьшают вероятность эффективных соударений между частицами, создают потенциальные барьеры. Кинетические факторы снижают скорость столкновения частиц и связаны в основном с гидродинамическими свойствами системы. Различают следующие факторы устойчивости (стабилизации) дисперсных систем. 1. Электростатический фактор (термодинамический); заключается в уменьшении поверхностного натяжения вследствие возникновения двойного электрического слоя на поверхности частиц в соответствии с уравнением Липпмана. 2. Адсорбционно-сольватный фактор (термодинамический); состоит в уменьшении поверхностного натяжения в результате взаимодействия частиц с дисперсной средой (уравнение Дюпре) или благодаря адсорбции стабилизаторов (адсорбционное уравнение Гиббса). 3. Энтропийный фактор (термодинамический); проявляется в стремлении дисперсной фазы к равномерному распределению по объёму систему под действием теплового движения. 4. Структурно-механический фактор (кинетический); связан с тем, что на разрушение пленок, образующихся на поверхности частиц и обладающих упругостью и механической прочностью, требуется энергия и время. 5. Гидродинамический фактор (кинетический); заключается в снижении скорости движения частиц при изменении вязкости и плотности дисперсионной среды. 6. Смешанные факторы наиболее характерны для реальных систем; агрегативная устойчивость обеспечивается действием нескольких факторов одновременно. Каждому фактору устойчивости соответствует специфический метод его нейтрализации. Например, электростатический фактор очень чувствителен к введению электролитов. Действие структурно-механического фактора можно предотвратить с помощью веществ, разжигающих упругие структурированные слои на поверхности частиц, а также механическим, термическим способами и др. Устойчивость дисперсных систем определяется балансом энергии притяжения и энергии отталкивания между частицами. По теории ДЛФО (Дерягина, Ландау, Фервея, Овербека), учитывающей только электростатическую составляющую расклинивающего давления (давления отталкивания), энергия отталкивания убывает с расстоянием по экспоненциальному закону. Для области малых электрических потенциалов суммарная энергия взаимодействия частиц (пластин) равна
где φδ – электрический потенциал диффузного слоя; χ; – величина, обратная толщине диффузного слоя; А* - константа Гамакера; h – расстояние между частицами (пластинами); ε; – диэлектрическая проницаемость дисперсной среды; ε0 – электрическая постоянная. При больших потенциалах и расстояниях между частицами (пластинами) эта энергия определяется уравнением
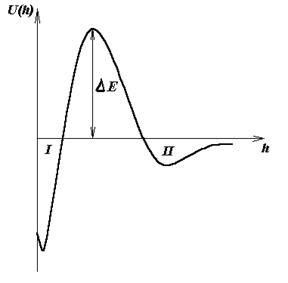
Суммарная потенциальная энергия взаимодействия частиц отрицательна на близких и далеких расстояниях (преобладает энергия притяжения). Она может быть положительна на средних расстояниях (преобладает энергия отталкивания). Максимум потенциальной кривой (рис 1.) отвечает потенциальному барьеру ΔЕ. Первый минимум I соответствует непосредственному соприкосновению частиц, а второй II – притяжению частиц, между которыми имеются прослойки среды. Коагуляция гидрофобныхдисперсных систем может происходить в результате различных внешних воздействий, например при механическом воздействий (ультразвука), действии электрического поля, при нагревании или замораживании системы. Коагуляция гидрофобных золей может быть вызвана также их сильным разбавлением или концентрированием. Наиболее часто коагуляция дисперсных систем происходит при добавлении электролитов. Различают два типа электролитной коагуляции коллоидных систем: 1) нейтрализационную, происходящую в результате снижения поверхностного потенциала частиц; 2) концентрационную, протекающую вследствие сжатия диффузной части двойного электрического слоя (потенциал поверхности в этом случае не изменяется). Нейтрализационная электролитическая коагуляция характерна для коллоидных систем, содержащих слабо заряженные частицы. Концентрационная коагуляция обычно наблюдается в сильно заряженных дисперсных системах.
Рис.1. Зависимость энергии взаимодействия U двух частиц от расстояния между ними h. . Введение электролитов снижает высоту потенциального барьера, но при небольших концентрациях электролита энергетический барьер остается достаточно велик и коагуляция не происходит. Агрегация наступает при введении определенного для данной системы количества электролита, соответствующего порогу коагуляции. Порок быстрой коагуляции ск определяет количество электролита, необходимое для коагуляции единицы объёма коллоидной системы при полном исчезновении потенциального барьера ΔЕ. При сохранении небольшого потенциального барьера в системе протекает медленная коагуляция. При электролитной коагуляции по концентрационному механизму (для сильно заряженных частиц) порок коагуляции ск в соответствии с правилом Дерягина-Ландау (обоснование эмпирического правила Шульца-Гарди) обратно пропорционален заряду z противоионов в шестой степени, т. е.
При нейтрализационной коагуляции (при малых потенциалах поверхности φ0 частиц) показатель степени z в уравнении уменьшается до двух (правило Эйлерса-Корфа). Строение коллоидной мицеллы схематически может быть изображено на примере мицеллы иодида серебра: {[(AgI)n mI-] xK+} (m-x)K+
ядро
частица
мицелла
|

 или
или 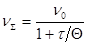
 - суммарное число частиц дисперсной фазы ко времени τ;;
- суммарное число частиц дисперсной фазы ко времени τ;;  - первоначальное число частиц;
- первоначальное число частиц; 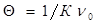 - время половинной коагуляции; К – константа скорости коагуляции.
- время половинной коагуляции; К – константа скорости коагуляции.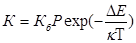 или
или