Для газа данной массы умножения давления газа на его объем постоянно, если температура газа не меняется.
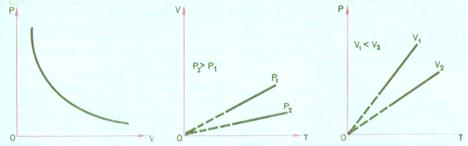
Этот закон экспериментально был открыт английским ученым Р. Бойлем (1627-1691) и несколько позже французским ученым Е. Мариоттом (1620-1684). Поэтому он и носит название закона Бойля-Мариотта. Зависимость давления газа от объема при постоянной температуре графически изображается кривой, которая называется изотермой. Изотерма газа изображает обратно пропорциональную зависимость между давлением и объемом. Кривую такого рода в математике называют гиперболой (рисунок 1, а).
Рисунок 1. а б в
3 Процесс изменения состояния термодинамической системы при постоянном давлении называют изобарным (от греческого слова «барос» – вес (тяжесть)). Соответственно уравнению в любом состоянии газа с давлением, которое не меняется, отношение объема газа к его температуре остается постоянным: Для газа данной массы отношение объема к температуре постоянно, если давление газа не меняется. Этот закон был осуществлен экспериментально в 1802 г. французским ученым Ж. Гей-Люссаком (1778-1850), и носит название закон Гей-Люссака. Согласно уравнению объем газа линейно зависит от температуры при постоянном давлении: V = const*T. Эта зависимость графически изображается прямой, которую называют изобарой (рисунок 26, б).
Процесс изменения состояния термодинамической системы при постоянном объеме называют изохорным (от греческого слова «хорема» – емкость). Из уравнения состояния вытекает, что в любом состоянии газа с неизменным объемом отношение давления газа к его температуре остается постоянным: р/Т = const при V= const
|

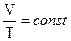 при р = const.
при р = const.


