Руди титану
По розповсюдженню в земній корі титан займає десяте місце серед інших хімічних елементів (0, 61 % по масі). Відомо більше 60 мінералів титану, із яких найбільше розповсюдження мають ільменіт, рутил, перовскіт і сфен. Ільменіт FeO TiO2 вперше був знайдений в Ільменітських горах на Уралі, звідки і отримав назву. Це блискучий мінерал буро –горного кольору. Важливим джерелом ільменіта являється титано- магнетитові залізні руди, в яких міститься двоокисі титану до 20%. Титано-магнезитові руди можна збагачувати гравітаційним і магнітним методами. В результаті вдається отримувати концентрат, який містить більше 40% TiO2, біля 50% окислів заліза, біля 8% окислів алюмінію, кремнію, магнію, кальцію. Рутил Ti O2 прозорий, має алмазно-металевий блиск, буває окрашений в різні кольори (червоно-коричневий, жовтий, синій, чорний). Великі родовища рутилу зустрічаються рідко. Перовскіт CaOхTiO2 містить більше 58% рутилу. Збагачення здійснюється гравітаційним і флотаційним методами, які дають можливість отримати концентрат з вмістом до 47% рутилу TiO2. Сфен (титаніт) CaOxTiO2xSiO2 зустрічається в природі разом з іншими корисними мінералами. Може бути перспективною сировиною в майбутньому при умові комплексної переробки. 3. Технологія виробництва титану. Відомо декілька способів отримання титану із його руд. Вибір способу металургійної переробки залежить від вимог і призначення кінцевого продукту, а також типу вихідної сировини і характеру домішок. Технологічний процес виробництва титану складається із таких стадій (операцій):
1. збагачення руди; 2. плавленя збагаченої руди в руднотермічній печі з метою отримання шлаку, який містить 65 – 85 % ТіО2 ;
2FeOxTiO2 + C = 2TiO2 +Fe +CO2
3. отримання концентрату чотирихлористого титану (TiCl 4) при температурі 900 оС та подальшому хлоруванні брикетів при 800 – 850 оС; порошкоподібний шлак з ТіО2 брекетують і загружають в електропіч де проходить реакція
ТіО2 + С + 2С = ТіС 4 + СО2 + Після отримання хлоридів Ті і інших складових здійснюється складна очистка і отримують чистий чотирьоххлористий титан; 4. відновлення титану з тетрахлориду магній -термічним способом в спеціальних реакторах (Рис.3). При цьому отримують губчату масу, яка містить 65 – 55 % Ti, 25 – 30%Mg, 10 – 15 % MgCl. В реакторі має місце наступна реакція:
ТіС + 2М = М С + Ті +О
Реторту охолоджують і виймають із печі. Титанову губку вибивають із реторти і сортують Отриману губку з титану переплавляють у дугових печах.
5. Чистий титан отримують іодідним способом:
Ті + 2І2 Ті І2 При температурі 200 оС реакція протікає зліва направо, а при 1300 – 1400 оС реакція протікає справа наліво. Цим способом отримують Ті високої чистоти. Рафінування титану здійснюють також шляхом вакуумної сепарації при температурі 900 – 950 оС, тиску 10-3 мм рт. Ст. Технічний титан містить не більше 1% домішок. Згідно з ГОСТ титан випускається таких марок: ТГ0(99, 65 Ті), ТГ1 (99, 21% Ті), ТГ2 (99, 18%Ті). Найбільший виробник по виробництву Ті і Mg є титано-магнієвий комбінат в Запоріжжі.
4. Титанові сплави. Для підвищення механічних властивостей титану його легують алюмінієм, який підвищує температуру алотропічного перетворення титана (альфа гратки в бета). Алюміній часто називають альфа-стабілізатором титану. Елементи, які стабілізують бета-фазу (молібден, ванадій, хром, марганець, залізо і ін.) називають бета-стабілізаторами. В промисловості застосовують титанові сплави із структурою альфа-твердого розчину, або змішаної структури (альфа + бета) твердого розчину. Алюміній, утворюючи з титаном твердий розчин, збільшує міцність, жароміцність і опір окисленню при високій температурі. Тому алюміній являється важливою складовою титанових сплавів і завжди входить до складу титанових сплавів. Для отримання сплавів змішаної структури титан, крім алюмінію, легують додатково хромом, марганцем, молібденом, а інколи і іншими бета-стабілізаторами. Двохфазні сплави титану мають майже подвоєну міцність порівняно з чистим титаном., однако підвищена міцність зберігається до температури 430 оС. Більшість цих сплавів мають хорошу пластичність і тому легше куються, штампуються і прокатуються, чим однофазні титанові сплави. Зварка цих сплавів утруднена, а шви отримують хрупкість. Однофазні бета титанові сплави майже не застосовуються. Вони дуже чутливі до забруднення атмосфери.
Лекція 7.Технологія виготовлення виробів із порошків. План 1.Порошковаметалургія та застосування ії продукції 2.Способи виготовлення порошків і їх властивості. 3.Формування виробів із порошків. Література. Збожна О.М. Основі технології. Навчальний посібник. 2-е видання 2002 рік. 1.Порошкова металургія та застосування її продукції. Порошкова металургія займається виробництвом порошків і виробів з них. Порошкової металургії отримують пів; конструкційні матеріали, які називаються металокерамікою - вироби із порошків спіканням(нагрівання) Свій початок історія порошкової металургії розпочалась у Стародавньому Єгипті, а пізніше в Київській Русі, це виготовляли різні вироби із заліза і кольорових металів (міді., платини)Проте промислове виробництво із порошків розпочалось в 19 ст. Технологія виробництва продукції із порошків дозволяє отримувати деталі машин та інструмент без оброблення різанням або з найменшим припуском. Порошкова металургія являється маловідходною або безвідходною технологією виготовлення різних виробів. Як і в технології виготовлення відливок порошкова металургія майже не потребує спеціальних верстатів для механічної обробки. Відходи при виготовленні деталей різанням із заготівок, отриманих методом розкатки, пресуванням становлять до 20-80 відсотків, а в процесі виготовлення порошковою металургією - всього 5-10.При цьому незначні затрати праці, а кількість технологічних операцій скорочується з 20-40 до 4-6. За допомогою порошкової металургії можна отримувати матеріали та вироби з наперед заданими властивостями -високою зносостійкістю, твердістю, стабільними магнітними та іншими властивостями. За допомогою порошкової металургії можна отримувати такі штучні матеріали та вироби з них, які не можна виготовляти іншим способом.Деталі, виготовленні із порошків містять пори, в яких може знаходитись змазка. Значить підшипники ковзання будуть довговічні так як тертя в них менше. Собівартість порошкових виробів менша порівняно з собівартістю виробів, отриманих литтям або різанням. У процесі виготовлення 1 тис. тонн деталей економиться понад 200 т. сталі, вивільняється 200 робітників і 50 металорізальних верстатів. Основна маса продукції порошкової металургії (60-70 відсотків)використовується в автомобілебудуванні. Порошкова металургія забезпечує машинобудівну промисловість конструкційними, фрикційними й антифрикційними матеріалами; електротехнічну й електронну - магнітами, катодами резисторами.; інструментальну та добувну - твердими та надтвердими сплавами; авіаційну та космічну, атомну енергетику - жаростійкими та міцними матеріалами; хімічну та металургійну промисловість - хімічно та термостійкими матеріалами, каталізаторами вогнетривами; дитячі іграшки – моделі 2.1Способи виготовлення порошків Порошки виробляють механічним та фізико-хімічним способами.це поділ умовний. Механічні способи: подрібнення, розселення, розсиплення. Хімічний склад таких порошків залишається незмінним. Фізико хімічні способи: відновлення з оксидів; дисоціація9розклад0 При цьому хімічний склад порошків значно відрізняється від складу сировини. Приклад: FеО + СО =Fе + О2 Fе2Оз+ СО = 2Fе0+202 Комбінований спосіб: 1)Розпилення рідкого металу, а потім відпалюють у середовищі водню. 2)Електроліз. а потім розпилювання 3)Відновлення з оксидів і розпилення. Спосіб отримання порошку впливає на форму та розмір частинок, його властивості та вартість Властивості Порошки отримані різним способом відрізняються розмірами та формою частинок, їх здатністю до спікання і пресування, а також призначення отриманої деталі 2.2 Властивості порошків Порошки характеризуються фізичними, хімічними та технологічними властивостями.ці властивості регламентуються стандартами та технічними умовами.До технологічних властивостей відносяться: насипна маса, здатність формуватись і пресуватись, плинність. Розмір порошків складає від 0, 1 до 110 мкн. Насипна маса — маса одиниці об’єму вільно насипаного порошку(кг/мЗ) Чим більші за розміром частинки і точніша їх форма, тим більше насипна маса порошку Плинність — це швидкість проходження порошку через отвір певного діаметру. Плинність впливає на рівномірність заповнення прес-форми порошком і швидкість ущільнення в ході пресування.чим менший розмір частинок, тим менша плинність. Здатність пресуватись - це здатність ущільнюватись і набувати форми під дією зовнішніх сил. Здатність формуватись - це здатність виробу зберігати свою форму після ущільнення за мінімального тиску. Усі ці властивості впливають на кінцевий результат порошкової металургії, яким є виріб. Порошки мають високу активність з киснем. Окиснення супроводжується нагріванням в результаті чого на повітрі можуть загоратись: метал горить!
3. Формування виробів з порошків
3.1 підготовка шихти до пресування виробів.
Однорідні (чисті) порошки не використовуються для виготовлення виробів. Використовується шихта - суміш порошків і спеціальних речовин (каучук, парафін, графіт, метал і спл.). Підготовляння шихти - важлива операція технологічного процесу. У процесі технології виробництва порошків на поверхню потрапляють молекули води, мастил, утворюються оксидні плівки. Навіть малий вміст на поверхні порошків цих речовин негативно впливає на властивості готових виробів. Питома поверхня порошків велика (м 2 /г)
Оксиди погіршують пресування та спікання. Водень, азот, оксид вуглецю збільшують крихкість. Чим дрібніші порошки, тим вони більше забруднені. Щоб запобігти забрудненню порошків, їх зберігають у щільно закритих контейнерах, заповнених інертним газом. Це дорого. Тому перед використанням порошків, їх очищують: відпалюютьу відповідній атмосфері. Це підвищує технологічні властивості порошків. Для полегшення формування та спікання до порошків додають спеціальні речовини. При виготовленні твердих сплавів додають розчин каучуку в бензині або парафіні, до порошків із сталі - веретенне мастило або олеїнову кислоту. У процесі виготовлення антифрикційних деталей до шихти додають графіт, дляфільтрів — карбонат алюмінію. Перемішують суміші у змішувачах. 3.2 Способи Формування виробів. Найбільш поширенні способи формування виробів є: 2.холодне та гаряче пресування; 3. вальцювання; 4.шлікерне лиття (у разові форми) Пресування. Вироби пресують у пресформах. Зусилля прикладають з одного або двох чи більше боків. Однобічне пресування застосовують для виготовлення виробів простої форми (втулки, кільця) Внутрішню поверхню змащують для отримання більш однорідної густини по діаметру і висоті виробу.
Вальцювання. Це економічно вигідний спосіб. Вироби виготовляють безперервним формуванням, а потім спікають. Цим способом отримують стрічку та прутки. Вальцювання можна здійснювати у вертикальному та горизонтальному напрямках. Вертикальне вальцювання дозволяє отримати біметал.
Рис. 1. Схема способів вальцювання порошків: 1-бункер; 2-порошок; 3- валки; 4 стрічка (готовий лист)
Шлікерне лиття. Шлікером називають суспензію, яку заливають у гіпсову або керамічну форму. Рідина із шлікера виходить крізь пори у формі, а в середині форми утворюється виріб. Підсушений виріб виймають із форми, для чого форму руйнують. Після висушування виріб спікають. 3.3 Спікання і обробка (викінчення) порошкових виробів. Вироби, отримані з порошків, мають малу міцність. Для того, щоб надати виробам великої міцності, їх спікають. Спікання називають відпалення виробів при температурі, яка становить 0, 7-0, 8 температури плавлення основної складової шихти. Час спікання становить 1-2 години. Під час спікання у виробах відбуваються складні фізико-хімічні процеси (відновлення оксидів, дифузія, рекристалізація, зняття залишкових напруг), поліпшуються механічні властивості.
а) однобічне; б) двобічне
Рис. Схема пресування порошків: 1 – пуансон; 2 – порошок; 3 – пресформа
При двобічному пресуванні пуансони рухаються назустріч один одному. Виріб отримується більш однорідним по густині порівняно з однобічним пресуванням. М ундштукове пресування. Застосовують при виготовленні виробів, довжина яких значно перевищує діаметр (прутки, труби тощо).Ці вироби виготовляють з порошків, які важко пресуються (берилію, вольфраму тощо) Щоб підвищити густину 9 однорідність) матеріалу виробу, використовуютьвібрацію, яка до порошку передається через контейнер або пуансон. За допомогою вібрації.можна в кілька разів зменшити зусилля на пуансон.
Рис. Схема мундштукового пресування порошків 1-пуансон, 2-порошок, 3-пресформа, 4-матриця Механізм деформації і спікання пдшорошків:
У масовому виробництві використовують печі безперервної дії. Спікання здійснюють в спеціальних атмосфера: водню, аміаку, інертному газі, вакуумі.)
Лекція 8. Хіміко-технологічні процеси у виробництві непродо-вольчих товарів 1. Значення, історія хімічних виробництв та структура хімічної промисловості. 2. Поняття про хіміко-технологічні процеси, їх апаратурне оформлення та параметри роботи. 3. Основні типи хімічних реакторів. 4. Поняття про матеріальний і енергетичний баланс виробництва та їх роль у економічних і технологічних розрахунках. 5. Узагальнена типова схема ХТП. 6. Загальні принципи інтенсифікації хімічних процесів, основні напрями їх вдосконалення і розвитку. Література. Желібо С.П., Анопко Д.В., Буслик В.М. і ін. Основи технологій виробництва в галузях народного господарства: Навчальний посібник. – К.: Кондор, 2005. – 716 с.
1. Значення, історія і структура хімічної промисловості Хімічна промисловість відноситься до міжгалузевих виробництв. Ця промисловість впливає на інші масштабні галузі народного господарства: гірничо-добувну, енергетику, металургію, нафтопереробну, агропромис-ловий комплекс, харчову, легку, фармацевтичну. Хімічна технологія – наука про найбільш економічно та екологічно обґрунтовані методи переробки сировини у засоби виробництва і предмети споживання. Хімічна технологія вивчає і розробляє фізико-хімічні процеси, технологічне обладнання, оптимізацію здійснення і управління цими процесами при виробництві різних речовин, продуктів, матеріалів і виробів. Підприємства хімічної промисловості України виробляють понад 130 тисяч різних хімічних продуктів і належать до найважливіших ланок продуктивних сил. Хімічна промисловість забезпечує інші галузі напівпродуктами (кокс, мазут, збагачені руди і таке ін.) Хімічні підприємства виробляють продукцію, що замінює метали, дерево, скло, шкіру. Різноманітність продукції хімічної промисловості пояснюється тим, що хімічні технології дають можливість отримати із одної сировини кілька різних продуктів, або навпаки, певний продукт – із різних видів сировини. В результаті переробки на хімічних заводах нафти, газу і вугілля, із них отримують бензин і мастила для двигунів, вибухові речовини, кокс, пластмаси, гуми і синтетичні каучуки, хімічні волокна і барвники, добрива і засоби захисту рослин, фармакологічні препарати, парфумерію, синтетичні миючі засоби, тару і художньо-декоративні вироби, лаки і фарби, клеї, будівельні матеріали та інші продукти. Хімічна промисловість матеріало- та енергомістка. Вона використовує різноманітну природну сировину: мінеральні і органічні корисні копалини, компоненти флори і фауни, промислові відходи, природні води і повітря. Для функціонування і розвитку хімічної промисловості Україна має достатню сировинну базу: вугілля, нафту і газ, калійні солі, кам’яну сіль, сірку, графіт, гіпс, вапняки і доломіти, глини і каоліни, природні води. Згідно із прийнятою класифікацією продукцію хімічної промисловості поділяють на 7 класів: - продукція неорганічної хімії і гірничо-хімічна сировина; - полімери – синтетичні каучуки, пластмаси і хімічні волокна; - лакофарбні матеріали і продукти; - синтетичні барвники й органічні напівпродукти; - продукти органічного синтезу (нафто-, коксо- та лісохімія); - хімічні реактиви і особливо чисті речовини; - медикаменти і хіміко-формацевтична продукція.
Історія хімічних виробництв. Історія хімічної промисловості розвивалась одночасно з накопиченням наукових знань хімії та розробкою хімічних технологій. Хімічна промисловість спочатку розвивалась для забезпечення лікарських та військових потреб. Витоки хімічних технологій сягають сивої давнини і стосуються, переважно, виробництва ліків та пороху (1250 р.). Накопичені алхіміками практичні знання по хімії поклали початок примітивним хімічним виробництвам. Початок промислового виробництва хімічних продуктів у Європі відноситься до XV ст., коли з’явились дрібні спеціалізовані виробництва кислот, солей, фармпрепаратів та деяких органічних речовин. В XVI – XVII ст. Росія мала власні хімічні виробництва фарб, селітри, пороху, соди, сірчаної кислоти. Лише у другій половині XVIII ст. було закладено основи хімтехнології як науки і навчальної дисципліни. У 1772 році І. Бекман вперше ввів термін «технологія» і описав детально технологію багатьох хімічних виробництв, створивши перший підручник по хімтехнології. Хімтехнологія лише в кінці XVIII ст. стала обов’язковою навчальною дисципліною в університетах і технічних вузах Європи та училищах комерційного і технічного профілю в Росії, де у 1803 році було створену першу кафедру хімічної технології. Поява у XIX ст. у Західній Європі великої кількості підручників та наукових досліджень з технології сприяло як швидкому росту і поширенню хімічних виробництв, так і розвитку науки про хімтехнології. Фундаментальні досягнення фізики, електротехніки та електрохімії у XIX ст. дали змогу у широких масштабах практично реалізувати електрохімічні методи виробництва багатьох важливих продуктів: лужних металів, алюмінію, хлору, фтору, водню, лугів та інше. Бурхливий розвиток органічної хімії та методів органічного синтезу у XIX та XX ст. заклав основи багатьох промислових технологій виробництва широкого спектру органічних речовин: барвників, харчових продуктів, фармпрепаратів, засобів захисту рослин, інсектицидів. Основними тенденціями сучасного розвитку хімічної промисловості є перехід до автоматизованих, безвідходних енергозберігаючих виробництв з широким використанням біотехнологічних процесів. Сучасні хімічні технології спрямовані, насамперед, на розв’язання глобальних проблем людства: збереження і поповнення продовольчих запасів шляхом переробки нехарчової сировини, енергозбереження і попередження забруднення біосфери. До провідних напрямків розвитку хімічних технологій належать: створення нових видів хімічної продукції багатоцільового призначення (водню, аміаку, метанолу), поглиблення комплексної переробки мінеральної сировини, нафти і газу, а також створення нових хімічних джерел струму та систем перетворення енергії.
2. Поняття про хіміко-технологічні процеси, їх схематичне оформлення та параметри роботи. Виробничі процеси в різних галузях хімічної промисловості характери-зуються великою складністю фізичних, механічних, електричних, високотемпературних та інших процесів і багатоетапністю, але виробничий процес прийнято називати хіміко-технологічним процесом так як хімічні реакції є серцевиною виробництва. Хіміко-технологічний процес (ХТП) – сукупність взаємопов’язаних фізичних та хімічних операцій, реалізація яких у певній послідовності дозволяє із вихідної сировини чи напівпродуктів отримати цільовий продукт. ХТП крім підготовки сировинних компонентів (матеріалів) та збагачення і очищення цільових продуктів включає три стадії: 1) подачу реагуючих компонентів у зону реакції; 2) хімічні реакції; 3) відведення із зони реакції отриманих продуктів. Стадія подачі компонентів повинна забезпечити їх надходження у необхідних співвідношеннях та максимально можливу гомогенізацію їх суміші шляхом механічного перемішування та інших процесів (плавлення та розчинення, возгонки – конденсації, адсорбції – десорбції). Як правило, в системі протікає кілька послідовних чи паралельних реакції з утворенням цільового чи побічного продукту, але при аналізі виробничих процесів враховують, як правило, лише ті реакції, які мають визначальний вплив на вихід та якість цільових продуктів. Сумарна швидкість ХТП лімітується найповільнішою їх стадією. Процес характеризується кінетичною (швидкістю реакції) та дифузійною областями (швидкістю подачі компонентів). Для більшості ХТП основними параметрами є: температура, тиск, каталізатор і його активність, концентрації взаємодіючих речовин і їх вид (тверді, рідкі), спосіб і параметри змішування компонентів, рівень кислотності. Оптимізація технологічних параметрів забезпечує максимальну продуктивність праці і найкращі економічні показники. Характер і величина параметрів технологічного процесу покладено в основу класифікації ХТП. Найпростішою є класифікація ХТП за наступними критеріями: а) видом вихідної сировини; a. типом основної хімічної реакції; b. способом організації процесу; c. кратністю обробки сировини. За видом вихідної сировини ХТП поділяють на процеси по переробці мінеральної, рослинної і тваринної сировини. За типом основної хімічної реакції ХТП поділяють на процеси, які ґрунтуються на: - простих і складних реакціях; - оборотних і необоротних реакціях; - гомогенних і гетерогенних реакціях; - каталітичних реакціях; - ендотермічних і екзотермічних реакціях; - електрохімічних реакціях; - фотохімічних реакціях; - радіаційно-хімічних реакціях. Прості реакції є одно стадійними, а складні – багатостадійними. Гомогенні і гетерогенні реакції протікають між речовинами, що знаходяться в одній чи різних фазах відповідно. За способом організації процесу ХТП можуть бути періодичними, безперервними і комбінованими. У періодичних процесах сировину вводять в реактор окремими порціями, а після завершення циклу також дискретно виводять цільовий продукт. У безперервних процесах сировину вводять в реактор постійним потоком. Після її перетворення в цільовий продукт, останній також безперервно виводять з реактора. Комбіновані процеси можуть характеризуватись різними комбінаціями безперервності та дискретності введення сировини і виведення продукту: періодичним введенням сировини та безперервним виведенням продукту; безперервним введенням сировини та періодичним виведенням продукту; періодичним введенням одного компонента, безперервним – другого при безперервному виведенні продукту. За кратністю обробки сировини ХТП поділяють на процеси з розімкнутою (відкритою), замкнутою (закритою) і комбінованою схемами. В процесах з відкритою схемою сировина за один цикл перебування в реакторі перетворюється на цільовий продукт. В процесах із закритою схемою через недостатній ступінь перетворення на цільовий продукт для досягнення прийнятної повноти реакції необхідне багаторазове повернення відокремленої від продукту сировини, що не прореагувала, подавати знову на вхід реактора. 3. Основні типи хімічних реакторів. Хімічні перетворення здійснюють у реакторах, конструкція яких розрахована на проведення процесів певного типу при параметрах, близьких до оптимальних. Хімічний реактор – технологічний апарат, в якому здійснюють хіміко-технологічні процеси, що поєднують хімічні реакції з масопереносом (дифузією). В реакторах здійснюються складні хімічні і фізичні процеси, тому вони повинні відповідати певним вимогам: - забезпечувати найбільшу продуктивність; - бути простими за конструкцією і недорогими; - найповніше використовувати тепло; - бути надійними в роботі при повній механізації та автоматичному регулюванні процесів. Реактори відрізняються як конструктивно, так і за режимами роботи.
Класифікація хімічних реакторів здійснюється за такими критеріями: 1) конструктивними особливостями (циліндри, тарільчатого типу, шахтні, обертові); 2) умовами теплообміну в реакторі (ізотермічні, адіабатичні, автотермічні); 3) фазовим складом реагуючої суміші (рідинно-твердофазні, газотвердофазні, газорідинні, газові); 4) способом організації процесу (періодичні, безперервної дії). 4. Поняття про матеріальний і енергетичний баланс виробництва та їх роль у економічних і технологічних розрахунках. Удосконалення технологічних процесів можливе лише на основі їхнього глибокого і всебічного техніко-економічного аналізу. Останній відображає всі поетапні затрати виробництва, що визначають собівартість продукції – один із найважливіших показників. Технологічний баланс, що зіставляє матеріальні та енергетичні затрати з фактичним випуском продукції, характеризує економічну ефективність виробництва. Основна роль технологічного балансу полягає в тому, що собівартість продукції повинна бути врівноважена з її ціною та ринковим попитом на неї, забезпечуючи при цьому рентабельність виробництва. Технологічний баланс – це зведена інформація у вигляді діаграм, таблиць чи рівнянь про надходження та витрати, результати зіставлення введених та отриманих у виробничому процесі матеріалів та енергії. Складовими технологічного балансу є матеріальний та енергетичний баланси, ґрунтовані на законах збереження матерії та енергії відповідно. Матеріальний баланс (МБ) – це застосований для конкретного процесу чи реакції закон збереження маси речовини, згідно з яким у замкнутій системі маса речовин, що вступають у взаємодію, дорівнює масі речовин, що утворились внаслідок цієї взаємодії. Рівняння матеріального балансу має вигляд:
mА + mБ + mС = mR + ms, (1) де mА, mБ, mС - вхідні речовини; mR, ms – відповідно цільовий і побічний продукти. Матеріальний баланс найчастіше складають на одиницю маси продукту, тобто розраховують, які маси вихідних речовин необхідні для отримання одиниць маси цільового продукту mR, а також скільки при цьому отримують побічного продукту ms. Із рівняння (1) отримаєм масу цільового продукту: mR = mА + mБ + mС - ms. (2)
Якщо вихідним матеріалом є одна речовина, то рівняння (2) буде мати вид: mR = mА - ms Найзручніше маси речовин на вході та виході системи визначати окремо для твердої, рідкої та газjподібної фази, а матеріальний баланс розраховувати за формулою: mt + mp + mг = mt’ + mp’ + mг’ , де mt, mp та mг – відповідно маси твердих, рідких, та газоподібних речовин на вході системи, а mt’, mp’ та mг’ - маси відповідних речовин на на виході. Для випадку неповноти реакції МБ розраховують за формулою: mА + mБ = mc + mд + mАА + mАВ + … + mЕ + mF + mT, (3) де mА і mБ – маси вхідних речовин; mc і mд – маси основних продуктів взаємодії; mАА і mАВ – маси залишків вихідних речовин, що не прореагували; mЕ і mF – маси побічних продуктів реакції; mT – маса відходів. Для розрахунку МБ необхідно знати хімсклад і деякі властивості сировинних компонентів, основних і побічних продуктів та відходів, а також хімічні рівняння основних перетворень у системі. Отримані на основі розрахунків результати зводять у таблицю із двох частин: доходної і розхідної, що полегшує аналіз даних і практичного їх використання. Енергетичний баланс (ЕБ) – це застосований для конкретного процесу чи реакції закон збереження енергії, згідно з яким кількість енергії (теплоти), внесеної в зону взаємодії речовин, дорівнює кількості енергії (теплоти), винесеної з цієї зони. Рівняння енергетичного балансу (ЕБ) можна записати в такому вигляді: QФР + QМФН + QTH = Q’ФР + Q’ BT, (4) де QФР – фізична теплота, введена в процес з вхідними речовинами; QМФН – теплота міжфазних переходів-розчинення, каналізації, випаровування, конденсації, плавлення; QTH - теплота, введена з теплоносіями – водою, газами, паливом; Q’ФР – фізична теплота виведена із процесу з продуктами реакції; Q’ BT – втрати теплоти в навколишнє середовище. Складові енергетичного балансу розраховуються на основі фізичних і термохімічних даних. Наприклад, введену з вхідними речовинами теплоту розраховують за формулою QФР = m х с х t, де m, c і t – маса, теплоємність і температура речовини відповідно. При неможливості розрахунків за термохімічними формулами Q’ BT визначають як різницю між сумами енергій на воді і виході системи. На основі розрахунків матеріального і енергетичного балансів розраховують витрати і втрати сировини, палива та інших матеріалів, фактичний вихід продукції, коефіцієнти використання енергії, приймають організаційні та технічні рішення по оптимізації параметрів роботи обладнання, максимальному використанню матеріальних і енергетичних ресурсів. Аналіз даних технологічних балансів широко використовують для вдосконалення роботи діючих і проектування нових підприємств.
|

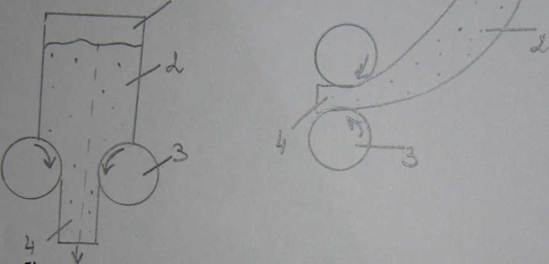




 Загальна схема технології виготовлення виробів із порошків: порошок; К1 - К.3 - спеціальні речовини; 1-змішування; 2- формування виробів; 3- спікання; 4-калібрування; 5- різання(доводка, свердління); 6- термічна та хіміко-термічна обробка;
Загальна схема технології виготовлення виробів із порошків: порошок; К1 - К.3 - спеціальні речовини; 1-змішування; 2- формування виробів; 3- спікання; 4-калібрування; 5- різання(доводка, свердління); 6- термічна та хіміко-термічна обробка;




