Важнейшее свойство аминокислот — их способность к конденсации с образованием пептидов
Дипептид имеет свободные –NH2 и –COOH группы и может взаимодействовать еще с одной молекулой аминогруппы, образуя трипептид, затем еще с одной молекулой – тетрапептид и т.д. При соединении друг с другом большого числа аминокислот образуются полипептиды.
Полипептидная цепь – основа белковых молекул, белки – это природные полипептиды.
ХИМИЧЕСКИЕ СВОЙСТВА АМИНОКИСЛОТ
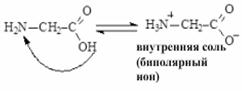
И в растворе и в кристаллическом состоянии аминокислоты могут существовать в виде внутренних солей (биполярных ионов), которые образуются за счет того, что карбоксильная группа отдает протон, а аминогруппа его присоединяет:
1 Аминокислоты могут реагировать со спиртами в присутствии газообразного хлороводорода, превращаясь в сложный эфир (точнее, в хлороводородную соль эфира):
Реакция этерификации – реакция между спиртом и кислотой с выделением воды и образованием сложного эфира. Сложные эфиры аминокислот не имеют биполярной структуры и являются летучими соединениями. Эта реакция имеет внешнюю аналогию с реакцией нейтрализации кислоты щелочью, хотя сложные эфиры по свойствам нисколько не напоминают соли.
|

 Аминогруппа одной аминокислоты может взаимодействовать с карбоксильной группой второй, образуя пептиды (соединения, состоящие из остатков аминокислот, связанных пептидной связью):
Аминогруппа одной аминокислоты может взаимодействовать с карбоксильной группой второй, образуя пептиды (соединения, состоящие из остатков аминокислот, связанных пептидной связью):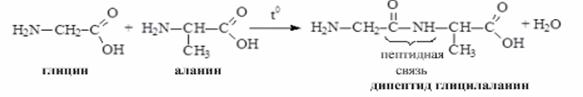

 Аминокислоты – амфотерные соединения, они могут проявлять как кислотные свойства, обусловленные наличием в их молекулах карбоксильной группы –СООН, так и основные свойства, обусловленные аминогруппой – NH2.
Аминокислоты – амфотерные соединения, они могут проявлять как кислотные свойства, обусловленные наличием в их молекулах карбоксильной группы –СООН, так и основные свойства, обусловленные аминогруппой – NH2.