Процесс водяного парообразования
Фазовая p-v диаграмма (рис. 4.1) системы, состоящей из жидкости и пара, представляя собой график зависимости удельных объёмов воды и пара от давления, делится нижней пограничной кривой BK и верхней пограничной кривой KC на три области. Влево от кривой BK до нулевой изотермы воды (линия AE) располагается область жидкости. Вправо от кривой KC и вверх от точки K располагается область перегретого пара. В области, ограниченной нижней и верхней пограничными кривыми, располагается двухфазная система, состоящий из смеси воды и пара (влажный пар). Обе кривые сливаются в одной точке K, которая называется критической точкой. В критической точке исчезает различие между жидкостью и паром. Выше критической точки двухфазное состояние системы невозможно. Линия AE представляет собой точки, в которых вода имеет температуру 0 Линия BK – это место точек, характеризующих воду в состоянии кипения при разных давлениях. Линия KC показывает зависимость удельного объёма сухого насыщенного пара от давления. В технике (в паровых котлах) пар из воды образуется при постоянном давлении, поэтому термодинамическую сторону процесса парообразования можно рассмотреть так же при постоянном давлении: p = const. Если рассмотреть процесс образования перегретого пара при давлении p 1. Подогрев жидкости от температуры 0 (температуры насыщения) T 2. Парообразование при постоянной температуре T 3. Перегрев пара (нагревание пара от температуры T Количество теплоты, необходимое для превращения в сухой насыщенный пар (точка с
p
a
0 v v
v
Рис. 4.1. Диаграмма состояния водяного пара Из p-v диаграммы видно, что каждому давлению соответствует своя температура насыщения (линия KC). Характер зависимости между давлением насыщенного пара p
p
p
t
Рис. 4.2. Кривая насыщения
Каждому веществу соответствует своя кривая насыщения. Поскольку для насыщенного пара его давление и температура однозначно определяют друг друга, любой процесс, протекающий в двухфазной области, изображается на p-v диаграмме линией, совпадающей с кривой насыщения. Связь между термическими и калорическими величинами в процессе парообразования устанавливает уравнение Клапейрона – Клаузиуса:
где p T
r – скрытая теплота парообразования, Дж/кг; v v Степень отклонения свойств насыщенного пара от идеально-газового состояния определяется отличием от единицы коэффициента сжимаемости водяного пара, определяемого по формуле:
где R – газовая постоянная для водяного пара (R = 462 Дж/кг град). Таким образом, если на основе опытных данных построить зависимость p r = T Используя опытные значения p Уравнение состояния для водяного пара, как для реального газа, весьма сложно и в расчётной практике не применяется. Вследствие этого для практических целей при определении параметров пара и воды на линии насыщения используются справочные таблицы и диаграммы, составленные на основе экспериментальных и теоретических исследований. В этих справочных данных приведены температуры насыщения (t Таблица 4.1. Параметры насыщенного пара и воды на линии насыщения
В настоящей работе процесс парообразования осуществляется в области влажного пара при постоянном объёме (изохорный процесс): v – const. Этот процесс на p-v диаграмме (рис. 4.1) представлен линией 1-2.
|

 С при различных давления. Область графика, заключённая между изотермой воды при температуре 0
С при различных давления. Область графика, заключённая между изотермой воды при температуре 0 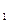 (см. рис. 4.1), то можно выделить три последовательно осуществляемых физических процесса:
(см. рис. 4.1), то можно выделить три последовательно осуществляемых физических процесса: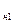 – отрезок a
– отрезок a  ) – отрезок с
) – отрезок с 
 T
T 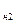 T
T  T
T 

 E
E
 p
p 




 p
p 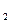 d
d 




 p
p  c
c 

 d
d  2 T
2 T 
 A B C T
A B C T 
 x = const
x = const
 v
v 

 v
v  v
v 

 и температурой насыщения T
и температурой насыщения T 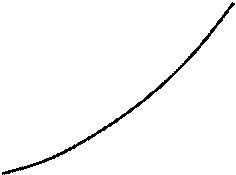 p
p 


 p
p 




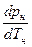 =
= 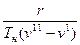 , (4.1)
, (4.1)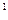 – удельный объём кипящей жидкости, м
– удельный объём кипящей жидкости, м 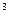 /кг;
/кг; – удельный объём сухого насыщенного пара, м
– удельный объём сухого насыщенного пара, м 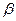 =
= 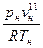 , (4.2)
, (4.2)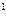 )
) 
 , Дж/кг (4.3)
, Дж/кг (4.3)