Задача 2. На окисление сернистого ангидрида по реакции 2SO2 +O2 Û 2SO3+Q поступает N0 =500 кмоль/ч газовой смеси
На окисление сернистого ангидрида по реакции 2SO2 +O2 Û 2SO3+Q поступает N0 =500 кмоль/ч газовой смеси, состоящей из четырех индивидуальных компонентов (мол. доли): nSO2=0, 15; nO2=0, 20; nSO3=0; nN2=0, 65. Степень превращения ХSO2 =0, 8. рассчитать материальный баланс процесса. Решение Решение выполняем в табличной форме по следующей схеме: · Рассчитываем мольное и массовое количество компонентов в приходе: Ni, 0 = N0× ni; mi, 0 = Ni, 0 × Mi; · Рассчитываем количество компонентов, участвующих в химической реакции; · Рассчитываем мольные и массовые количества компонентов в расходе. Решение задачи приведено в табл. 1.6. Таблица.1.6. Таблица материального баланса
При компьютерном расчете в среде пакета Excel оперируем адресами клеток: · для заполнения столбца D: в клетку D3 вносим значение =$B$9*C3, а затем копируем это произведение в клетки D4: D6. В клетке D7 получаем значение суммы, используя значок автосуммы S; · для заполнения столбца Е в клетку Е3 вносим произведение =D3*C3 и копируем его в клетки Е4: Е6. В клетке Е7 получаем значение суммы, используя значок автосуммы S; · для заполнения столбца G: в клетку G3 вносим значение =$D$3*$B$10, в клетку G4 - =$D$3*$B$10* F4/F3, в клетку G5 - =$D$3*$B$10* F5/F3. В клетке G6 значение равно 0; · для заполнения столбца Н в клетку Н3 вносим значение =D3-G3 и копируем его в клетки Н4: Н6. В клетке Н7 получаем значение суммы, используя значок автосуммы S; · для заполнения столбца I в клетку I3 вносим произведение =H3*B3 и копируем его в клетки I4: I6. В клетке I7 получаем значение суммы, используя значок автосуммы S. Решение с использованием программы EXCEL приведено в табл.1.7. Таблица 1.7. Расчет материального баланса с использованием программы EXCEL
На синтез аммиака по реакции N2+3H2 Û 2NH3 +Q поступает 50000 кг/ч газовой смеси, состоящей из четырех индивидуальных компонентов (мол. доли): nH2, 0 =0, 75, nN2, 0=0, 15, nNH3, 0 =0, 05, nCH4, 0=0, 05. Степень превращения водорода ХН2 - 0, 18. рассчитать материальный баланс процесса. Решение Исходный поток задан в массовых единицах, а его состав – в мольных долях. Для приведения размерностей состава и расхода к одним единицам измерения следует предпринять одно из следующих действий: · рассчитать молярную массу смеси по формуле (1.6), а затем мольный расход смеси по формуле (1.8) либо · пересчитать мольный состав потока в массовый по формуле (1.4). В решении, представленном в табл. 1.8, реализован первый путь. Ход расчета: · По формуле (1.6) рассчитываем молярную массу смеси и получаем Мсм = 7, 35 кг/кмоль. При компьютерном расчете в клетку В12 вводим выражение: =С3*B3+C4*B4+C5*B5+C6*B6; · По формуле (1.7) находим мольный расход смеси. При компьютерном расчете в клетку В13 вводим выражение =В9/В12. N0, см = 6802, 72109 кг/кмоль. Далее решаем по схеме, приведенной в задаче 1. Решение (с использованием пакета EXCEL) приведено в табл.1.8. Таблица 1.8. Расчет материального баланса с использованием программы Excel
На синтез аммиака по реакции N2+3H2 = 2NH3+Q поступает 50000 кмоль/ч газовой смеси, состоящей из четырех индивидуальных компонентов (масс. доли): gH2, 0=0, 15, gN2, 0 =0, 55, gNH3, 0 =0, 20; gCH4, 0=0, 10. Степень превращения водорода ХН2 - 0, 18. рассчитать материальный баланс процесса. Решение Исходный поток задан в мольных единицах, а его состав – в массовых долях. Следует пересчитать состав потока из массовых долей в мольные по формуле (1.5). Далее решать по схеме, приведенной в задаче 1. Ход расчета: 1. Рассчитываем мольные доли компонентов потока (см. столбец D в таблице). · в клетку D12 вводим выражение: =С3/B3+C4/B4+C5/B5+C6/B6 и получаем 0, 112658; · в столбец D вводим формулы для расчета ni. В клетку D3: =С3/B3/$D$12; в клетку D4: =С4/B4/$D$12 и т.д. Решение с использованием пакета EXCEL приведено в табл.1.9. Таблица 1.9. Расчет материального баланса с использованием программы Excel
1.6.4.Расчет материального баланса обратимых реакций, протекающих при смешении газовых потоков
|

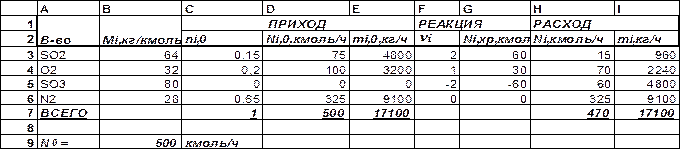 Задача 3
Задача 3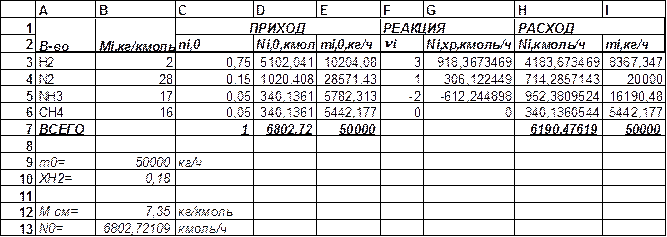 Задача 4
Задача 4



