Измерение первичной продукции.
Редактор: С. Лсбкдкап "Издательство ВИНОМ" 103473, Москва, Краснопролетарская, 16. Лицензия па издательскую деятельность серия./IP №0652-19 от 26.06,97 г. Издательство " Невский Диалект" Санкт-Петербург, 195220, Гражданский пр., 1-1. Лицензия на издательскую деятельность серия ЛР №065012 от 18.02.97 г. Подписано D печать 19.03.99. Формат 70x100 '/Hi. бумага офсетная. Печать офсетная. Гарнитура Петербург. Усл. печ. л. 27,3. Тираж 2000. Заказ 259 Отпечатано с готовых диапозитивов в типографии ИПО П|И)физдат, 1090/1'I, Москва, Крутицкий нал, 18. Илр № 050003 от 19.10.91 г. ISBN SVTeSDlBl-T 91785798 901319 ПЕРВИЧНАЯ ПРОДУКЦИЯ Первичная продукция лежит в основе всей трофической структуры сообщества. Все механизмы экосистемы приводятся в движение энергией, поставляемой фотосинтезом. Поток энергии через популяции растительноядных, плотоядных и детритоядных животных и происходящие в экосистеме круговороты питательных веществ в конечном счете зависят от первичной продуктивности растений. В состав растений входит не одна глюкоза (что следует из известного уравнения фотосинтеза). В различных биохимических процессах глюкоза используется не только в качестве источника энергии, но и в качестве материала для построения других более сложных органических соединений. В результате соответствующих перестроек сахара превращаются в жиры, масла и целлюлозу - основной материал, из которого состоят стенки растительных клеток. Азот, фосфор, сера и магний, соединяясь с углеродом, кислородом и водородом, образуют целый ряд белков, нуклеиновых кислот и пигментов. Хлорофилл, помимо атомов азота и углерода, содержит атом магния, подобно тому, как гемоглобин содержит атом железа. Таким образом, даже если все другие необходимые материалы имелись бы в достатке, растение, лишенное магния, не могло бы продуцировать хлорофилл, а тем самым не могло бы расти. Совершенно ясно, что растения не могут также функционировать и в отсутствие воды. Количество воды, необходимое для фотосинтеза, - это всего лишь капля по сравнению с тем огромным ее количеством, которое необходимо для того, чтобы покрыть расходы на транспирацию. Ткани растений состоят главным образом из воды, и вода служит той средой, в которой должны быть растворены питательные вещества, для того чтобы они стали доступными растениям. В основное уравнение продукции должно входить не только сырье, необходимое для фотосинтеза, но и ряд минеральных веществ. В создании продукции участвует много биологических реакций, но в общем виде этот процесс можно свести к следующему суммарному уравнению: СО2 + Н2О + минеральные вещества Наличие света и соответствующие температуры__ → → Растительная продукция + Кислород Не все сахара, образованные в процессе фотосинтеза, включаются в растительную биомассу, т. е. не все они идут на увеличение размеров и числа растений. Некоторая часть сахаров должна быть окислена, с тем, чтобы высвободить энергию, необходимую для биосинтеза и поддержания функций растения. В этом смысле растения не отличаются от животных: для поддержания своего существования им необходима энергия. Можно выделить два вида продукции - общую и чистую. Общая продукция - это вся та энергия, которая была ассимилирована в процессе фотосинтеза. Чистая продукция - это накопление энергии в растительной биомассе, проявляющееся в росте или размножении растений. Разность между общей и чистой продукцией составляет то количество энергии, которое растение расходует на дыхание. Таким образом, часть общей продукции (фотосинтез) идет на дыхание (функции поддержания), а часть представляет собой чистую продукцию (рост и размножение). В большинстве случаев при исследовании продуктивности растений, особенно в наземных местообитаниях, экологи измеряют не общую, а чистую продукцию, поскольку методы ее измерения менее сложны и поскольку именно она служит мерой ресурсов, доступных гетеротрофным потребителям в данной экосистеме. Измерение первичной продукции. Чистую продукцию удобно выражать в граммах ассимилированного углерода, в сухом весе или в энергетическом эквиваленте сухого веса. Всеми этими показателями пользуются попеременно. Содержание энергии в каком-либо органическом соединении зависит, прежде всего, от содержания в нем углерода и азота. Содержание углерода по весу в большинстве растительных тканей близко к его содержанию в глюкозе, т. е. к 40%. Когда в растениях сахара превращаются в жиры и масла, кислород отщепляется от их молекул, так что относительное содержание углерода возрастает. Например, трипальмитинглицерид (С51Н98С6) содержит 76% углерода по весу. Содержание энергии на 1 г в жирах и маслах более чем вдвое превышает ее содержание в сахарах, а поэтому они очень часто используются растениями и животными для запасания энергии. Соединение двуокиси углерода и воды в процессе фотосинтеза требует затраты 9,3 ккал энергии на каждый грамм ассимилированного углерода. Поэтому полное окисление какого-либо углеродсодержащего соединения до двуокиси углерода и воды должно было бы сопровождаться высвобождением ровно 9,3 ккал на 1 г окисленного углерода. Практически вследствие биохимических перестроек, с которыми связано образование большинства сложных органических соединений, количества энергии оказываются несколько иными. Принято считать, что при окислении 1 г углерода (сахаров, крахмала, целлюлозы) высвобождается 4,2 ккал энергии, 1 г белка—5,7 ккал, а 1 г жира—9,5 ккал. Общее уравнение продукции допускает несколько возможных методов измерения первичной продукции естественных местообитаний. Поглощение двуокиси углерода и минеральных питательных веществ, выделение кислорода - все эти величины пропорциональны продукции. Для измерения поглощения двуокиси углерода и продукции кислорода и органического вещества существуют надежные методы. Первичную продукцию наземных экосистем обычно оцениваютпогодовому приросту растительной биомассы (чистая продукция). Для того чтобы определить прирост за год, в конце вегетационного сезона растения срезают, высушивают и взвешивают. Этот метод сбора урожая обычно используют при определении биомассы культурных и дикорастущих растений в умеренных областях, где вся надземная часть у большинства растений ежегодно отмирает. Поскольку рост корней обычно не учитывается (из почв большинства типов корни извлекать трудно), урожай измеряет чистую годовую наземную продуктивность, которая чаще всего и используется в качестве основы для сравнения продуктивности наземных сообществ. Метод сбора урожая сталкивается с некоторыми трудностями. Часть первичной продукции поедают растительноядные животные. Рост корней, как только что отмечалось, измерить трудно, хотя корневые системы однолетних растений иногда удается отделить от почвы путем длительного отмывания. Однако у многолетников рост корней продолжается из года в год, так что их биомасса представляет собой результат многолетнего роста. Трудности измерения, создаваемые в луговых местообитаниях ростом корней, еще больше увеличиваются в лесах вследствие роста ветвей и стволов деревьев. Сбор листового опада и обрезка свежих побегов дают возможность оценить продукцию лишь частично. Годовой прирост деревянистых частей часто вычисляют, определяя отношение окружности ствола к общей биомассе и измеряя затем годовые приросты живых деревьев. Для оценки общей биомассы срубают ряд деревьев увеличивающегося размера, отделяют стволы от ветвей, а иногда и от корней, после чего сжигают все эти части по отдельности в больших печах и взвешивают золу. Годовой прирост окружности живых деревьев можно затем перевести в увеличение общего веса. Для полной оценки продукции к полученной величине прибавляют прирост листьев, цветков и плодов, т. е. частей, которые возобновляются каждый год. Специфической чертой продукционного процесса в водоемах служит то, что в образовании первичной продукции их большое значение имеет планктон, биомасса которого, как правило, во много раз меньше годовой продукции. Поэтому ни биомасса планктона в какой-либо момент года, например во время его максимального развития, ни средняя биомасса за год не могут служить мерой первичной продукции В природе одновременно происходят два противоположных процесса - построение и разрушение органических веществ. Новообразование органических веществ в темноте прекращается, следовательно, прекращается и потребление углекислоты из окружающей среды и выделение в среду эквивалентного количества кислорода. Процессы же дыхания, т. е. потребление кислорода и выделение углекислоты, в темноте идут с той же скоростью, что и на свету. Поэтому, сравнив результаты жизнедеятельности водных сообществ на свету и в темноте, можно рассчитать величину первичной продукции, а в известных случаях и деструкции в водоемах. О процессах построения и деструкции в принципе можно судить по нескольким различным показателям, например, по скорости потребления кислорода, выделения углекислоты, изменению рН, накоплению продуктов фотосинтеза и пр. В практике исследований в подавляющем большинстве случаев прибегали к измерениям содержания в воде растворенного кислорода. Следует сказать, что скорость потребления кислорода служит наиболее распространенным показателем интенсивности обмена водных организмов и скорости минерализации органических веществ, или скорости деструкции. Наконец, биомасса водных организмов, пропорциональная количеству органических веществ, может быть выражена эквивалентным ей количеством кислорода, потребного для полного окисления. Биомасса, выраженная в единицах кислорода, оказывается непосредственно сравнимой с результатами измерений интенсивности фотосинтеза (первичной продукции) и дыхания (деструкции). Таким образом, есть основания выделить кислородный метод определения величины первичной продукции в водоемах. При прослеживании круговорота углерода и изучении некоторых других вопросов можно было бы отдать предпочтение углекислоте в качестве единицы измерения, но для энергетического рассмотрения биотического круговорота углекислота как единица измерения непригодна, так как энергетический эквивалент ее в несравненно большей мере изменяется в зависимости от химического состава вещества. Известно, что для безазотистого дыхательного коэффициента (ДК) энергетические эквиваленты О2 и СО2 составляют следующее число калорий на 1 мл. Таблица
Для кислорода энергетический эквивалент при ДК=0,70 отклоняется всего на 7% от его значения при ДК=1,0, в то время как для углекислоты соответствующая разность составляет 33%. Для определения величин первичной продукции планктона могут быть использованы наблюдения в дневное и ночное время в открытой воде водоемов, т. е. расчеты величин первичной продукции по суточному ходу содержания кислорода и углекислоты, или же наблюдения за результатами жизнедеятельности планктона в воде, заключенной в незатемненные и затемненные сосуды. Наибольшее распространение получил последний способ, который может быть обозначен как метод склянок. По истечении известного срока экспозиции, например 24 часов, в незатемненном сосуде должно содержаться больше продуктов фотосинтеза и растворенного в воде кислорода и меньше углекислоты, чем в затемненном. Очевидно, что разности в содержании кислорода или углекислоты строго пропорциональны интенсивности фотосинтеза планктона. Таким образом, об интенсивности фотосинтеза планктона можно судить, пользуясь разными критериями. Соответственно с этим можно различить по меньшей мере три варианта метода склянок. Из них первый технически наиболее простой и наиболее распространенный кислородный вариант. Техника применения метода склянок проста. В этом существенное достоинство метода, который может быть использован, и в экспедиционных условиях. Склянки должны быть из белого стекла и иметь притертые пробки. Наиболее удобны склянки вместимостью 60— 160 мл. При таком объеме три склянки («контрольная» - для определения начального содержания кислорода, затемненная и незатемненная) могут быть заполнены из одного литрового батометра. С помощью склянок такого размера сделана большая часть наблюдений на разных водоемах, и поэтому такая вместимость их желательна для стандартизации метода. При всех наблюдениях методом склянок, особенно при стационарных работах, рекомендуется на каждый горизонт устанавливать две светлые и две затемненные склянки, как это и практиковалось почти всеми авторами. Когда наблюдения ведутся с помощью большого числа склянок, то при определении содержания кислорода удобно титровать не все содержимое склянки, а некоторый объем, отобранный с помощью пипетки после тщательного перемешивания раствора. При этом возможно повысить точность анализа путем повторного титрования. Например, из склянки в 120 мл можно дважды отобрать по 50 мл. При этом способе существенно облегчаются расчеты и отпадает необходимость точной калибровки склянок, но лишь в случае, когда все склянки имеют примерно один и тот же объем. Склянки с пробами, отобранными на нужной глубине, экспонируются на той же глубине. За исключением специальных наблюдений, срок пребывания склянок в водоеме должен быть равен 24 часам. На протяжении суток начинаются и заканчиваются циклические изменения освещения и других условий. Расчет первичной продукции по кислородной модификации метода склянок осуществляется следующим образом. Начальное содержание О2 в склянке перед экспонированием составляло V1, после экспозиции в светлой склянке содержание О2 было равно Vс, в темной склянке – Vт. Время экспозиции t = 24 ч. Первичную продукцию (мг О2/л.ч.) вычисляют по формулам: валовая продукция: Рвал = (Vс - Vт )/ t чистая продукция: Рчис = (Vс – V1 )/ t деструкция: Д = (V1 – Vт ) /t В данном случае первичная продукция и деструкция выражены в единицах кислорода. Первичная продукция может быть выражена в разных взаимоэквивалентных единицах. При переходе от одних единиц к другим принято исходить из следующих предпосылок: оксикалорийный коэффициент для органического вещества (ОВ) смешанного состава равен 3,4 кал/мг О2; в органическом веществе содержится 46% углерода; ассимиляционный коэффициент (АК) равен 1,12, а дыхательный коэффициент (ДК) равен 0,89. При этих условиях получаем следующие переходные коэффициенты: 3,2 мгО/мгС, 10,6 кал/мгС, 0,69 мгОВ/мгО2, 2,15 мгОВ/мгС. Если АК = 1,25 при ДК = 0,80, то коэффициент перехода от мгО2 к мгС составит 0,30, от мгС к калориям – 11,3. Радиоуглеродную модификацию метода склянок для определения первичной продукции морского планктона впервые применил Стеман-Нильсен во время работ датской морской экспедиции на судне «Галатея» (по Винберг,1960). Сущность предложенного Стеман-Нильсеном метода сводится к следующему. К заключенной в незатемненную склянку пробе добавляется известное количество меченой углекислоты в виде раствора карбоната или бикарбоната. Стеман-Нильсен ввел в практику исследований удобный прием предварительного приготовления ампул, содержащих нужные дозы раствора бикарбоната с меченым углеродом. Им применялись серии ампул, содержащих от 0,8 до 8 мкСu. После некоторого срока экспозиции проба профильтровывается через мембранный фильтр. Измерив активность фильтра с осевшим на нем планктоном (г) и зная общую начальную активность внесенного радиоуглерода (R), находят отношение этих величин г/R. Принимается, что количество ассимилированной углекислоты находится в том же соотношении с общим количеством ее во взятом объеме воды (с). Определив последнюю величину гидрохимическим путем, легко рассчитать искомое количество ассимилированной углекислоты (А). Очевидно, А = r c/ R Однако в такие расчеты приходится вносить некоторые поправки. Прежде всего допущение об одинаковой скорости ассимиляции С12 и С14 заведомо не совсем верно. Известно, что С14 ассимилируется с несколько меньшей скоростью. Это вызывает необходимость поправки на так называемую дискриминацию С14. Стеман-Нильсен считает, что меньшая скорость ассимиляции С14 компенсируется поправкой +5%. На результаты измерений методом меченого углерода может оказать влияние также темновая фиксация углекислоты, но она обычно не превосходит 1 - 2% от скорости ассимиляции на свету. Однако в загрязненных водах, где много бактерий, она может приобретать исключительно большое значение. Наиболее слабым местом метода является то, что с его помощью фактически измеряется не все количество ассимилированного радиоактивного углерода. Некоторая часть ассимилированных атомов во время опыта принимает участие в дыхании и вновь уходит во внешнюю среду в составе выделенных при дыхании молекул СО2. Какая доля от ассимилированных атомов С14 будет вновь отдана окружающей клетки среде, зависит от многих условий, в частности, и от продолжительности опытов. В длительных опытах вся выделяемая npи дыхании углекислота идентична ассимилированной; в этих условиях этим методом измеряется не валовая, а чистая продукция, т. е. не истинный, а видимый фотосинтез. Полагают, что при кратковременных опытах в среднем 60% выделяемой при дыхании углекислоты приходится за счет ассимилированной при фотосинтезе и что в условиях оптимального освещения интенсивность дыхания составляет 10% от интенсивности фотосинтеза. Тогда для получения истинного фотосинтеза (валовой продукции) следует внести поправку +6%. Вместе с поправками на дискриминацию С14 и на темновую фиксацию углекислоты (-1%) - это составит (+5 - 1+6) =10%. Последнюю величину (10%) Стеман-Нильсен вводит во все расчеты первичной продукции планктона. Но такая величина поправки годится только для условий, при которых дыхание составляет 10% от фотосинтеза. Когда дыхание составляет 25% от фотосинтеза, поправка равна 20%, при 50% поправка будет 50% и т.д. Таким образом, в различных условиях поправка должна быть разной, так что любое принятое постоянное значение ее будет в значительной мере произвольным. В связи с этим Джитс предложил отказаться от внесения поправки, ограничиваясь точными указаниями, при каких условиях (сроки экспозиции, освещение и пр.) получены соответствующие данные. Стеман-Нильсен отмечает, что при низких интенсивностях света поправка особенно велика. Поэтому он считает, что метод С14 не пригоден для измерений интенсивности фотосинтеза при очень малых интенсивностях света. Наличие хлорофилла в клетках является необходимым условием фотосинтеза. Большое число работ показывает закономерную связь между количеством хлорофилла растительных клеток и их продукцией и биомассой. Хлорофилльный метод измерения первичной продукции фитопланктона является весьма приближенным и его использование рекомендуется только в том случае, если невозможно измерение скляночным методом. Ориентировочный расчет продукции и биомассы фитопланктона по концентрации хлорофилла "а" проводят исходя из того, что хлорофилл "а" составляет 2,5 % сухой биомассы или 6,75% содержания органического углерода. Содержание хлорофилла "а" определяют фотометрическими и спектрофотометрическими методами. X. Одум (Н. Оdum) определял продукцию в сообществе целой реки, сравнивая изменение содержания кислорода в речной воде в дневное и ночное время и внося поправки на обмен кислородом между рекой и атмосферой. Комбинируя метод Одума с методом светлых и темных бутылей и с обычными методами сбора урожая (для тех мест, где растут крупные водоросли), можно довольно точно измерить продукцию в водных сообществах. Для измерения фотосинтеза в наземных экосистемах удобнее использовать обмен двуокиси углерода, чем обмен кислорода, так как двуокиси углерода в атмосфере содержится меньше. Небольшие изменения содержания двуокиси углерода измерить относительно легко (в атмосфере содержится всего 0,03% СО2), и утечки из камер для взятия проб не порождают серьезных ошибок. Метод измерения продукции по двуокиси углерода сходен с методом светлых и темных склянок. Часть местообитания или даже отдельное растение заключают в воздухонепроницаемую камеру и сравнивают уменьшение содержания СО2 в течение дня с его повышением (за счет одного только дыхания) ночью. Этот метод позволяет довольно точно измерять общую продукцию. Использование радиоактивного углерода, в частности изотопа 14С, представляет собой модификацию метода измерения продуктивности, основанную на газообмене. Когда в воздухонепроницаемую камеру добавляют известное количество радиоактивного углерода в форме СО2, растения ассимилируют радиоактивные атомы углерода в такой же пропорции, в какой они содержатся в воздухе камеры. Скорость фиксации углерода вычисляют, разделяя количество радиоактивного углерода, содержащееся в растении, на долю радиоактивной СО2 в камере в начале эксперимента. Таким образом, если растение ассимилирует 10 мг 14С за 1 ч, а доля 14СО2 в камере равна 5%, то можно вычислить, что растение ассимилирует углерод со скоростью 200 мг/ч (10:0,05). В процессе дыхания растение в конечном счете снова выделяет часть ассимилированного углерода в воздух в виде СО2, которую оно может ассимилировать вторично. Измеряя поглощение радиоактивного углерода на протяжении 1-3 ч, можно получить надежную оценку общей продуктивности. По прошествии одного-двух дней поглощение и выделение радиоактивного углерода приближается к стационарному уровню и получаемые оценки скорее относятся к чистой, нежели к общей продукции. Помимо С02 и воды, для синтеза органических соединений растения используют и другие вещества. Исчезновение из водных местообитаний растворенных нитратов и фосфатов может иногда служить относительной мерой чистой продукции, но только при определенных условиях: рост должен происходить быстро и растения должны превращать неорганические питательные вещества в биомассу гораздо быстрее, чем вещества эти становятся им доступными в результате разложения мертвых растений или смешивания с глубинными слоями воды. Когда процессы продукции и разложения уравновешиваются и устанавливается некий стационарный режим, то освобождение неорганических питательных веществ при разложении происходит с такой же скоростью, как их ассимиляция при фотосинтезе, а поэтому концентрация в среде растворенных питательных веществ не изменяется. Кроме того, следует иметь в виду, что накопление питательных веществ в растениях не обязательно связано какой-то постоянной зависимостью со скоростью продукции. Известно, например, что водоросли поглощают больше фосфора при высоком содержании в среде растворенных фосфатов, чем при их недостатке. А иногда растворенные минеральные вещества выделяются растениями в среду. Многие физические и химические процессы, в частности эрозия, апвеллинг и осаждение, также оказывают влияние на содержание питательных веществ в водных системах. Надежные оценки продуктивности по исчезновению из среды неорганических питательных веществ можно получить только в период «цветения» водорослей, наступающий в морях и озерах умеренной и арктической зон вслед за зимним периодом покоя.. Сравнение нескольких методов измерения продуктивности водных экосистем было проведено на фьордовом озере Огак на Баффиновой Земле (Канада). Первичную продукцию измеряли в течение всего вегетационного сезона по поглощению радиоактивного углерода в светлых бутылях, помещенных в озеро, а кроме того, наблюдали за изменением концентрации хлорофилла, нитратов, фосфатов и растворенного кислорода (рис. 7.2). Суточная продуктивность озера быстро возрастала в начале лета, когда лед исчезал с поверхности и свет начинал проникать в глубину воды. Концентрация хлорофилла возрастала параллельно возрастанию продуктивности, а концентрации нитратов и фосфатов понижались на протяжении всего лета. Концентрация растворенного кислорода повышалась весной вместе с вспышкой растительной продукции, но затем усиление дыхания зоопланктона затруднило выявление какой-либо прямой зависимости между концентрацией кислорода и продукцией. Любопытно, что возрастание продукции, наблюдавшееся в конце лета, не зависело ни от одного из регистрируемых факторов.
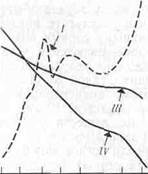
Рис. 7.2. Соотношение между продуктивностью фитопланктона (/) к концентрацией хлорофилла (II), фосфатов (х1,7) (III), нитратов (IV), кислорода (V) и зоопланктона (VI, произвольные единицы) в озере Огак на Баффиновой Земле.
|