Растворы слабых электролитов. Константа диссоциации слабого электролита. Факторы, влияющие на степень диссоциации слабого электролита.
Слабые электролиты (a < 3 % в 0,1 М растворах). Слабыми электролитами являются H2S, H2CO3, HNO2, HCN, H2SiO3, H3BO3, HClO и др., а также большинство оснований многовалентных металлов, NH4OH и вода. Слабые электролиты диссоциируют частично и обратимо. В их растворах преобладают не ионы, а молекулы. К равновесию, которое устанавливается в растворе слабого электролита между молекулами и ионами, можно применить законы химического равновесия и записать константу равновесия, которая называется константой диссоциации (КД) и приводится в таблицах. Константа диссоциации характеризует силу электролита: чем больше величина КД., тем сильнее электролит, и наоборот.
Степень диссоциации зависит от природы электролита, его концентрации, природы растворителя, присутствия в растворе одноименных ионов, температуры. Для одного и того же электролита при данной температуре степень диссоциации (a) увеличивается с разбавлением раствора; при больших разбавлениях электролит полностью диссоциирует (a®1). С увеличением температуры a также увеличивается.
|

 HNO2
HNO2  H+ + NO2– (уравнение электролитической диссоциации)
H+ + NO2– (уравнение электролитической диссоциации)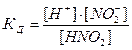
 1, где [H+], [NO2-], [HNO2] – молярные равновесные концентрации соответствующих частиц в растворе, КД– константа диссоциации азотистой кислоты HNO2
1, где [H+], [NO2-], [HNO2] – молярные равновесные концентрации соответствующих частиц в растворе, КД– константа диссоциации азотистой кислоты HNO2


