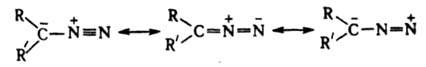Введение. В ходе данной работы произведён расчёт различных составляющих ошибки наведения
СИНТЕЗ 2-НАФТОЛОРАНЖЕВОГО КРАСИТЕЛЯ Отчет по лабораторной работе № 1 по дисциплине «Органическая химия»
Специальность 1 - 49 01 02 «Технология и хранения и переработки животного сырья» Специализация 1 – 49 01 02 01 «Технология мяса и мясных продуктов»
Могилев 2014г
Цель работы Получить 2-нафтолоранжевый краситель, исходя из 5 г сульфаниловой кислоты. Введение
В основе технологии получения азокрасителей лежат две химические реакции: 1) диазотирование ароматического амина, 2) сочетание полученного диазосоединения с амином или фенолом 2-нафтолоранжевый краситель относится к группе красителей, молекула которых содержит -N=N-.Однако не всякое окрашенное вещество представляет собой краситель; последний помимо окраски должен обладать еще способностью поглощаться окрашиваемым волокном и прочно на нем закрепляться. Эту способность придают красителю так называемые ауксохромные группы, например гидроксильная группа, аминогруппа,сульфогруппа и некоторые другие. Сейчас естественные красители полностью вытеснены синтетическими. Области применения природных красителей всё больше и больше суживались, и в наши дни они ограничены лишь специальными областями, например, окрашивание некоторых продуктов питания.[1,4,5] Диазосоединeния, содержат группировку N2, связанную с одним органическим остатком. Свойства алифатических и ароматических диазосоединений различаются очень резко. Наиболее важны в практическом отношении соли диазония. Из-за низкой термической стабильности их обычно используют сразу после получения, не выделяя из растворов. Твердые соли диазония, у которых Х - остаток минеральной кислоты (например, HSO4-, NO3-, Сl-, СlO4-), неустойчивы и часто взрываются. Соли с анионами комплексных кислот (ZnCl3- и BF4-), а также с ArSO3-сравнительно устойчивы. Щелочная соль цис-диазотата в твердом виде крайне неустойчива. В щелочном растворе при нагревании циc-диазотат превращается в транс-форму, щелочные соли которой стабильны; они бесцветны или окрашены в желтый цвет. При недостаточной кислотности среды образуются т. н. диазосмолы, что часто является причиной низкого выхода и плохого качества фенолов и азокрасителей, получаемых в соответствующих производствах. Соли диазония в присутствии солей Cu (I) и некоторых других металлов легко замещают диазо-группу атомом галогена, а также группами CN, NCS, NO2, HS, RS, SO2H и др. В кислых средах при действии SnCl2 соли диазония восстанавливаются в арилгидразины: Диазотирование — взаимодействие ароматических аминов с HNO2 с образованием ароматического диазосоединения. Обычно при диазотировании пользуются NaNO2 в присутствии избытка неорганической кислоты: R—NH2 + 2HCl + NaNO2 —> R—N2Cl + NaCl + 2H2O где R — органический радикал.
|

 . Под действием света соли диазония разлагаются, причем особенно легко, если в орто- и пара-положениях находятся сильные электронодонорные заместители; в результате фотолиза выделяется N2, происходит сужение кольца и образуются высокомолекулярные соединения.
. Под действием света соли диазония разлагаются, причем особенно легко, если в орто- и пара-положениях находятся сильные электронодонорные заместители; в результате фотолиза выделяется N2, происходит сужение кольца и образуются высокомолекулярные соединения.