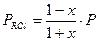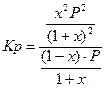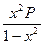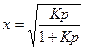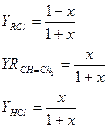Расчет константы равновесия химической реакции.
Расчет константы равновесия химической реакции приведен в Таблица 7. Расчет константы равновесия химической реакции.
Зависимость константы равновесия химической реакции от температуры отражена на рисунке 5.
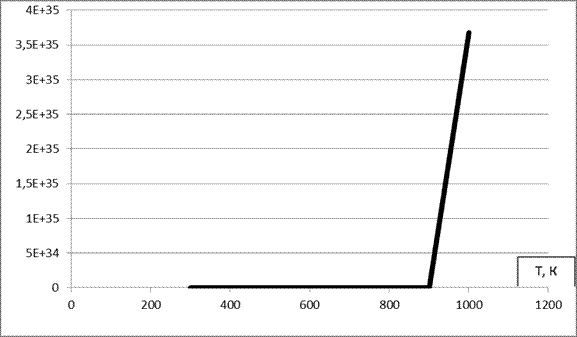
Рисунок 5. Зависимость Кр=f(T)
Из рисунка 5 можно отметить резкое увеличение Кр, начиная от температуры 900 К. Равновесие при этих температурах резко сдвинуто в сторону продуктов реакции. Расчет равновесного состава реакционной смеси по закону действующих масс.
Для данной реакции: Кр = Парциальные давления определяются по закону Дальтона:
Материальный баланс веществ в реакционной смеси определяется по выражениям: nRCl=1-x, nRCН=CH2=x, nRCl=x, где х – равновесный выход продукта. Мольный состав реакционной смеси будет равен: ån i = nRCl+ nRCН=CH2+ nHCl =1-x+x+x=1+x.
Kp=
Расчет равновесного состава реакционной смеси по закону действующих масс представлен в таблице 8.
Таблица 8. Расчет равновесного состава реакционной смеси
Из таблицы 8 следует, что равновесный выход достигается уже при Т=400 К. При этой температуре протекание реакции не лимитируется термодинамическими ограничениями.
|

 = - RTlnKp
= - RTlnKp
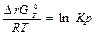
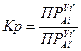
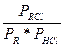
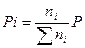
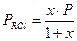 ,
,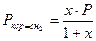 ,
,