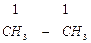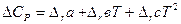Расчет изменения термодинамических функций по закону Гесса для стандартных условий.Для общей реакции: ν1А 1 + ν 2А2 = ν Изменение энтальпий, энтропий и теплоемкостей определяются по формулам:
где
Таблица 2. Расчет термодинамических функций методом введения поправок.
Расчет изменения термодинамических функций по закону Гесса для стандартных условий. Для общей реакции: ν1А 1 + ν 2А2 = ν Изменение энтальпий, энтропий и теплоемкостей определяются по формулам:
где
Для данной реакции: ΔrH0298= ΔfH0298(C7H15Cl)- ΔfH0298(C7H14)- fH0298(HCl)=-213926+61923+92310= = -59693 Дж/моль Процесс изменения энтальпии реакции имеет отрицательный показатель, следовательно, этот процесс экзотермический.
ΔrS0298= ΔS0298(C7H15Cl)- ΔS0298(C7H14)- ΔS0298(HCl)= 209,492-423,58-186,79= = -400,868 Дж/моль*К
Изменение энтропии убывает в этой химической реакции вследствие того, что из неупорядоченного состояния системы (два соединения) образуется одно соединение.
Δra= a(C7H15Cl)- a(C7H14)- a(HCl)= 35,686-9,80-26,53= -0,644 Δrb= b(C7H15Cl)- b(C7H14)- b(HCl)= 561,645-605,85-4,60= -48,805 Δrc= c(C7H15Cl)- c(C7H14)- c(HCl)= -207,984+334,15-1,09= 125,076
|

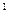 1А
1А 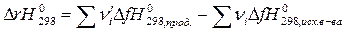 ,
,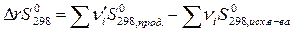 ,
,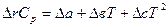 ,
,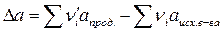 ,
,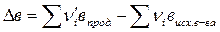 ,
,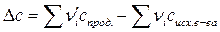 .
. , Дж/моль
, Дж/моль
 ,
Дж/
моль К
,
Дж/
моль К