Строение атома и периодический закон
Строение атома и периодический закон
1. Составить электронную формулу элемента. Описать химические свойства по его положению в Периодической системе. 2. Назвать элементы, имеющие следующие электронные формулы (с указанием символа, порядкового номера, группы, подгруппы, периода): a) Is22s22p63s23p1, б) Is22s22p63s23p63d54s1, в) Is22s22p63s23p63d104s24p5. 3. Какой из элементов — магний или барий — обладает более выраженными металлическими свойствами и почему? 4. Составить молекулярные формулы соединений: а) алюминия с углеродом, б) стронция с селеном, в) галлия с иодом, г) фосфора с, хлором. 5. Указать среди приведенных структурных символов элементов изотопы и изобары: Изобары, атомы различных химических элементов с одинаковым массовым числом А. Ядра И. содержатравное число нуклонов, но различные числа протонов Z и нейтронов N. Например, атомы 104Be, 105B, 106Cпредставляют собой три И. с A = 10.
изомеры одинаковых по атомному составу и молекулярной массе, но различающихся по строению или расположению атомов в пространстве и, вследствие этого, по свойствам
6. Сколько валентных электронов у мышьяка? Какие степени окисления он может проявлять в соединениях? 7. Могут ли электроны иона K+ находиться на следующих орбиталях: 8. Приведите примеры 4-х частиц (атомы, ионы) с электронной конфигурацией 1s22s22p6 9. Сколько элементов было бы в третьем периоде, если бы спиновое квантовое число имело единственное значение +1 (остальные квантовые числа имеют обычные значения)?
10. Какие квантовые числа и как должны, по вашему мнению, измениться при переходе от нашего мира к а) двумерному; б) четырехмерному?
Квантовые числа - это энергетические параметры, определяющие состояние электрона и тип атомной орбитали, на которой он находится.
|

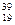 К,
К,  Pt,
Pt,  Ni
Ni 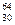 Zn,
Zn, 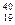 K,
K, 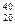 Ca,
Ca, 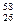 Fe,
Fe,  Pt,
Pt,  Ar,
Ar,  Hg,
Hg, 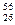 Fe,
Fe, 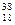 Аг,
Аг, 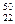 Ti,
Ti, 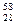 Ni,
Ni, 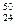 Cr,
Cr,  Zn.
Zn.


