Фазовое равновесие в идеальной бинарной смеси
Когда силы взаимодействия между одинаковыми (ЛЛК-ЛЛК, ТЛК-ТЛК) и разными (ЛЛК-ТЛК) молекулами различаются незначительно, то коэффициенты активности близки к единице. Для данного случая из равенства (1а) с учетом условия (х 1 + х 2=1) получают уравнение фазового равновесия Фенске
Чем больше величина относительной летучести a, тем легче разделить бинарную смесь ректификацией. 2.4 Диаграммы фазового равновесия Р-х, t-х-у, у-х для идеальной бинарной смеси и взаимосвязь между ними Общее давление паров над идеальной бинарной смесью летучих веществ при фиксированной температуре линейно возрастает с увеличением доли ЛЛК в жидкости:
При кипении смеси летучих веществ паровая фаза обогащается ЛЛК. При конденсации паровой смеси в жидкую фазу преимущественно переходит ТЛК.
2.5 t-х-y диаграммы фазового равновесия азеотропных смесей
|

 (2а)
(2а) . (2б)
. (2б)


 Положительное отклонение
от закона Рауля. Силы ЛЛК-ТЛК
меньше сил ЛЛК-ЛЛК и ТЛК-ТЛК.
Положительное отклонение
от закона Рауля. Силы ЛЛК-ТЛК
меньше сил ЛЛК-ЛЛК и ТЛК-ТЛК.
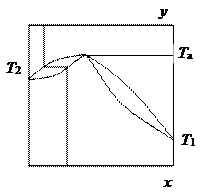 Отрицательное отклонение
от закона Рауля. Силы ЛЛК-ТЛК больше сил ЛЛК-ЛЛК и ТЛК-ТЛК.
Отрицательное отклонение
от закона Рауля. Силы ЛЛК-ТЛК больше сил ЛЛК-ЛЛК и ТЛК-ТЛК.
 Т-х-y диаграмма для ограниченно растворимых веществ.
Т-х-y диаграмма для ограниченно растворимых веществ.



