Растворы неэлектролитов
Растворы неэлектролитов состоят из незаряженных частиц. Они могут быть образованы различными парами органических жидкостей, например бензолом и толуолом. Установлено, что молекулы нелетучего растворенного компонента раствора препятствуют улетучиванию из раствора молекул растворителя. Согласно закону Рауля понижение давления DP насыщенного пара растворителя над раствором пропорционально мольной доле растворенного нелетучего вещества ni: DP = P0 – P = P0 ni, или где Р 0 – давление насыщенного пара растворителя над чистым растворителем; P – давление насыщенного пара растворителя над раствором, DP – разность между давлениями насыщенного пара растворителя над раствором P и растворителем Р 0; n – количество растворенного вещества в растворе (моль); N – количество вещества растворителя (моль); ni – мольная доля растворенного вещества. Из закона Рауля возникают два следствия. 1. Температура кипения раствора выше температуры кипения растворителя. Повышение температуры кипения DТкип пропорционально моляльной концентрации раствора сm: DТкип = Кэсm, (24) где Кэ – эбулиоскопическая постоянная растворителя.
где g – масса растворенного вещества, г; G – масса растворителя, г; 2. Температура замерзания раствора ниже температуры замерзания чистого растворителя. Понижение температуры замерзания DТзам пропорционально моляльной концентрации раствора сm: DТзам = Кксm, (26) где Кк – криоскопическая постоянная. Значения Кэ и Кк зависят от природы растворителя. Используя уравнения
где DТ – изменение температуры кипения или замерзания раствора; Самопроизвольный переход растворителя через полупроницаемую мембрану, разделяющую раствор и растворитель или два раствора с различной концентрацией растворенного вещества, называется осмосом. Осмос обусловлен диффузией молекул растворителя через полупроницаемую перегородку (мембрану), которая пропускает только молекулы растворителя. Количественно осмос характеризуется осмотическим давлением, равным силе, приходящейся на единицу площади поверхности, и заставляющей молекулы растворителя проникать через полупроницаемую перегородку. Осмотическое давление возрастает с увеличением концентрации растворенного вещества и температуры. Вант-Гофф предположил, что для осмотического давления можно применить уравнение состояния идеального газа: pV=nRT; где p – осмотическое давление (Па); n – количество вещества (моль); V – объем раствора (м3); С – молярная концентрация раствора, R – универсальная газовая постоянная, 8,3144 Дж/(моль×К).
|

 , (23)
, (23)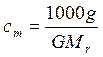 (25)
(25)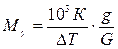 , (27)
, (27) ; p =СRT, (28)
; p =СRT, (28)


