Кристаллические структуры металлов и сплавов.
Магний өндіру технологиясы Магний өндірісіндегі негізгі шикізат болып магнезит MgCO3, доломит MgCO3× CaCO3, карналлит MgCl2 × KCl × 6H2O қолданылады. Металдық магнийді алудың екі әдісі бар: термиялық; және электролиттік. Бірінші әдіс магний тотығының көміртегімен немесе кремниймен тотықсыздануына, ал екінші әдіс балқытылған хлорлы магнийдің MgCl2 электролизіне негізделген. Негізінен металдық магнийді өндірудің электролиттік әдісі кеңінен таралған. Ол екі негізгі үрдістерден тұрады: бастапқы шикізаттан хлорлы магнийді алу және оның электролизі. Хлорлы магниді алу үшін магнезитті немесе доломитті күйдіруден алынған магний тотығын 800 - 900оС - те көміртегінің қатысуымен хлорлайды:
MgCO3 = MgO + CO2,
MgCO3×CaCO3 = MgO + CaО + 2CO2,
MgO + Cl2 + C = MgCl2 + CO2.
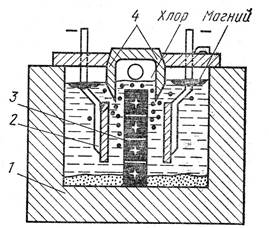
Балқытылған магний хлоридінің электролизі шамотпен футеровкаланған тікбұрышты герметикалық ванна түріндегі элетролиздегіштерде іске асырылады (сурет 1). Анодтарды графиттен, ал катодтарды екі болат пластиналарынан жасайды. Электролит ретінде хлорлы тұздар MgCl2 (7 - 15%), NaCl, KCl, CaCl2 балқымасы қолданылады. Анод пен катод кеңістіктері оттөзімді диафрагмамен бөлінген. Тотықсызданғаннан кейін магний мен хлор әрекеттеспеуі қажет, өйткені осының салдарынан магний хлорда жанып кетеді:
Mg + Cl2 = MgCl2.
Электр тоғы электролит арқылы өткенде оны қыздырып, электрхимиялық үрдіс іске асады. Магний иондары катодта тотықсызданады:
Mg2+ + 2e = Mg.
Магнийдің тығыздығы электролит тығыздығынан кем, соның салдарынан ол қалқып шығып, ванна бетінде жинақталады. Таза магнийдің тотығуының алдын алу үшін ванна беті керамикалық қақпақпен жабылады. Балқыған магний вакуумды шөміштермен және сифондармен периодты түрде ваннадан шығарылады. Анодта түзілген хлор арнайы құбыр арқылы сорылып алынады. Электролизден кейін магнийдің құрамында көп мөлшерде қоспалар болады. Оны тигельді пештерде қождамалармен өңдеу немесе ұшыру арқылы қайта балқытып рафинадтайды. Құрамында 99,9% - дан артық магний бар рафинадталған металл құю машинасында құйылады. Құю кезінде магний ағыны күкірт ұнтағын үрлеу арқылы тотығудан қорғалады.
Магнийді электролиздегіш сұлбасы:
1 - болат бүркенішіндегі отқа төзімді кірпіштен жасалған ванна; 2 - болат катодтары; 3 - графитті анодтар; 4 - отқа төзімді диафрагмалар.
Магний кентастарының басты кен орындары магнезиялы калий тұзды қазбалары. Магнезиттің ірі кен орындары метаморфозды доломиттерде көп кездеседі. Магнезит отқа төзімді шикізат, магний металын алуға қолданылады. Калий-магнийлі тұздарды тыңайтқыш алу үшін өңдегенде шыққан қалдықтардан да магний алынады. Солтүстік Арал маңындағы Жақсықылыш, Жаманқылыш көлдерінде, Жамбыл облысындағы Тұзкөлде эпсомит, астраханит сияқты магнийлі тұздардың қабаттары ұшырасады. Маңғыстаудағы Қаракие ойысына Каспий теңізінен құйылған су буланғанда едәуір мөлшерде магнийлі тұздар тұнады. Шығыс Қазақстан, Қостанай, Қарағанды, Павлодар облыстарының ультранегізді талькты-карбонатты жыныстарында магний кентастарының мөлшері мол.
I. ОБЩЕЕ ПРЕДСТАВЛЕНИЕ О СТРОЕНИИ МЕТАЛЛОВ Кристаллические структуры металлов и сплавов. Металлы и их сплавы в твердом состоянии – это кристаллические тела, атомы которых располагаются относительно друг друга в определенном, геометрически правильном порядке, образуя кристаллическую решетку. В кристаллической решетке можно выделить элемент объема, образованный минимальным количеством атомов, многократное повторение которого в пространстве по трем непараллельным направлениям позволяет воспроизвести весь кристалл. Этот элементарный объем, характеризующий особенности строения данного типа кристалла, называется элементарной ячейкой. Для ее описания используют 6 величин: три ребра ячейки a,b,c и три угла между ними α, β, γ (рис. 1.1, а) – это параметры элементарной ячейки. Существует 14 типов кристаллических решеток, свойственных элементам периодической системы. Наиболее распространенные – это (рис1.1, б-г): 1) объемно-центрированная кубическая (ОЦК) – атомы расположены в вершинах и центре куба (Na, V, Nb, Feα, K, Cr, W); 2) гранецентрированная кубическая (ГЦК) - атомы расположены в вершинах куба и в центре каждой грани (Pb, Al, Ni, Cu, Co, Feγ и др.); 3) гексагональная плотноупакованная (ГПУ) – четырнадцать атомов расположены в вершинах и центре шестиугольных оснований призмы, а три – в средней плоскости призмы (Mg, Ti, Zn, Be, Ca и др.)
.
Рис.1.1.1 14 типов кристаллических решеток (пространственные решетки Бравэ). Все 14 решеток Бравэ распределены по семи кристаллическим системам (сингониям) в соответствии с ориентацией и относительными величинами параметров решетки (рис. 1.1.1). Кристаллическую решетку характеризуют следующие основные параметры: Период решетки с – расстояние между двумя соседними параллельными кристаллографическими плоскостями, составляет 0,1-0,7 нм (1 нм= 10-9 см), (рис.1.1, б – параметр а, рис.1.1, в – параметр а, рис.1.1, г – параметр с). Координационное число – это количество атомов, находящихся на наиболее близком и равном расстоянии от любого выбранного атома в решетке. Для ОЦК координационное число – 8, для ГЦК – 12, для ГПУ – 12. Базис – количество атомов, приходящихся на одну элементарную ячейку. (Так, на одну элементарную ячейку ОЦК решетки приходятся два атома: один, находящийся в центре куба и принадлежащий только данной ячейке, и второй – как сумма долей, которую вносят атомы, расположенные в вершинах куба и принадлежащие одновременно восьми сопряженным элементарным ячейкам (1/8 * 8 = 1), т.е. каждый атом в вершине куба принадлежит одновременно 8-ми сопряженным элементарным ячейкам)). Базисное число ГЦК и ГПУ решеток равно 4. Коэффициент компактности (плотность упаковки) решетки η – это отношение объема Va, занимаемого атомами, к объему элементарной ячейки Vp: η= Va/ Vp Плотность упаковки ηоцк=0,68, ηгцк=0,74, ηгпу=0,74. Т.к. плотность атомов в различных плоскостях неодинакова, то химические, физические, механические свойства отдельно взятого кристалла в разных направлениях будут отличаться. Такое различие свойств называется анизотропией. В аморфных телах атомы не образуют кристаллическую решетку и их свойства не зависят от направления, т.е. они изотропны. Технические металлы – поликристаллические тела,состоящие из множества мелких различно ориентированных кристаллов, и их свойства во всех направлениях усредняются. Т.е. металлы и сплавы изотропны. Структура поликристаллического тела показана на рис. 1.2.
Рис. 1.2. Структура поликристаллического тела.
|