Молекула- кинетикалық теорияның негізгі қағидалары.
Молекулалардың өлшемдері. Броундық қозғалыс. Оқушылардың 7-9 сыныптағы физика және 8-9 сыныптағы химия курсынан алған білімдерін негізге ала отырып МКТ негіздерін оқытуды заттың құрылысынан бастаған дұрыс. Оқушылар молекула және атомның құрылысы, элементар бөлшектер (протон, нейтрон,электрон және т.б) жөніндегі алғашқы мағлұматтарына сүйене отырып, зат дегеніміз бөлшектерден тұратынын және ол материяның бір түрі екенін анықтаймыз. Оқушыларға молекула, атом, ион, атом ядросы, элементар бөлшектер (протон, нейтрон, электрон және т.б.) заттың әр түрлі құрылымдық формасы екенін түсіндіру керек. Зат құрлысының МКТ негізі ретінде әрқайсысы тәжірибе жүзінде дәлелденген үш қағида алынады: 1)зат ұсақ бөлшектерден тұрады; 2)бұл бөлшектер бір -бірімен өзара әсерлеседі; 3)бөлшектер үнемі қозғалыста болады. МКТ негіздері тақырыбындағы негізгі ұғым молекула ұғымы оны оқушылардың түсінуінің қиындығы сонда бұл бар нәрсе, бірақ оны қарапайым түрде бақылауға болмайды. Сондықтан да мұғалім оқушыларға бар екенін,оны танып білуге болатынын дәлелдеп шығуы тиіс. Негізінен молекулалардың бар болуының шындығына көз жеткізу үшін олардың өлшемдерін анықтайтын және олардың қозғалыста болатынын дәлелдейтін классикалық тәжірибелерге көбірек көңіл бөліп оқытқан жөн. 1) Молекулалардың өлшемін ең алғаш рет Рэллейдің жасаған тәжірибесінен көруге болады: Мұнда үлкен ыдысқа құйылған зәйтүн майының жайылуын қарастырып молекуланың диаметрі анықталады. 2) Молекулалардың массасын француз ғалымы Ж.Пэрреннің (1870-1943жж.) жасаған тәжірибесінен анықтауға болады (суды шайыр тамшысы ауадағы молекулалар сиякты қозғалыста болады). Перрен 0,0001 см эмульсия қабатындағы шайыр тамшыларының санын микроскоп арқылы санаған
мұнда Қазіргі кезде молекуланың массасы өте дәлдікпен анықталған. Мысалы, оттегі молекуласының массасы 3) Молекуланың жылдамдығын Штерн 1920 жылы анықтаған. Молекула 1секундта 500 метр жер жүреді. Штерн тәжірибесінің үлгісін "Айналмалы диск" арқылы көрсетуге болады. 4) Зат мөлшері ұғымдары енгізіліп, формуласы беріледі. 5) Заттың мольдік массасы деп бір мольдің мөлшерінде алынған заттың массасын айтамыз. Ал,
Мольдік масса былай анықталады: Молекулалардың қозғалыста болғанын Броунның (ағылшын ботанигі) бақылауларын айта отырып түсіндіру керек. Броундық қозғалысты бақылаудан шығатын қорытындылар: а) қалқыған броундық бөлшектердің қозғалысы молекулалардың соқтығысқанынан пайда болады, ә) броундық бөлшектердің қозғалысы үздіксіз және бейберекет қозғалыста болады, ол сол заттың қасиеттеріне тәуелді. б) қалқыған бөлшектердің броундық қозғалысы молекулалардың қозғалысын көрсетеді. в) бөлшектердің броундық қозғалысы молекулалардың бар екенін, олардың үнемі бейберекет қозғалыста болатынын дәлелдейді. Реал газдарды танып, оқып білу ушін идеал газ үлгісін қарастырамыз. Негізінен физикада идеал газдың екі анықтамасы бар: термодинамика және молекула-кинетикалық. Термодинамикадағы анықтамасы бойынша идеал газ дегеніміз температура тұрақты болғанда, белгілі массада газдың қысымы оның көлеміне кері пропорционал болатын газ. Молекула-кинетикалық көзқарас бойынша идеал газ деп молекулалары материалдық нүкте болып табылатын, өзара әсерлеспейтін, соқтығысқан кезде серпімді соқтығыс болатын газды айтады. Газ молекулалары арасында жылулық тепе-теңдік орнағанда ғана идеал газ деп айтуға болатынын оқушыларға ескерту қажет. Идеал газ үлгісінің қолдану шегі- өте жоғарғы қысымда және өте төменгі температурада қолдануға болмайды. Егер газ сығылса, оның тығыздығы артады және молекулалардың арасындағы қашықтық кішірейеді, олардың соқтығысуы көбейеді, әрі бір-бірімен әсерлесуі көбейеді. Мұндай жағдайда молекулалардың өлшемін ескермеуге болмайды. Ал газдың қысымы тек молекулалардың соқтығысуынаң ғана емес, олардың өзара әсерлесіне байланысты. Егерде газдың қысымы 108Па-даң артса, онда Бойль-Мариот заңынаң көп ауытқу болатының эксперименттен белгілі. Өте төменгі температурада осындай жағдайлар болады. Идеал газ ұғымын қалыптастыруға қайталау сабақтарында жалпы жоспарды пайдалануға болады.
|



 м биіктікте ыдыс түбімен салыстырғанда тамшылар саны екі есеге азайған. Осы заңдылықты ауадағы оттегі молекулаларына қолданып, оттегі молекуласының массасын анықтады.
м биіктікте ыдыс түбімен салыстырғанда тамшылар саны екі есеге азайған. Осы заңдылықты ауадағы оттегі молекулаларына қолданып, оттегі молекуласының массасын анықтады.
 шайырдың бір тамшысының массасы.
шайырдың бір тамшысының массасы.  км атмосфераның биіктігі. Шамалардың мәндерінде оттегі молекуласының массасы
км атмосфераның биіктігі. Шамалардың мәндерінде оттегі молекуласының массасы 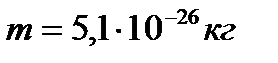 екендігін есептеп тапқан.
екендігін есептеп тапқан.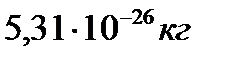 , сутегі молекуласының массасы
, сутегі молекуласының массасы  .
. және
және 
 мольдік масса. БХБЖ зат мөлшері мольмен өрнектеледі. Бір моль бұл массасы 0,012 кг көміртегіндегі қанша атом болса, сонша молекуласы немесе атомы бар заттың мөлшері. Кез-келген заттың 1 моліндегі атомдар, иондар немесе молекулалар саны бірдей. Бір молдегі атомдар саны
мольдік масса. БХБЖ зат мөлшері мольмен өрнектеледі. Бір моль бұл массасы 0,012 кг көміртегіндегі қанша атом болса, сонша молекуласы немесе атомы бар заттың мөлшері. Кез-келген заттың 1 моліндегі атомдар, иондар немесе молекулалар саны бірдей. Бір молдегі атомдар саны  деп белгілейді және оны итальян ғалымы (ХІХ ғасыр) құрметіне Авагадро тұрақтысы деп аталады және
деп белгілейді және оны итальян ғалымы (ХІХ ғасыр) құрметіне Авагадро тұрақтысы деп аталады және  тең.
тең. .
.  заттың массасы.
заттың массасы. , мұндағы
, мұндағы  заттың салыстырмалы массасы. Заттағы молекулалар саны мына формулалармен анықталады:
заттың салыстырмалы массасы. Заттағы молекулалар саны мына формулалармен анықталады:  .
.


