РЕАКЦИИ ИЗОКУМАРИНОВ
По отношению к реагентам, способствующим гидролизу, изокумарины ведут себя как типичные лактоны. Так, они устойчивы к кислым и нейтральным реагентам [3], но взаимодействуют со щелочами, причем характер получающихся соединений зависит от заместителей, находящихся в положениях 3 и 4. З-Алкил- и 3-арилизокумарины образуют при этом о-карбоксибензил- кетоны (VIII), тогда как 3-хлоризокумарин (VI) дает гомофталевый ангидрид (IV). Сам изокумарин, по имеющимся сведениям, переходит в димерный виниловый эфир, а 5,6,7-триметоксиизокумарин (XXXV) —в w -окси-2,3,4-триметокси-6-карбоксистирол (XXXVI). Структура, приписываемая последнему соединению, кажется соответствующей действительности, поскольку о-карб- оксифенилацетальдегиды являются винилогами β-альдегидокислот [2].
3-Бензоил-7,8-диметоксиизокумарин (XXXVII) дает тот же α-дикетон (XXXVIII), который образуется при кипячении фенацилового эфира опиано- вой кислоты с натрием [1].
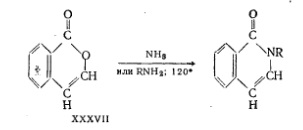
При взаимодействии со щелочью 4-карбоксиизокумарин образует муравьиную и гомофталевую кислоты. Обработка изокумаринов аммиаком или первичными аминами приводит к образованию изокарбостирилов [7].
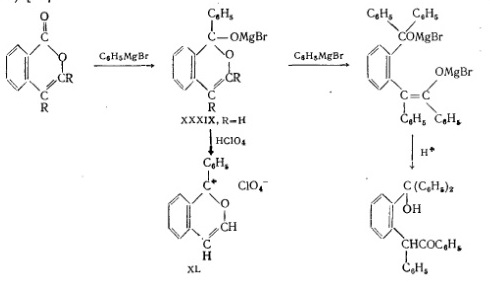
Реакции присоединения у изокумаринов протекают нормально; так, изокумарины могут присоединить 1 или 2 моля [20] магнийорганического соединения в зависимости от соотношения обоих реагентов. Продукт взаимодействия эквимолекулярных количеств изокумарина и бромистого фенилмагния (XXXIX) при обработке хлорной кислотой образует соль изобензопирилия (ХЬ) [19].
Изокумарин присоединяет бром, образуя дибромид. Продукт присоединения брома к З-бензоил-7,8-Диметоксиизокумарину неустойчив. Имеются сведения о том, что 3-хлоризокумарин (VI) устойчив к действию муравьиной и иодистоводороднон кислот, цинка и уксусной кислоты, а также растворов иодистого натрия и перманганата калия в ацетоне.
СОДЕРЖАНИЕ В ПРИРОДЕ Для бергенина- соединения, выделенного из корней различных видов растений семейства на основании изучения его химических свойств предложена следующая формула [20]:
ЛИТЕРАТУРА 1. Whitmоге, Сооneу, J.Am. Chem. Soc., 66, I2?7 (1944). 2. Dieckmann, Ber., 47, 1428 (1914). 3. Davies, Poole, J. Chem. Soc.,»928, 1616. 4. Buu-Hoi, Bull. soc. chim. France, (51. II, 338 (1941). 5. G r a e b c, Trumpy, Bcr., 31. 375 (1898). 6. H о г с n u, Jacques, Bull. soc. chim. France, 1048, 53. 7. a) Dieскmann, Mtiser, Ber., 41, 3253 (1908): 8. Nightingale, French, J. Org. Chem., 10, 533 (1945). 9. J о h n s t о n, et al„ J. Org. Chem.. 13. 477 (1948). 10. H. H.Воронцов, Л. H. Богусевич, ЖОХ, 10, 2014 (1940). 11. Fiеsсг, Ресhсt, J. Am. Chem. Soc., 68. 2577 (1946). 12. Nogami, J. Pharm. Soc. Japan, 61, 24 (1941). 13. Zincк e, Bcr., 25, 1493 (1895). 14. J о w с t t, P у m a n, J. Chem. Soc., 91. 92 (1907). 15. Bamberger. Kitschcld, Bcr., 25, 892 (1892). 16. Gabriel, Ber., 18, 2445, 3471 (1885). 17. N о g a m i, J. Pharm. Soc. Japan, 61, 21 (1941). 18. G a b r i*e I, Bcr., 36, 570 (1903). 19. W a nag, Wilbc, Bcr., 71, 1448 (1938). 20. Bain, Per к in, Robinson, J. Chem. Soc.. 105, 2392(1914).
|