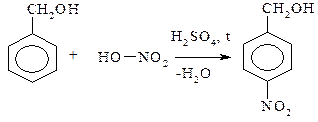Химические свойства. I. Кислотно-оснóвные свойства
I. Кислотно-оснóвные свойства. Спирты – слабые амфотерные соединения. 1. Взаимодействие с натрием (кислотные свойства) 2С2H5–ОН + 2Nа ® 2 С2H5–ОNа + Н2 этилат натрия Алкоголяты легко гидролизуются, что показывает – спирты более слабые кислоты, чем вода: С2H5– ОNа + НОН ® С2H5–ОН + NаОН 2. Взаимодействие с сильной кислотой НС1 (основные свойства). Оснóвным центром в спиртах является атом О, обладающий неподелённой парой электронов. При действии на спирты сильными кислотами происходит присоединение Н+ к атому кислорода группы ОН и образуется неустойчивый алкилоксониевый ион:
II. Реакции SN по гр. –ОН Гр. -ОН является плохоуходящей группой (связь мало полярна), поэтому большинство реакций проводят в кислой среде. Механизм р-ции:
1. Взаимодействие с галогеноводородами: Если реакция идет с галогеноводородами, то присоединяться будет галогенид-ион: СН3-СН2 - ОН + НСl ® СН3-СН2Сl + Н2О 2. Реакция алкилирования (введение алкила R в молекулу). Заместить –ОН гр. на галоген можно при действии РСl3, РСl5 и SОСl2, например: С2Н5ОН + РСl5 → С2Н5Сl + HCl + POCl3 С2Н5ОН + SOСl2 → С2Н5Сl + HCl + SO2 По такому механизму легче реагируют третичные спирты. III. Реакции SЕ. К ним относятся реакции взаимодействия спиртов с органическими и минеральными кислотами с образованием сложных эфиров: 1. Взаимодействие с уксусной кислотой.
этиловый эфир уксусной кислоты 2.
этилнитрат
IV. Реакции Е (отщепления, или элиминирования) Эти реакции конкурируют с реакциями SN.
При избытке Н2SО4 и более высокой температуре, чем в случае реакции образования простых эфиров, идет регенерация катализатора и образуется алкен: СН3-СН2+ + НSО4- ® СН2 = СН2 + Н2SО4
Легче идет реакция SE для третичных спиртов, труднее для вторичных и первичных, т.к. в последних случаях образуется менее стабильные катионы. В данных реакциях выполняется правило А. Зайцева: «При дегидратации спиртов атом Н отщепляется от соседнего атома С с меньшим содержанием атомов Н».
Бутанол-2 бутен - 2 В организме гр. –ОН превращается в легкоуходящую путем образования эфиров с Н3РО4:
V. Реакции окисления 1. Первичные и вторичные спирты окисляются СuО, растворами КМnО4, К2Сr2О7 при нагревании с образованием соответствующих карбонилсодержащих соединений:

 СН3-СН2- СН3-СН2- 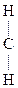 -ОН + О -ОН + О 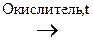 СН3-CH2- СН3-CH2- 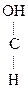 -ОН -ОН 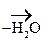 СН3-СН2- СН3-СН2- 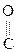 -Н -Н
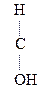 - СН3 + О - СН3 + О 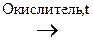 СН3- СН3- 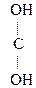 - СН3 - СН3 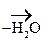 СН3- СН3- 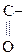 СН3 СН3
Ацетон (кетон) 5CH3OH + 6KMnO4 + 9H2SO4 → 5CO2↑ + 6MnSO4 + K2SO4 + 19H2O 5C2H5OH + 4KMnO4 + 6H2SO4 → 5CH3COOH + 4MnSO4 + 2K2SO4 + 11H2O Окисление спиртов под действием дихроматов натрия или калия является качественной реакцией. В результате взаимодействия спирт окисляется, а дихромат – ион восстанавливается до Cr+3, в результате чего оранжевое окрашивание переходит в сине-зеленое. Cr2O72- + 14H+ + 6 ẻ → 2Cr3+ + 7H2O оранжевый сине-зеленый
на холоду протекает реакция по уравнению: 3С2Н5ОН + 2K2Cr2O7 + 8H2SO4 → 3CH3COOH + 2Cr2(SO4)3 + 2K2SO4 + 11H2O При нагревании: 3С2Н5ОН + K2Cr2O7 + 4H2SO4 → 3CH3COH + Cr2(SO4)3 + K2SO4 + 6H2O
2. Третичные спирты окисляются с трудом. К реакциям окисления относятся и реакции дегидрирования: СН3 - 3. Спирты горят: С2Н6О + 2О2 → 2СО2 + 3Н2О
VI. По радикалу (R) протекают реакции, характерные для соответствующих углеводородов (УВ). В случае предельных – SR, непредельных – АN, ароматических – SЕ: 1. Реакции по α- углеродному атому с галогенами: СН3-СН2-ОН + 3Вr2 Этанол Нарколан 2. Реакции с галогенами в непредельных спиртах: СН2 = СН-СН2-ОН + Вr2 Аллиловый спирт 2,3- Дибромпропанол 3. Реакции по ароматическому кольцу:
Бензиловый спирт n-Нитрофенилметанол
|

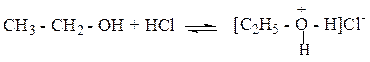 Этилоксоний хлорид
Этилоксоний хлорид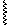 СН3-СН2-ОН + Н+ ® СН3-СН2-
СН3-СН2-ОН + Н+ ® СН3-СН2- 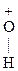 -Н ® СН3-СН2+ + Н2О
-Н ® СН3-СН2+ + Н2О С2H5 – О Н + Н О –
С2H5 – О Н + Н О – 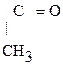
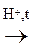 СН3 – О –
СН3 – О – 
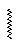 СН3-СН2-ОН + Н+
СН3-СН2-ОН + Н+ 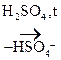 СН3-СН2-
СН3-СН2- 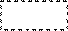
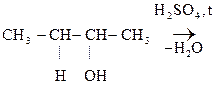 СН3-СН = СН -СН3
СН3-СН = СН -СН3 СН3-СН2-ОН + НО–РО3Н2
СН3-СН2-ОН + НО–РО3Н2 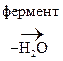 СН3-СН2-ОРО3Н2
СН3-СН2-ОРО3Н2


 СН3 -
СН3 - 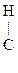 = О + Н2
= О + Н2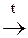 СВr3-СН2-ОН + 3НВr
СВr3-СН2-ОН + 3НВr СН2 Вr–СНВr–СН2ОН
СН2 Вr–СНВr–СН2ОН