Обработка результатов эксперимента
1. Вычислить количество тепла, поглощенного (выделенного) при растворении:
где 2. Вычислить тепловой эффект растворения 1 моль соли:
где n соли – число моль использованной в опыте соли; точное число моль вычислить по соотношению массы соли по протоколу и молярной массы соли:
3. Оценить погрешность опыта:
D solvH теор – рассчитать по закону Гесса исходя из стандартных теплот образования солей и ионов, которые являются справочными данными. Пример расчета теплоты растворения соли 1. Составить уравнение реакции растворения соли:
2. Записать закон Гесса применительно к данной реакции:
символ «aq» означает ион в водном растворе, символ «s» означает твердое вещество. 3. Подставить численные значения и произвести расчет. Содержание отчета по лабораторной работе 1. Название работы 2. Цель работы 3. Ход эксперимента 4. Экспериментальные данные по протоколу 5. Обработка экспериментальных данных 6. Выводы (в выводах – об тепловых эффектах процесса растворения в целом и о тепловых эффектах стадий растворения соли) Содержание Введение. 3 Правила работы в лаборатории. 5 Определение эквивалентной массы.. 8 Лабораторная работа № 1. Определение эквивалентной массы металла 10 Лабораторная работа № 2. Определение эквивалента карбоната натрия 14 Лабораторная работа № 3. Исследование скорости химических реакций и химического равновесия 19 Лабораторная работа № 4. Приготовление раствора и определение его концентрации 36 Лабораторная работа № 5. Исследование реакций в растворах электролитов 45 Лабораторная работа № 6. Исследование гидролиза солей. 56 Лабораторная работа № 7. Приготовление буферного раствора. 66 Лабораторная работа № 8. Исследование растворимости солей. 76 Лабораторная работа № 9. Исследование окислительно-восстановительных реакций 85 Лабораторная работа № 10. Исследование комплексных соединений 97 Лабораторная работа № 11. Определение энтальпии реакции нейтрализации 111 Лабораторная работа № 12. Определение теплоты растворения соли 117 Содержание. 122
|

 ,
, – удельная теплоемкость раствора, упрощенно принимаемая равной теплоемкости воды, которая составляет 4,18 Дж/г·K.
– удельная теплоемкость раствора, упрощенно принимаемая равной теплоемкости воды, которая составляет 4,18 Дж/г·K. ,
, .
. ,
,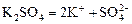 .
. ,
,


