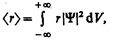Максвелл ввел понятие полного тока,равного сумме токов проводимости (а также конвекционных токов) и смещения.Плотность полного тока 15 страница
Придавая n различные целочисленные значения, получим для атома водорода (Z = 1), согласно формуле (212.3), возможные уровни энергии, схематически представленные на рис. 294. Энергия атома водорода с увеличением n возрастает и энергетические уровни сближаются к границе, соответствующей значению n = ¥. Атом водорода обладает, таким образом, минимальной энергией (E 1 = –13,55 эВ) при n = 1 и максимальной (Е ¥ = 0) при n = ¥. Следовательно, значение Е ¥ = 0 соответствует ионизации атома (отрыву от него электрона). Согласно второму постулату Бора (см. (210.2)), при переходе атома водорода (Z= 1) из стационарного состояния л в стационарное состояние т с меньшей энергией испускается квант
откуда частота излучения
где R = mee 4/(8 h 3 Воспользовавшись при вычислении R современными значениями универсальных постоянных, получим величину, совпадающую с экспериментальным значением постоянной Ридберга в эмпирических формулах для атома водорода (см. § 209). Это совпадение убедительно доказывает правильность полученной Бором формулы (212.3) для энергетических уровней водородоподобной системы. Подставляя, например, в формулу (212.4) т= 1 и п= 2, 3, 4,..., получим группу линий, образующих серию Лаймана (см. § 209) и соответствующих переходам электронов с возбужденных уровней (n = 2, 3, 4,...) на основной (m = l). Аналогично, при подстановке m = 2, 3, 4, 5, 6 и соответствующих им значений n получим серии Бальмера, Пашена, Брэкета, Пфунда и Хэмфри (часть из них схематически представлена на рис. 294), описанные в § 209. Следовательно, по теории Бора, количественно объяснившей спектр атома водорода, спектральные серии соответствуют излучению, возникающему в результате перехода атома в данное состояние из возбужденных состояний, расположенных выше данного.
Спектр поглощения атома водорода является линейчатым, но содержит при нормальных условиях только серию Лаймана. Он также объясняется теорией Бора. Так как свободные атомы водорода обычно находятся в основном состоянии (стационарное состояние с наименьшей энергией при n = 1), то при сообщении атомам извне определенной энергии могут наблюдаться лишь переходы атомов из основного состояния в возбужденные (возникает серия Лаймана). Теория Бора была крупным шагом в развитии атомной физики и явилась важным этапом в создании квантовой механики. Однако эта теория обладает внутренними противоречиями (с одной стороны, применяет законы классической физики, а с другой — основывается на квантовых постулатах). В теории Бора рассмотрены спектры атома водорода и водородоподобных систем и вычислены частоты спектральных линий, однако эта теория не смогла объяснить интенсивности спектральных линий и ответить на вопрос: почему совершаются те или иные переходы? Серьезным недостатком теории Бора была невозможность описания с ее помощью спектра атома гелия — одного из простейших атомов, непосредственно следующего за атомом водорода.
Глава 28 Элементы квантовой механики § 213. Корпускулярно-волновой дуализм свойств вещества Французский ученый Луи де Бройль (1892—1987), осознавая существующую в природе симметрию и развивая представления о двойственной корпускулярно-волновой природе света, выдвинул в 1923 г. гипотезу об универсальности корпускулярно-волнового дуализма. Де Бройль утверждал, что не только фотоны, но и электроны и любые другие частицы материи наряду с корпускулярными обладают также волновыми свойствами. Итак, согласно де Бройлю, с каждым микрообъектом связываются, с одной стороны, корпускулярные характеристики — энергия Е и импульс p, а с другой — волновые характеристики — частота n и длина волны l. Количественные соотношения, связывающие корпускулярные и волновые свойства частиц, такие же, как для фотонов:
Смелость гипотезы де Бройля заключалась именно в том, что соотношение (213.1) постулировалось не только для фотонов, но и для других микрочастиц, в частности для таких, которые обладают массой покоя. Таким образом, любой частице, обладающей импульсом, сопоставляют волновой процесс с длиной волны, определяемой по формуле де Бройля:
Это соотношение справедливо для любой частицы с импульсом р. Вскоре гипотеза де Бройля была подтверждена экспериментально. В 1927 г. американские физики К. Дэвиссон (1881—1958) и Л. Джермер (1896—1971) обнаружили, что пучок электронов, рассеивающийся от естественной дифракционной решетки — кристалла никеля, — дает отчетливую дифракционную картину. Дифракционные максимумы соответствовали формуле Вульфа — Брэггов (182.1), а брэгговская длина волны оказалась в точности равной длине волны, вычисленной по формуле (213.2). В дальнейшем формула де Бройля была подтверждена опытами П. С. Тартаковского и Г. Томсона, наблюдавших дифракционную картину при прохождении пучка быстрых электронов (энергия»50 кэВ) через металлическую фольгу (толщиной»1 мкм). Так как дифракционная картина исследовалась для потока электронов, то необходимо было доказать, что волновые свойства присущи не только потоку большой совокупности электронов, но и каждому электрону в отдельности. Это удалось экспериментально подтвердить в 1948 г. российскому физику В. А. Фабриканту (р. 1907). Он показал, что даже в случае столь слабого электронного пучка, когда каждый электрон проходит через прибор независимо от других (промежуток времени между двумя электронами в 104 раз больше времени прохождения электроном прибора), возникающая при длительной экспозиции дифракционная картина не отличается от дифракционных картин, получаемых при короткой экспозиции для потоков электронов, в десятки миллионов раз более интенсивных. Следовательно, волновые свойства частиц не являются свойством их коллектива, а присущи каждой частице в отдельности. Впоследствии дифракционные явления обнаружили также для нейтронов, протонов, атомных и молекулярных пучков. Это окончательно послужило доказательством наличия волновых свойств микрочастиц и позволило описывать движение микрочастиц в виде волнового процесса, характеризующегося определенной длиной волны, рассчитываемой по формуле де Бройля (213.2). Открытие волновых свойств микрочастиц привело к появлению и развитию новых методов исследования структуры веществ, таких,как электронография и нейтронография (см. § 182), а также к возникновению новой отрасли науки — электронной оптики (см. § 169). Экспериментальное доказательство наличия волновых свойств микрочастиц привело к выводу о том, что перед нами универсальное явление, общее свойство материи. Но тогда волновые свойства должны быть присущи и макроскопическим телам. Почему же они не обнаружены экспериментально? Например, частице массой 1 г, движущейся со скоростью 1 м/с, соответствует волна де Бройля с l = 6,62×10–31 м. Такая длина волны лежит за пределами доступной наблюдению области (периодических структур с периодом d»10–31 м не существует). Поэтому считается, что макроскопические тела проявляют только одну сторону своих свойств — корпускулярную — и не проявляют волновую. Представление о двойственной корпускулярно-волновой природе частиц вещества углубляется еще тем, что на частицы вещества переносится связь между полной энергией частицы e и частотой n волн де Бройля:
Это свидетельствует о том, что соотношение между энергией и частотой в формуле (213.3) имеет характер универсального соотношения, справедливогокак для фотонов, так и для любых других микрочастиц. Справедливость же соотношения (213.3) вытекает из согласия с опытом тех теоретических результатов, которые получены с его помощью в квантовой механике, атомной и ядерной физике. Подтвержденная экспериментально гипотеза да Бройля о корпускулярно-волновом дуализме свойств вещества коренным образом изменила представления о свойствах микрообъектов. Всем микрообъектам присущи и корпускулярные, и волновые свойства; в то же время любую из микрочастиц нельзя считать ни частицей, ни волной в классическом понимании. Современная трактовка корпускулярно-волнового дуализма может быть выражена словами академика В. А. Фока (1898—1974): «Можно сказать, что для атомного объекта существует потенциальная возможность проявлять себя, в зависимости от внешних условий, либо как волна, либо как частица, либо промежуточным образом. Именно в этой потенциальной возможности различных проявлений свойств, присущих микрообъекту, и состоит дуализм волна—частица. Всякое иное, более буквальное, понимание этого дуализма в вида какой-нибудь модели неправильно.» (в сб.: Философские вопросы современной физики. — М.: Изд-во АН СССР, 1959). § 214. Некоторые свойства волн да Бройля Рассмотрим свободно движущуюся со скоростью v частицу массой т. Вычислим для нее фазовую и групповую скорости волн да Бройля. Фазовая скорость, согласно (154.8),
(E = ћw и p=ћk, где k= 2 p/l— волновое число). Так как c>v, то фазовая скорость волн де Бройля больше скорости света в вакууме (фазовая скорость волн может быть как меньше, так и больше с в отличие от групповой скорости волн (см. § 155)). Групповая скорость, согласно (155.1),
Для свободной частицы
Следовательно, групповая скорость волн де Бройля равна скорости частицы. Групповая скорость фотона Волны да Бройля испытывают дисперсию (см. § 154). Действительно, подставив в выражение (214.1) v фаз =E/p формулу (40.7) Е= § 215. Соотношение неопределенностей Согласно двойственной корпускулярно-волновой природе частиц вещества, для описания микрочастиц используются то волновые, то корпускулярные представления. Поэтому приписывать им все свойства частиц и все свойства волн нельзя. Естественно, что необходимо внести некоторые ограничения в применении к объектам микромира понятий классической механики. В классической механике всякая частица движется по определенной траектории, так что в любой момент времени точно фиксированы ее координата и импульс. Микрочастицы из-за наличия у них волновых свойств существенно отличаются от классических частиц. Одно из основных различий заключается в том, что нельзя говорить о движении микрочастицы по определенной траектории и неправомерно говорить об одновременных точных значениях ее координаты и импульса. Это следует из корпускулярно-волнового дуализма. Так, понятие «длина волны в данной точке» лишено физического смысла, а поскольку импульс выражается через длину волны (см. (213.1)), то отсюда следует, что микрочастица с определенным импульсом имеет полностью неопределенную координату. И наоборот, если микрочастица находится в состоянии с точным значением координаты, то ее импульс является полностью неопределенным. В. Гейзенберг, учитывая волновые свойства микрочастиц и связанные с волновыми свойствами ограничения в их поведении, пришел в 1927 г. к выводу, что объект микромира невозможно одновременно с любой наперед заданной точностью характеризовать и координатой и импульсом. Согласно соотношению неопределенностей Гейзенберга, микрочастица (микрообъект) не может иметь одновременно и определенную координату (х, у, z), и определенную соответствующую проекцию импульса (рх, pу, pz), причем неопределенности этих величин удовлетворяют условиям
т. е. произведение неопределенностей координаты и соответствующей ей проекции импульса не может быть меньше величины порядка h. Из соотношения неопределенностей (215.1) следует, что, например, если микрочастица находится в состоянии с точным значением координаты (D x = 0), то в этом состоянии соответствующая проекция ее импульса оказывается совершенно неопределенной (D px ® ¥), и наоборот. Таким образом, для микрочастицы не существует состояний, в которых ее координаты и импульс имели бы одновременно точные значения. Отсюда вытекает и фактическая невозможность одновременно с любой наперед заданной точностью измерить координату и импульс микрообъекта. Поясним, что соотношение неопределенностей действительно вытекает из волновых свойств микрочастиц. Пусть поток электронов проходит через узкую щель шириной D х, расположенную перпендикулярно направлению их движения (рис. 295). Так как электроны обладают волновыми свойствами, то при их прохождении через щель, размер которой сравним с длиной волны де Бройля l электрона, наблюдается дифракция. Дифракционная картина, наблюдаемая на экране (Э), характеризуется главным максимумом, расположенным симметрично оси Y, и побочными максимумами по обе стороны от главного (их не рассматриваем, таккак основная доля интенсивности приходится на главный максимум).
До прохождения через щель электроны двигались вдоль оси Y, поэтому составляющая импульса рх= 0, так что D px =0, а координата х частицы является совершенно неопределенной. В момент прохождения электронов через щель их положение в направлении оси Х определяется с точностью до ширины щели, т. е. с точностью D х. В этот же момент вследствие дифракции электроны отклоняются от первоначального направления и будут двигаться в пределах угла 2 j (j — угол, соответствующий первому дифракционному минимуму). Следовательно, появляется неопределенность в значении составляющей импульса вдоль оси X, которая, как следует из рис. 295 и формулы (213.1), равна
Для простоты ограничимся рассмотрением только тех электронов, которые попадают на экран в пределах главного максимума. Из теории дифракции (см. § 179) известно, что первый минимум соответствует углу j, удовлетворяющему условию
где D х — ширина щели, а l — длина волны де Бройля. Из формул (215.2) и (215.3) получим
где учтено, что для некоторой, хотя и незначительной, части электронов, попадающих за пределы главного максимума, величина D рx ³ р sin j. Следовательно, получаем выражение
т. е. соотношение неопределенностей (215.1). Невозможность одновременно точно определить координату и соответствующую проекцию импульса не связана с несовершенством методов измерения или измерительных приборов, а является следствием специфики микрообъектов, отражающей особенности их объективных свойств, а именно двойственной корпускулярно-волновой природы. Соотношение неопределенностей получено при одновременном использовании классических характеристик движения частицы (координаты, импульса) и наличия у нее волновых свойств. Так как в классической механике принимается, что измерение координаты и импульса может быть произведено с любой точностью, то соотношение неопределенностей является, таким образом, квантовым ограничением применимости классической механики к микрообъектам. Соотношение неопределенностей, отражая специфику физики микрочастиц, позволяет оценить, например, в какой мере можно применять понятия классической механики к микрочастицам, в частности, с какой степенью точности можно говорить о траекториях микрочастиц. Известно, что движение по траектории характеризуется в любой момент времени определенными значениями координат и скорости. Выразим соотношение неопределенностей (215.1) в виде
Из этого выражения следует, что чем больше масса частицы, тем меньше неопределенности ее координаты и скорости и, следовательно, с тем большей точностью можно применять к этой частице понятие траектории. Так, например, уже для пылинки массой 10–12 кг и линейными размерами 10–6 м, координата которой определена с точностью до 0,01 ее размеров (D х = 10–8 м), неопределенность скорости, по (215.4), D vx = 6,62×10–34/(10–8×10–12) м/с = 6,62×10–14 м/с, т. е. не будет сказываться при всех скоростях, с которыми пылинка может двигаться. Таким образом, для макроскопических тел их волновые свойства не играют никакой роли; координата и скорость макротел могут быть одновременно измерены достаточно точно. Это означает, что для описания движения макротел с абсолютной достоверностью можно пользоваться законами классической механики. Предположим, пучок электронов движется вдоль оси х со скоростью v =108 м/с, определяемой с точностью до 0,01% (D vx» 104 м/с). Какова точность определения координаты электрона? По формуле (215.4),
т. е. положение электрона может быть определено с точностью до тысячных долей миллиметра. Такая точность достаточна, чтобы можно было говорить о движении электронов по определенной траектории, иными словами, описывать их движение законами классической механики. Применим соотношение неопределенностей к электрону, движущемуся в атоме водорода. Допустим, что неопределенность координаты электрона D x» 10–10 м (порядка размеров самого атома, т. е. можно считать, что электрон принадлежит данному атому). Тогда, согласно (215.4), D vx =6,62 ×;10–34 / (9,11×10–31 ×10–10) = 7,27×106 м/с. Используя законы классической физики, можно показать, что при движении электрона вокруг ядра по круговой орбите радиуса»0,5×10–10 м его скорость v» 2,3×106 м/с. Таким образом, неопределенность скорости в несколько раз больше самой скорости. Очевидно, что в данном случае нельзя говорить о движении электрона в атоме по определенной траектории, иными словами, для описания движения электрона в атоме нельзя пользоваться законами классической физики. В квантовой теории рассматривается также соотношение неопределенностей для энергии Е и времени t, т. е. неопределенности этих величии удовлетворяют условию
Подчеркнем, что D Е — неопределенность энергии некоторого состояния системы, D t — промежуток времени, в течение которого оно существует. Следовательно, система, имеющая среднее время жизни D t, не может быть охарактеризована определенным значением энергии; разброс энергии D E = h /D t возрастает с уменьшением среднего времени жизни. Из выражения (215.5) следует, что частота излученного фотона также должна иметь неопределенность D n = D E / h, т. е. линии спектра должны характеризоваться частотой, равной n ± D E / h..Опыт действительно показывает, что все спектральные линии размыты; измеряя ширину спектральной линии, можно оценить порядок времени существования атома в возбужденном состоянии. § 216. Волновая функция и ее статистический смысл Экспериментальное подтверждение идеи де Бройля об универсальности корпускулярно-волнового дуализма, ограниченность применения классической механики к микрообъектам, диктуемая соотношением неопределенностей, а также противоречие целого ряда экспериментов с применяемыми в начале XX в. теориями привели к новому этапу развития квантовой теории — созданию квантовой механики, описывающей законы движения и взаимодействия микрочастиц с учетом их волновых свойств. Ее создание и развитие охватывает период с 1900 г. (формулировка Планком квантовой гипотезы; см. § 200) до 20-х годов XX в.; оно связано прежде всего с работами австрийского физика Э. Шредингера (1887—1961), немецкого физика В. Гейзенберга и английского физика П. Дирака (1902—1984). На данном этапе развития возникли новые принципиальные проблемы, в частности проблема физической природы волн де Бройля. Для выяснения этой проблемы сравним дифракцию световых волн и микрочастиц. Дифракционная картина, наблюдаемая для световых волн, характеризуется тем, что в результате наложения дифрагирующих волн друг на друга в различных точках пространства происходит усиление или ослабление амплитуды колебаний. Согласно волновым представлениям о природе света, интенсивность дифракционной картины пропорциональна квадрату амплитуды световой волны. По представлениям фотонной теории, интенсивность определяется числом фотонов, попадающих в данную точку дифракционной картины. Следовательно, число фотонов в данной точке дифракционной картины задается квадратом амплитуды световой волны, в то время как для одного фотона квадрат амплитуды определяет вероятность попадания фотона в ту или иную точку. Дифракционная картина, наблюдаемая для микрочастиц, также характеризуется неодинаковым распределением потоков микрочастиц, рассеянных или отраженных по различным направлениям, — в одних направлениях наблюдается большее число частиц, чем в других. Наличие максимумов в дифракционной картине с точки зрения волновой теории означает, что эти направления соответствуют наибольшей интенсивности волн де Бройля. С другой стороны, интенсивность волн де Бройля оказывается больше там, где имеется большее число частиц, т. е. интенсивность волн де Бройля в данной точке пространства определяет число частил, попавших в эту точку. Таким образом, дифракционная картина для микрочастиц является проявлением статистической (вероятностной) закономерности, согласно которой частицы попадают в те места, где интенсивность волн де Бройля наибольшая. Необходимость вероятностного подхода к описанию микрочастиц является важнейшей отличительной особенностью квантовой теории. Можно ли волны де Бройля истолковывать как волны вероятности, т. е. считать, что вероятность обнаружить микрочастицу в различных точках пространства меняется по волновому закону? Такое толкование волн де Бройля уже неверно хотя бы потому, что тогда вероятность обнаружить частицу в некоторых точках пространства может быть отрицательна, что не имеет смысла. Чтобы устранить эти трудности, немецкий физик М. Борн (1882—1970) в 1926 г. предположил, что по волновому закону меняется не сама вероятность, а величина, названная амплитудой вероятности и обозначаемая Y(х, у, z, t). Эту величину называют также волновой функцией (или Y-функцией). Амплитуда вероятности может быть комплексной, и вероятность W пропорциональна квадрату ее модуля:
(|Y|2=YY*, Y * — функция, комплексно сопряженная с Y). Таким образом, описание состояния микрообъекта с помощью волновой функции имеет статистический, вероятностный характер: квадрат модуля волновой функции (квадрат модуля амплитуды волн де Бройля) определяет вероятность нахождения частицы в момент времени t в области с координатами х и x+dx, у и y+dy, z и z+dz. Итак, в квантовой механике состояние микрочастиц описывается принципиально по-новому — с помощью волновой функции, которая является основным носителем информации об их корпускулярных и волновых свойствах. Вероятность нахождения частицы в элементе объемом d V равна
Величина
(квадрат модуля Y-функции) имеет смысл плотности вероятности, т. е. определяет вероятность нахождения частицы в единичном объеме в окрестности точки с координатами х, у, z. Таким образом, физический смысл имеет не сама Y-функция, а квадрат ее модуля |Y|2, которым задается интенсивность волн де Бройля. Вероятность найти частицу в момент времени t в конечном объеме V, согласно теореме сложения вероятностей, равна
Так как |Y|2d V определяется как вероятность, то необходимо волновую функцию Y нормировать так, чтобы вероятность достоверного события обращалась в единицу, если за объем V принять бесконечный объем всего пространства. Это означает, что при данном условии частица должна находиться где-то в пространстве. Следовательно, условие нормировки вероятностей
где данный интеграл (216.3) вычисляется по всему бесконечному пространству, т. е. по координатам х, у, z от –¥ до ¥. Таким образом, условие (216.3) говорит об объективном существовании частицы в пространстве. Чтобы волновая функция являлась объективной характеристикой состояния микрочастиц, она должна удовлетворять ряду ограничительных условий. Функция Y, характеризующая вероятность обнаружения действия микрочастицы в элементе объема, должна быть конечной (вероятность не может быть больше единицы), однозначной (вероятность не может быть неоднозначной величиной) и непрерывной (вероятность не может изменяться скачком). Волновая функция удовлетворяет принципу суперпозиции: если система может находиться в различных состояниях, описываемых волновыми функциями Y1, Y2,..., Y n,... то она также может находиться в состоянии Y, описываемом линейной комбинацией этих функций:
где С n (n =1, 2,...)—произвольные, вообще говоря, комплексные числа. Сложение волновых функций (амплитуд вероятностей), а не вероятностей (определяемых квадратами модулей волновых функций) принципиально отличает квантовую теорию от классической статистической теории, в которой для независимых событий справедлива теорема сложения вероятностей. Волновая функция Y, являясь основной характеристикой состояния микрообъектов, позволяет в квантовой механике вычислять средние значения физических величин, характеризующих данный микрообъект. Например, среднее расстояние á r ñ электрона от ядра вычисляют по формуле
где интегрирование производится, как и в случае (216.3). § 217. Общее уравнение Шредингера. Уравнение Шредингера для стационарных состояний
|


 (212.4)
(212.4) ).
).
 (213.1)
(213.1) (213.2)
(213.2) (213.3)
(213.3) (214.1)
(214.1)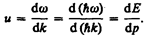
 (см. (40.7)) и
(см. (40.7)) и
 т. е. равна скорости самого фотона.
т. е. равна скорости самого фотона. , увидим, что скорость волн де Бройля зависит от длины волны. Это обстоятельство сыграло в свое время большую роль в развитии положений квантовой механики. После установления корпускулярно-волнового дуализма делались попытки связать корпускулярные свойства частиц с волновыми и рассматривать частицы как «узкие» волновые пакеты (см. § 155), «составленные» из волн де Бройля. Это позволяло как бы отойти от двойственности свойств частиц. Такая гипотеза соответствовала локализации частицы в данный момент времени в определенной ограниченной области пространства. Аргументом в пользу этой гипотезы являлось и то, что скорость распространения центра пакета (групповая скорость) оказалась, как показано выше, равной скорости частицы. Однако подобное представление частицы в виде волнового пакета (группы волн де Бройля) оказалось несостоятельным из-за сильной дисперсии волн де Бройля, приводящей к «быстрому расплыванию» (примерно 10–26 с!) волнового пакета или даже разделению его на несколько пакетов.
, увидим, что скорость волн де Бройля зависит от длины волны. Это обстоятельство сыграло в свое время большую роль в развитии положений квантовой механики. После установления корпускулярно-волнового дуализма делались попытки связать корпускулярные свойства частиц с волновыми и рассматривать частицы как «узкие» волновые пакеты (см. § 155), «составленные» из волн де Бройля. Это позволяло как бы отойти от двойственности свойств частиц. Такая гипотеза соответствовала локализации частицы в данный момент времени в определенной ограниченной области пространства. Аргументом в пользу этой гипотезы являлось и то, что скорость распространения центра пакета (групповая скорость) оказалась, как показано выше, равной скорости частицы. Однако подобное представление частицы в виде волнового пакета (группы волн де Бройля) оказалось несостоятельным из-за сильной дисперсии волн де Бройля, приводящей к «быстрому расплыванию» (примерно 10–26 с!) волнового пакета или даже разделению его на несколько пакетов. (215.1)
(215.1)
 (215.2)
(215.2) (215.3)
(215.3)

 (215.4)
(215.4)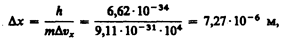
 (215.5)
(215.5) (216.1)
(216.1) (216.2)
(216.2)

 (216.3)
(216.3)