Лабораторна робота № 202. ДОСЛІДЖЕННЯ ЗАЛЕЖНОСТІ КОЕФІЦІЄНТА В’ЯЗКОСТІ РІДИНИ ВІД ТЕМПЕРАТУРИ
Завдання: визначити коефіцієнт в’язкості гліцерину за різних температур в інтервалі 18–40° С, побудувати графік залежності h = f (t °С) і розрахувати енергію активації молекули. Приладдя: віскозиметр Хепплера з досліджуваною рідиною, скляною кулькою і термометром; лабораторний автотрансформатор (ЛАТР); секундомір. Теоретичний матеріал, який необхідно засвоїти під час підготовки до роботи: Див. лабораторну роботу №201.
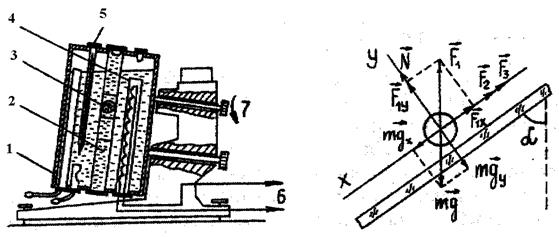
Опис установки. Віскозиметр Хепплера (рис. 2) складається зі скляного термостата 1, заповненого водою, всередині якого розміщена трубка 2 з досліджуваною рідиною і скляною кулькою 3. Трубка 2 нахилена під кутом 10° до вертикалі. В термостаті розміщений нагрівник 4 і термометр 5. Живлення нагрівника (не більше 80 В) забезпечують за допомогою ЛАТР 6. Скляний термостат 1 можна обертати навколо осі 00 і фіксувати гвинтом 7 у двох положеннях – прямому й оберненому. Це дає змогу виконувати багаторазові експерименти з досліджуваною рідиною, не виймаючи з неї скляної кульки.
Ідея роботи та виведення робочої формули. Визначення коефіцієнта в’язкості рідини за допомогою віскозиметра Хепплера ґрунтується на вимірюванні часу руху скляної кульки на заданому відрізку шляху у в’язкій рідині, температуру якої можна змінювати. Під час руху кульки на неї діють такі сили: сила тяжіння сила Архімеда Сили, які діють на кульку, показані на рис. 3. Якщо осі Х та У вибрати так, як показано на рис. 3, то, розклавши сили F1 і mg на складові, рівняння руху кульки (за умови, що її рух рівномірний) можна записати у виглядi
або Врахуємо, що швидкість кульки V можна виразити як v=l/t, (3) де l – відстань, яку проходить кулька; t – час руху. Із (2) і (3) отримаємо
або h = b (r 1- r 0) t, (4) де b є сталою приладу. Вираз (4) – це робоча формула цієї лабораторної роботи. Відомо, що коефіцієнт в’язкості залежить від температури. Для газів цю залежність визначає таке співвідношення:
де r – густина; Т – абсолютна температура газу; m – маса молекули; ` l – середня довжина вільного пробігу. Із (5) можна бачити, що для газів h збільшується з підвищенням температури. В’язкість рідин, на відміну від газів, зменшується з підвищенням температури. Це зумовлено різним характером руху молекул у рідинах і газах. Перехід молекули рідини від коливального до поступального руху (перехід в інше положення рівноваги) потребує певної енергії активації. Тому коефіцієнт в’язкості рідини залежить від температури так:
де Е – енергія активації молекули; k – стала Больцмана; Т – абсолютна температура; h 0– стала, що має розмірність коефіцієнта в’язкості. Якщо експериментально визначити коефіцієнти в’язкості рідини h 1i h 2 за різних температур Т1 і Т2, то на підставі (6) легко отримати співвідношення для визначення енергії активації молекул рідини:
|

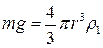 ,
, , сила тертя до стінки трубки F2=mN, сила опору рідини рухові кульки F3, яка за формулою Стокса дорівнює 6prhv, де r – радіус кульки; r1 і r0 – густина матеріалу кульки і рідини; m – коефіцієнт тертя; N – сила реакції; h – коефіцієнт в’язкості рідини; v – швидкість руху кульки.
, сила тертя до стінки трубки F2=mN, сила опору рідини рухові кульки F3, яка за формулою Стокса дорівнює 6prhv, де r – радіус кульки; r1 і r0 – густина матеріалу кульки і рідини; m – коефіцієнт тертя; N – сила реакції; h – коефіцієнт в’язкості рідини; v – швидкість руху кульки.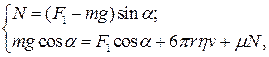 (1)
(1) . (2)
. (2)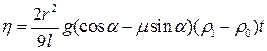 ,
,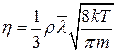 , (5)
, (5)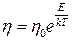 ,(6)
,(6)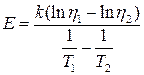 . (7)
. (7)


