Получение цементного клинкера
Исходные сырьевые материалы в соответствующих расчету пропорциях измельчаются в лабораторной мельнице и тщательно перемешиваются. Готовую сырьевую смесь увлажняют до 5-7%, после чего под давлением 20-30 МПа прессуют образцы-цилиндры диаметром и высотой 2 см. Образцы-цилиндры высушивают в сушильном шкафу при 120°С в течение 2-3 ч, затем обжигают в печи при температуре 1100-1500°С. После обжига образцы охлаждают до комнатной температуры. Состав сырьевой смеси и степень ее измельчения, режим обжига (температура, продолжительность и кратность обжига) и охлаждения указываются преподавателем. Контроль качества обжига клинкера, как правило, осуществляется путем определения содержания свободного оксида кальция. Определение свободного оксида кальция этилово-глицератным методом. Этилово-глицератный метод основан на взаимодействии несвязанной извести клинкера с глицерином в спиртовом растворе с образованием глицерата кальция.
СаО + СН - ОН ® СН - ОН Са + Н2О СН2 - ОН СН2 - О Затем глицерат кальция титруют спиртовым раствором бензойной кислоты или уксуснокислого аммония по реакции:
СН - ОН Са + 2С6Н5СООН ® СН - ОН + Са (С6Н5СОО)2 СН2 - О СН2 - ОН
СН - ОН Са + 2СН3СООNН4 ® СН - ОН + Са (СН3СОО)2 + 2NH3 СН2 - О СН2 - ОН Из всех качественных методов определения свободного оксида кальция этилово-глицератный метод наиболее надежный. Для определения СаОсв пробу клинкера массой 3-5 г дробят в фарфоровой ступке, затем помещают ее в агатовую ступку и растирают до полного прохождения через сито № 008. Навеску не более 0,5 г измельченного порошка отвешивают на аналитических весах с точностью 0,0002 г, высыпают в коническую колбу емкостью 250 мл, добавляют 30 мл спиртоглицеринового раствора и несколько капель спиртового раствора фенолфталеина. Содержимое колбы перемешивают, присоединяют к колбе обратный холодильник, устанавливают ее на электрическую плитку и кипятят в течение 10 мин. Скорость появления розового окрашивания раствора зависит от количества содержащегося свободного оксида кальция. Если после получасового непрерывного кипячения окраска не появилась, можно считать, что СаОсв отсутствует. При появлении розового окрашивания кипящую жидкость примерно через каждые 10 мин кипячения титруют раствором бензойной кислоты или уксуснокислого аммония до исчезновения розового окрашивания. Нагревание и титрование повторяют до тех пор, пока не прекратится появление розового окрашивания после 15-20 мин кипячения. Тогда титрование можно считать законченным. Содержание свободной СаО в процентах рассчитывают по формуле
где V - количество раствора бензойной кислоты или уксуснокислого аммония, пошедшее на титрование, мл; Т СаО - количество СаО, соответствующее 1 мл 0,1 н раствора бензойной кислоты или уксуснокислого аммония, г (Т СаО = 0,0028); m - масса навески клинкера, г. Определение свободного оксида кальция сахаратным методом. Наиболее простым является сахаратный метод определения свободного оксида кальция в клинкере. Он применяется при высоком содержании свободного оксида кальция, т. е. в том случае, когда другие методы требуют весьма длительного времени определения. Однако следует отметить, что сахаратный метод по сравнению с вышеизложенным менее точен. Навеску не более 0,25 г тонкоизмельченного (проход через сито № 008) клинкера помещают в коническую колбу емкостью 250 мл и обрабатывают 50 мл 10%-ным раствором сахара. Содержимое колбы перемешивают, после чего производят титрование 1 н раствором кислоты в присутствии фенолфталеина. Содержание свободного СаО в процентах определяют по формуле:
где V - количество раствора соляной кислоты, пошедшее на титрование, мл; k - поправка к титру 1 н HCl; 0,02804 - количество оксида кальция, соответствующее 1 мл точно 1 н раствора соляной кислоты, г; m - масса навески клинкера, г.
|

 СН2 - ОН СН2 - О
СН2 - ОН СН2 - О СН2 - О СН2 - ОН
СН2 - О СН2 - ОН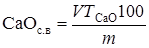 ,
,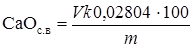 ,
,


