Влияние комплексообразования на растворимость
малорастворимых солей Многие комплексные соединения относятся к слабейшим из известных электролитов, и в соответствии с принципом Ле Шателье, и в случае их образования растворимость малорастворимых солей должна увеличиваться. Например, сравним растворимость CoS в воде и 1М водном растворе аммиака. Ионно-молекулярное уравнение этой реакции: CoS¯ + 6NH3 «[Co(NH3)6]2+ + S2–. K = [Co(NH3)62+]×[S2–]/[NH3]6 = ПрCoS/K1-6[Co(NH3)6]2+ = 4 . 10–21/10–5 ×10–15 Пренебрегая изменением концентрации аммиака (т.к. он в большом избытке) и учитывая, что [Co(NH3)62+] = [S2–], получим: [Co(NH3)62+]2/16 = 10–16, откуда [Co(NH3)62+] = 10–16 = 10–8 моль/дм3; очевидно, такой же будет растворимость CoS (моль/дм3). Растворимость CoS в воде Р =
|

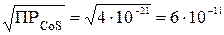 моль/дм3
моль/дм3


