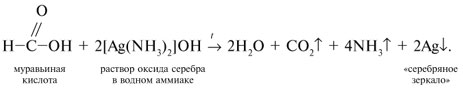Задание 1: Изучите предложенный материал и вставьте недостающие термины и словосочетания.
Рабочая тетрадь к практическому занятию №7. КАРБОНОВЫЕ КИСЛОТЫ. Студент должен: знать: - эмпирические названия изучаемых предельных карбоновых кислот; - зависимость свойств карбоновых кислот от строения карбоксильной группы и взаимного влияния атомов в молекуле; - области применения карбоновых кислот; - общие способы получения карбоновых кислот; уметь: - составлять формулы карбоновых кислот; - называть их по систематической номенклатуре; - составлять уравнения реакций, подтверждающих химические свойства карбоновых кислот. - решать расчетные задачи по формулам и уравнениям реакций.
Теоретический материал. Задание 1: Изучите предложенный материал и вставьте недостающие термины и словосочетания.
Рассмотрим химические свойства карбоновых кислот на примере уксусной кислоты.
1. Карбоновые кислоты диссоциируют в водном растворе с отщеплением протонов Н+, обусловливающих кислую среду раствора:
Водные растворы карбоновых кислот изменяют окраску индикаторов и являются электролитами. По сравнению с сильными минеральными кислотами (H2SO4, HNO3, HCl) – это слабые кислоты. 2. Карбоновые кислоты реагируют с активными металлами (примерно от Li до Fe в ряду напряжений металлов), выделяя водород:
3. Кислоты реагируют с основными оксидами:
4. Кислоты реагируют с основаниями:
5. Кислоты реагируют с аммиаком на холоду с образованием солей аммония:
Соли аммония карбоновых кислот термически неустойчивые соединения, при нагревании они отщепляют воду и превращаются в амиды кислот:
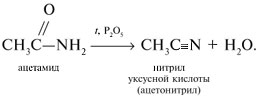
При нагревании амидов с водоотнимающими средствами (например, с пентаоксидом фосфора Р2О5) образуются нитрилы карбоновых кислот:
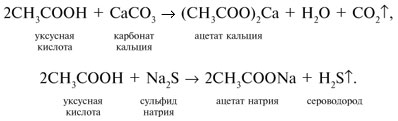
6. Карбоновые кислоты реагируют с солями более слабых и летучих кислот:
7. Кислоты RCOOH реагируют со спиртами R'OH (реакция этерификации) с образованием сложных эфиров RCOOR'. Это обратимая реакция:
8. Кислоты реагируют с хлоридами фосфора РСl3, РСl5, а также с тионилхлоридом SOCl2, обменивая гидроксильную группу на атом хлора:
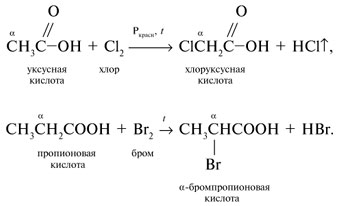
9. Вследствие электроноакцепторного влияния карбоксильной группы СООН атомы водорода при углероде в
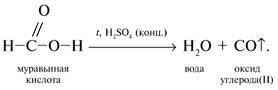
Муравьиная кислота НСООН по химическим свойствам несколько отличается от других карбоновых кислот. Так, для нее неизвестны хлорангидрид и ангидрид. В присутствии водоотнимающих средств (PCl5, SOCl2, H2SO4 (конц.)) муравьиная кислота отщепляет воду с выделением оксида углерода(II):
Из-за наличия в молекуле Н–СООН альдегидного протона муравьиная кислота легко окисляется, в частности дает реакцию «серебряного зеркала»:
Ангидриды карбоновых кислот RC(O)–O–C(O)R получают взаимодействием галогенангидридов с солями карбоновых кислот:
Задача. Для нейтрализации смеси двух соседних членов гомологического ряда двухосновных предельных карбоновых кислот потребовалось 333 мл раствора гидроксида бария с концентрацией 0,09 моль/л, при этом образовалась смесь солей общей массой 7,31 г. Определите, какие вещества входили в состав смеси и в каком количестве.
|


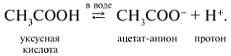
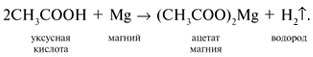
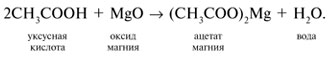
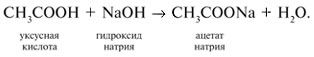
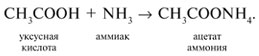
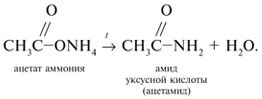
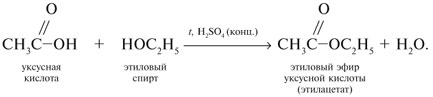

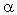 -положении довольно подвижные и могут замещаться на атомы хлора или брома:
-положении довольно подвижные и могут замещаться на атомы хлора или брома: