|
|
|
|
Гетероциклические соединения – это органические вещества, в цикле которых помимо атомов углерода содержатся атомы других химических элементов, называемые гетероатомами. Валентность гетероатомов должна быть не менее двух. Поэтому в их роли чаще всего выступают кислород, азот, сера.
Некоторые соединения с атомами кислорода или азота имеют циклическую структуру. Это циклические ангидриды, циклические сложные эфиры (лактиды и лактоны), циклические амиды (дикетопиперазины и лактамы). Однако данные вещества легко вступают в реакции, сопровождающиеся раскрытием цикла, например, подвергаются гидролизу. Поэтому они не являются истинными гетероциклическими соединениями, для которых характерна высокая прочность цикла.
Значение гетероциклических соединений весьма велико. Они входят в состав многих веществ природного происхождения, участвуют в биохимических процессах, протекающих в организме человека и животных, входят в состав липидов, белков, нуклеиновых кислот, ферментов, витаминов, биологически активных веществ. Более половины всех лекарственных веществ содержит в своей структуре гетероциклы. Почти все алкалоиды имеют гетероциклическую структуру.
Понимание медико-биологических аспектов роли гетероциклических соединений невозможно без глубоких знаний вопросов их строения и свойств.
Учебно-методическое пособие «Биохимия гетероциклических соединений» предназначено для преподавателей, студентов факультета ветеринарной медицины, зооинженерного факультета и факультета заочного обучения. Пособие написано в соответствии с программой курса «Органическая и биологическая химия».
В пособии разбираются строение и свойства гетероциклических соединений с одним и несколькими гетероатомами и имеющие пяти-, шестичленную структуру, а также конденсированную систему циклов. Особое внимание уделяется медико-биологическому значению данных гетероциклических соединений и их важнейших производных.
Для закрепления изучаемого студентами материала в пособии приведены контрольные вопросы и тестовые задания, которые студентам необходимо выполнить по разделу «Гетероциклические соединения».
В конце пособия приведены предметный указатель и список необходимой литературы.
методические рекомендации при изучении раздела «Гетероциклические соединения»
Цель изучения раздела: разобрать строение, свойства и медико-биологическое значение важнейших групп гетероциклических соединений и их производных.
Основные теоретические вопросы при изучении раздела
- Классификация и номенклатура гетероциклических соединений.
- Пятичленные гетероциклы с одним гетероатомом.
- Пятичленные гетероциклы с двумя гетероатомами.
- Шестичленные гетероциклы с одним и двумя гетероатомами азота.
- Гетероциклические соединения с конденсированными системами.
· КЛАССИФИКАЦИЯ И НОМЕНКЛАТУРА ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ
Гетероциклические соединения очень разнообразны. Они различаются общим числом атомов в цикле, количеством и природой самих гетероатомов, степенью насыщенности цикла. Эти различия лежат в основе классификации гетероциклических соединений, которые делятся на группы в зависимости от числа атомов в цикле. Наиболее распространенными являются пяти - и шестичленные гетероциклы с одним и двумя гетероатомами.
Гетероциклические соединения могут быть насыщенными, ненасыщенными и ароматическими. Ненасыщенные гетероциклы встречаются в природных и биологически активных соединениях чаще, чем насыщенные.
Большое значение имеют гетероциклы, конденсированные с бензольным кольцом или с другим гетероциклом.
В зависимости от природы гетероатома различают азот-, кислород- и серусодержащие гетероциклические соединения.
Названия ароматических гетероциклов, как правило, тривиальные, но они приняты номенклатурой ИЮПАК, в том числе и в качестве названий родоначальных структур при построении систематических названий. В номенклатуре ИЮПАК имеются и систематические названия для самих гетероциклов, но они пока мало используются, особенно в химии пяти- и шестичленных гетероциклов.
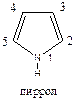
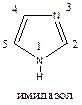

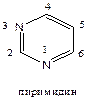

Нумерация атомов в гетероциклах начинается от гетероатома. В гетероциклах с одним гетероатомом атомы углерода иногда обозначаются греческими буквами, начиная от атома углерода, соседнего с гетероатомом, как это показано на примерах пиррола и пиридина. В гетероциклах с несколькими равноценными гетероатомами нумерация проводится так, чтобы гетероатомы получили наименьшие номера. Например, из двух возможных направлений нумерации в случае пиримидина правильным считается такое, при котором атомы азота получают номера 1 и 3, а не 1 и 5. Если имеются два атома азота с различным электронным строением (—N— и —NH—), то нумерацию ведут от —NH—, как это показано на примере имидазола (пурин составляет исключение). В гетероциклах с различными гетероатомами старшим считается кислород, далее сера и затем азот.
Названия производных гетероциклов строятся по общим правилам систематической номенклатуры органических соединений, например 2-метилпиридин (тривиальное название a-пиколин).

· ароматичность ГЕТЕРОЦИКЛИЧЕСКИХ СОЕДИНЕНИЙ
Наибольшее значение представляют пятичленные (пиррол, фуран, тиофен, имидазол, пиразол) и шестичленные (пиридин, пиримидин) ароматические гетероциклические соединения. Они соответствуют критериям ароматичности, т.е. имеют плоский цикл, сопряженную электронную систему, охватывающую все атомы цикла и содержащую согласно правила Хюккеля 4n+2 обобщенных р-электронов.
Пиррол - пятичленный гетероцикл с одним атомом азота. Атомы углерода и азота находятся в нем в sp2-гибридизации (рисунок 1). На негибридной р -орбитали атома азота в пирроле находится неподеленная пара электронов. Она участвует в сопряжении с р -электронами четырех атомов углерода с образованием единого 6 р-электронного облака. Три sp2-гибридные орбитали образуют три s-связи. Атом азота с рассмотренным электронным строением принято называть пиррольным.
В других пятичленных гетероциклах, имеющих один гетероатом (фуран и тиофен) - неподеленная пара электронов соответственно атомов кислорода и серы, так же, как и пиррольного атома азота, включается в сопряжение с р -электронами атомов углерода с образованием единого электронного облака, по числу электронов отвечающего правилу Хюккеля.

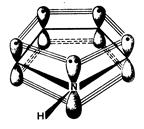
Рисунок 1 - Электронное строение пиррола.
Пиридин представляет собой шестичленный гетероцикл с одним атомом азота и по своему электронному строению напоминает бензол (рисунок 2). Атомы углерода и атом азота находятся в состоянии sp2-гибридизации. Все s-связи (С—С, С—N и С—Н) лежат в одной плоскости. Из трех sp2-гибридных орбиталей две вступают в образование s-связей с двумя атомами углерода, а третья орбиталь содержит неподеленную пару электронов. За счет электрона, находящегося на негибридной р -орбитали, атом азота участвует в образовании единого 6 р-электронного облака с р -электронами пяти атомов углерода. Атом азотас таким электронным строением называют пиридиновым.
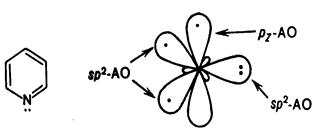
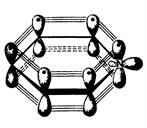
Рисунок 2 - Электронное строение пиридина.
Таким образом, структура пиридина удовлетворяет критериям ароматичности.
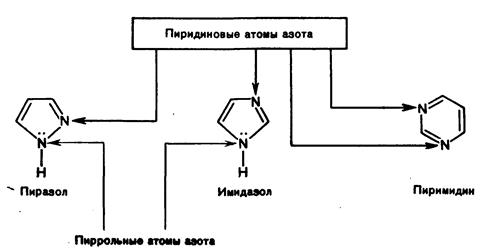
К ароматических гетероциклам, имеющим два гетероатома относятся имидазол, пиразол и пиримидин. В имидазоле и пиразоле один из атомов азота относится к пиррольному типу, а другой - к пиридиновому. Пиррольный атом азота вносит в сопряженную систему два р -электрона, а пиридиновый - один р -электрон. Остальные три р-электрона поставляют три атома углерода.
В пиримидине оба атома азота являются пиридиновыми и предоставляют по одному р -электрону в сопряжение с р -электронами четырех атомов углерода.
· ПЯТИЧЛЕННЫЕ ГЕТЕРОЦИКЛЫ С ОДНИМ ГЕТЕРОАТОМОМ
Среди соединений этой группы наиболее распространены пиррол, фуран и тиофен. Данные вещества относятся к ароматическим, т.к. содержат согласно правилу Хюккеля плоский замкнутый цикл и сопряженную систему, включающую (4n+2) электрона. В этих соединениях сопряженная система имеет 6 электронов: по одному от четырех sp2-гибридизованных атомов углерода и еще два электрона за счет неподеленной пары электронов атома азота (кислорода или серы).
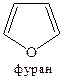

Взаимопревращения между данными соединениями можно отразить схемой:
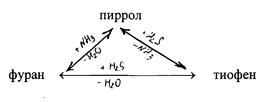
Пиррол представляет собойбесцветная жидкость (т. кип. 130 °С, т. пл. -18 °С) с запахом хлороформа. Он слабо растворим в воде, легко растворяется в большинстве органических растворителей; на воздухе темнеет и постепенно осмоляется. При воздействии на пиррол минеральных кислот образуется полимерная масса темного цвета, не имеющая практического применения. Такая неустойчивость пиррола в сильнокислой среде называется ацидофобностью (что означает «кислотобоязнь»). Эту особенность следует учитывать при экспериментальной работе с пирролом, например проведении реакций электрофильного замещения. Многие из применяемых реагентов являются сильными кислотами, например серная кислота в реакции сульфирования, азотная кислота в реакции нитрования, а в реакции галогенирования опасен выделяющийся галогеноводород.
Пиррол практически лишен основных свойств, так как неподеленная пара электронов азота является составной частью сопряженной системы ароматического кольца.
В реакциях с калием, натрием или амидом натрия NH-группа пиррола проявляет кислотный характер.
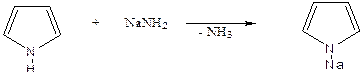
пиррол пирролнатрий
Пиррол как ароматическое соединение склонен к реакциям электрофильного замещения. В этих реакциях атакуются преимущественно α-атомы углерода, где электронная плотность несколько выше, чем на β-атомах углерода. Для устранения прямого действия кислоты реакции осуществляют с помощью реагентов, не содержащих протон.
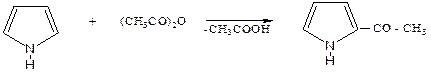
пиррол 2 - ацетилпиррол
Пиррол способен восстанавливаться в присутствии катализаторов (Pd, Pt, Ni и др.) с образованием насыщенного гетероцикла пирролидина. При ступенчатом восстановлении пиррола, например цинком в хлороводородной кислоте, сначала образуется ненасыщенный гетероцикл 3-пирролин, затем пирролидин.

Пирролидин, являющийся циклическим вторичным амином, проявляет более сильные основные свойства, чем аммиак. Цикл пирролидина встречается во многих природных соединениях, особенно растительного происхождения. К ним относятся алкалоиды никотин, атропин, кокаин.

никотин
Пирролидиновое кольцо входит в состав аминокислот пролина и оксипролина, являющихся компонентами ряда белков.

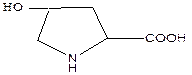
пролин оксипролин
Кольцо пиррола и его производных входит в состав гемсодержащих белков (гемоглобина, миоглобина, цитохромов, каталазы и др.), витамина В12, хлорофилла.

гем
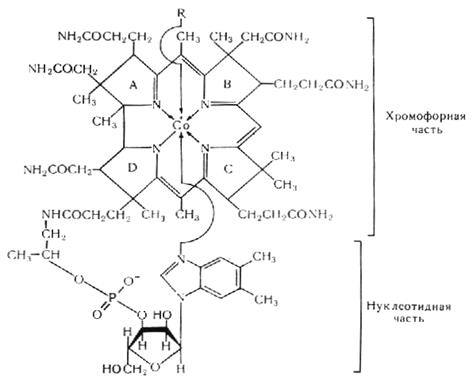
ВИТАМИН В12 (КОБАЛАМИН)
При распаде гемоглобина и ряда других гемопротеинов в организме человека и животных образуется желчный пигмент билирубин, представляющий собой линейную тетрапиррольную структуру.
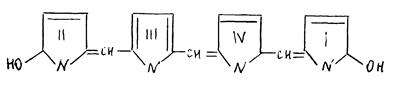
билирубин
Фуран — бесцветная легкокипящая жидкость (т. кип. 31 °С), по растворимости и химическим свойствам напоминающая пиррол. Фуран также ацидофобен и при действии минеральных кислот подвергается полимеризации.
Реакции электрофильного замещения (нитрование, сульфирование, ацилирование) протекают для фурана аналогично рассмотренным для пиррола. При гидрировании фурана в присутствии катализатора образуется тетрагидрофуран, широко используемый как растворитель.
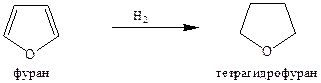
Одним из важнейших производных фурана является фурфурол (фуран-2-карбальдегид). В промышленности его получают в больших количествах из непищевого растительного сырья, содержащего полисахариды (отходы древесины, солома, кукурузная кочерыжка и др.). Фурфурол — маслянистая жидкость (т. кип. 162 °С), имеющая запах ржаного хлеба; именно он и обусловливает аромат свежеиспеченного хлеба.
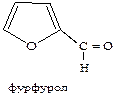
В медицине находят применение производные 5-нитрофурфурола. Они получаются при нитровании фурфурола непосредственно азотной кислотой в присутствии уксусного ангидрида (который блокирует альдегидную группу от легкого окисления) и последующим взаимодействием 5-нитрофурфурола с соединениями, содержащими аминогруппу. Образующиеся при этом имины обладают бактерицидной и некоторыми другими видами физиологической активности. Наиболее часто используемые лекарственные средства этой группы – фурацилин и фуразолидон.

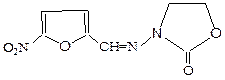
Данные соединения эффективны при гнойно-воспалительных процессах, вызываемых микроорганизмами (дизентерии, брюшном тифе и др.).
Тиофен среди пятичленных гетероциклов с одним гетероатомом в наибольшей степени проявляет ароматические свойства. Он и по физическим свойствам напоминает бензол. Тиофен — бесцветная жидкость (т. кип. 84 °С; у бензола 80 °С), имеющая запах бензола, не растворимая в воде. Тиофен содержится в каменноугольном дегте и легких фракциях нефти, является примесью в техническом бензоле (до 0,5 %).
Тиофен как «π-избыточная» система легче бензола вступает в реакции электрофильного замещения. В отличие от пиррола и фурана, тиофен неацидофобен из-за своей высокой ароматичности. Например, тиофен легко сульфируется концентрированной серной кислотой при комнатной температуре, тогда как бензол в этих условиях с серной кислотой не реагирует. На этом основана очистка технического бензола от примеси тиофена: образовавшаяся тиофен-2-сульфо-кислота, будучи намного полярнее бензола, растворима в серной кислоте, что позволяет легко разделить два слоя — более легкий бензольный и нижний кислотный.
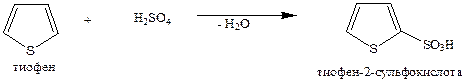
Для тиофена в меньшей степени, чем для пиррола и фурана, характерны реакции с потерей ароматичности, т.е. реакции присоединения, например восстановления.
В медицине и фармации производные тиофена находят ограниченное применение. Они содержатся в препарате ихтиол, который представляет собой сложную смесь веществ, получаемых из сернистых сланцев. Кольцо гидрированного тиофена входит в состав витамина Н (биотина).
- Пятичленные гетероциклы с двумя гетероатомами
Важнейшими представителями этой группы соединений являются гетероциклы, в которых один или оба гетероатома представлены атомами азота. К их числу относятся имидазол, пиразол и тиазол. Эти гетероциклы обладают ароматичностью. Наличие в них второго гетероатома, более электроотрицательного, чем атом углерода, приводит к уменьшению электронной плотности на атомах углерода. Это делает рассматриваемые гетероциклы менее активными в реакциях электрофильного замещения по сравнению с соединениями, имеющими только один гетероатом.

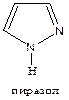
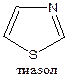
Имидазол (систематическое название 1,3-диазол) — кристаллическое вещество (т. пл, 90°С; т. кип. 256 °С), хорошо растворимое в воде и этаноле.
Имидазол проявляет основные свойства за счет пиридинового атома азота и слабые кислотные свойства за счет пиррольного азота. Следовательно, имидазол как амфотерное соединение способен принимать или отщеплять протон. Подвижность атома водорода NH-группы создает возможность его переноса к пиридиновому атому азота, являющемуся центром основности. Такой перенос протона обуславливает таутомерию имидазола, т. е. его существование в виде таутомерных форм, у которых положения 4 и 5 кольца равноценны. Например, 4- и 5-метилимидазол являются таутомерами, т. е. они настолько легко и быстро переходят один в другой, что выделить их в виде индивидуальных соединений невозможно.
Реакционная способность имидазола в реакциях электрофильного замещения понижена. Например, реакции сульфирования и нитрования протекают с большим трудом, в частности имидазол нитруется в 1010 раз медленнее, чем бензол. Причина этого заключается главным образом в том, что в кислой среде имидазол превращается в имидазолий-катион, который практически невосприимчив к атаке электрофильным реагентом. В реакциях нитрования и сульфирования замещение идет преимущественно в положении 4 или 5.
Производными имидазола, имеющими важное биологическое значение, являются аминокислота гистидин, входящая в состав белков, и ее производное гистамин.
Гистамин для взрослых организмов является заменимой аминокислотой, а для растущих – необходимым фактором питания.
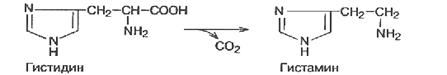
Гистамин образуется в организме человека и животных из гистидина ферментативным путем в результате реакции декарбоксилирования. Он снижает кровяное давление, расширяя стенки кровеносных сосудов, стимулирует секрецию соляной кислоты в желудке, участвует в аллергических реакциях организма.
Конденсированная система бензимидазола входит в состав некоторых биологически активных веществ, например витамина В12, и является основой лекарственного средства дибазола (2-бензилбензимидазола).

Пиразол (1,2-диазол) — кристаллическое вещество (т. пл. 70 °С; т. кип. 187°С), хорошо растворимое в воде, этаноле, эфире. В отличие от имидазола, пиразол и его производные в природе не встречаются, однако на основе пиразола синтезированы многие лекарственные средства.
Химические свойства пиразола во многом подобны свойствам имидазола. Пиразол проявляет одновременно кислотные и основные свойства.
В реакциях электрофильного замещения (сульфирование, нитрование, галогенирование) пиразол ведет себя аналогично имидазолу. Место электрофильной атаки зависит от условий реакции, но чаще всего электрофильный реагент вступает в положение 4 с наибольшей электронной плотностью.
Многие лекарственные средства на основе пиразола являются производными пиразолона-3. К таким соединениям относятся антипирин (1,5-диметил-2-фенилпиразолон-3) и амидопирин (1,5-диметил-4-диметиламино-2-фенилпиразолон-3).
Антипирин, амидопирин, а также водорастворимое сульфопроизводное амидопирина анальгин, применяются как жаропонижающие и болеутоляющие средства. С этой же целью используется производное насыщенного пиразола — бутадион.
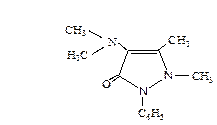
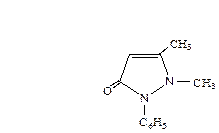
амидопирин антипирин
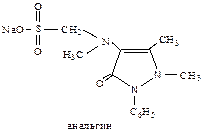

Тиазол (1,3-тиазол) — представитель ароматических гетероциклов с двумя различными гетероатомами. Он обладает слабыми основными свойствами и образует соли с сильными кислотами за счет пиридинового атома азота. Структура тиазола встречается в составе важных биологически активных веществ — тиамина (витамина В1), противомикробного сульфаниламидного препарата норсульфазола.
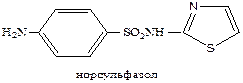
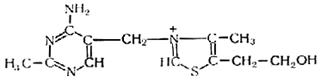
тиамин (витамин В1)
· шестичленные гетрероциклы с одним и двумя
Дата добавления: 2015-09-04; просмотров: 3211. Нарушение авторских прав; Мы поможем в написании вашей работы! |
|
|
|
|
Типы конфликтных личностей (Дж. Скотт) Дж. Г. Скотт опирается на типологию Р. М. Брансом, но дополняет её. Они убеждены в своей абсолютной правоте и хотят, чтобы...
|
МЕТОДИКА ИЗУЧЕНИЯ МОРФЕМНОГО СОСТАВА СЛОВА В НАЧАЛЬНЫХ КЛАССАХ В практике речевого общения широко известен следующий факт: как взрослые...
|




